名校
解题方法
1 . 利用如图的装置(省略部分加热装置)制备 (铋酸钠),已知
(铋酸钠),已知 不溶于冷水且在酸性溶液中迅速分解,
不溶于冷水且在酸性溶液中迅速分解, 是一种难溶于水的白色沉淀。下列说法正确的是
是一种难溶于水的白色沉淀。下列说法正确的是
 (铋酸钠),已知
(铋酸钠),已知 不溶于冷水且在酸性溶液中迅速分解,
不溶于冷水且在酸性溶液中迅速分解, 是一种难溶于水的白色沉淀。下列说法正确的是
是一种难溶于水的白色沉淀。下列说法正确的是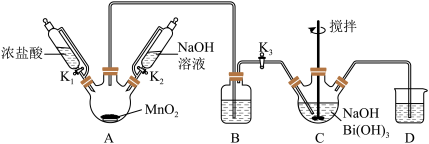
A.装置B应放入饱和 溶液,目的是吸收A中挥发的盐酸 溶液,目的是吸收A中挥发的盐酸 |
B.为使 完全转化为 完全转化为 ,反应过程中应向装置C通入过量 ,反应过程中应向装置C通入过量 |
C.拆除装置前必须进行的操作是关闭 、 、 ,打开 ,打开 |
D.上述反应中若消耗22.4L  则理论上可制得280g 则理论上可制得280g  |
您最近半年使用:0次
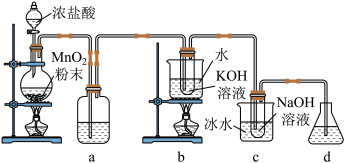
2 . 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。
(1)盛放浓盐酸的仪器名称是___________ ,a的作用为___________ 。
(2)d中可选用试剂___________(填字母)。
(3)浓盐酸与二氧化锰反应的离子方程式是___________ 。
(4)b中采用的加热方式是___________ ,化学反应的离子方程式是___________ 。
(5)c中采用冰水浴冷却的目的是___________ 。
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显___________ 色。可知该条件下KClO3的氧化能力___________ (填“大于”或“小于”)NaClO。
(1)盛放浓盐酸的仪器名称是
(2)d中可选用试剂___________(填字母)。
| A.Na2S | B.NaCl | C.Ca(OH)2 | D.H2SO4 |
(3)浓盐酸与二氧化锰反应的离子方程式是
(4)b中采用的加热方式是
(5)c中采用冰水浴冷却的目的是
(6)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显
您最近半年使用:0次
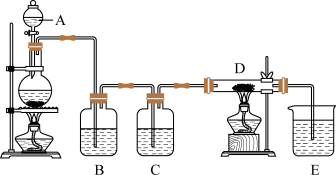
3 . 如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(内置有铁粉)。请回答下列问题:_______ ,烧瓶中反应的化学方程式是_______ 。
(2)装置B中盛放的液体是_______ ,气体通过装置B的目的是_______ 。装置C中盛放的液体是_______ ,气体通过装置C的目的是_______ 。
(3)D中反应的化学方程式是_______ 。
(4)烧杯E中盛放的液体是_______ ,反应的离子方程式是_______ 。
(5)写出工业上用氯气和石灰乳制取漂白粉的化学方程式:_______ 。
(2)装置B中盛放的液体是
(3)D中反应的化学方程式是
(4)烧杯E中盛放的液体是
(5)写出工业上用氯气和石灰乳制取漂白粉的化学方程式:
您最近半年使用:0次
名校
4 . 三氧化二铬 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化:
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。
(1)写出溶液B中的所有阳离子__________ 。写出步骤Ⅱ中生成气体C的离子方程式__________ 。沉淀E的化学式为__________ 。
(2)下列说法正确的是__________。
(3)在碱性条件下, 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式__________ 。根据该反应原理,设计实验检验上述反应后溶液中生成的阴离子__________ 。
 是一种绿色固体,常作颜料。以它为原料实现如下转化:
是一种绿色固体,常作颜料。以它为原料实现如下转化: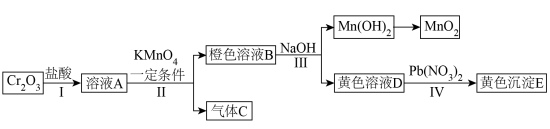
②沉淀E溶于浓的强碱。
③在二价锰盐中,除少数
 、
、 难溶与水外,其余大部分易溶于水。
难溶与水外,其余大部分易溶于水。(1)写出溶液B中的所有阳离子
(2)下列说法正确的是__________。
| A.气体C在工业上可通过电解法制备 |
| B.在溶液B中加入乙醇,溶液变为绿色,再变为蓝色 |
| C.将步骤Ⅰ中的盐酸换成硫酸,仅影响步骤Ⅱ的反应 |
| D.在步骤Ⅲ中,溶液B加入纯碱溶液,也能分离出锰元素 |
(3)在碱性条件下,
 具有强还原剂,可被
具有强还原剂,可被 氧化为最高价,写出两者恰好反应的离子方程式
氧化为最高价,写出两者恰好反应的离子方程式
您最近半年使用:0次
解题方法
5 . 下列离子方程式书写正确的是
A.NaHCO3溶液与NaOH溶液反应: +OH-= +OH-= +H2O +H2O |
| B.氯气与烧碱溶液作用:Cl2+2OH-=2Cl-+H2O |
C.用浓盐酸制取氯气:MnO2+2H++2Cl- Mn2++Cl2↑+H2O Mn2++Cl2↑+H2O |
| D.Fe与Cl2反应:Fe+Cl2=Fe2++2Cl- |
您最近半年使用:0次
名校
解题方法
6 . 在实验室做H2在氯气中燃烧实验中,下列标志的要求不需要的是
A. | B. | C. | D. |
您最近半年使用:0次
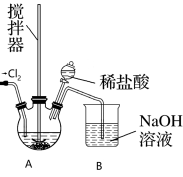
7 . 研究发现,氯化铁在抑制焚烧烟气中高毒性二恶英等氯代芳构化合物的氯化生成机制中具有显著作用。某兴趣小组以废铁屑为原料,用如图所示装置制备 。
。
Ⅰ.废铁屑的处理:取一小烧杯,放入约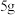 废铁屑,向其中注入
废铁屑,向其中注入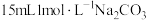 溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
Ⅱ. 溶液的制备:将处理后的废铁屑加入装置
溶液的制备:将处理后的废铁屑加入装置 的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含
的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含 的混合液。
的混合液。
Ⅲ. 溶液的制备:向
溶液的制备:向 的混合液中缓慢通入足量的氯气。
的混合液中缓慢通入足量的氯气。
Ⅳ. 产品的分离提纯:将三颈烧瓶中的溶液转移出来,经过一系列操作,然后过滤、洗涤、重结晶、干燥,得到
产品的分离提纯:将三颈烧瓶中的溶液转移出来,经过一系列操作,然后过滤、洗涤、重结晶、干燥,得到 产品。
产品。
Ⅴ. 产品的纯度测定:用碘量法滴定并计算。
产品的纯度测定:用碘量法滴定并计算。
(1)洗涤废铁屑上的油污时,用热的 溶液效果会更好,结合离子方程式解释原因:
溶液效果会更好,结合离子方程式解释原因:_______ 。
(2)实验室利用 和浓盐酸制备
和浓盐酸制备 的离子方程式为
的离子方程式为_______ ;图中盛装稀盐酸的仪器名称为_______ ,装置B的作用是_______ 。
(3)步骤Ⅳ中的一系列操作是蒸发浓缩、冷却结晶,但蒸发浓缩时要先加入少量盐酸或在 气流中进行,原因是
气流中进行,原因是_______ 。
(4)已知碘量法的滴定反应: 。测定
。测定 产品纯度(设
产品纯度(设 的摩尔质量为
的摩尔质量为 ,杂质不参与反应)的步骤:
,杂质不参与反应)的步骤:
a.用分析天平称取 粗产品;
粗产品;
b.将粗产品配成 溶液;
溶液;
c.用①_______ (填“酸式”或“碱式”)滴定管量取 待测液于锥形瓶中;
待测液于锥形瓶中;
d.加入稍过量的KI溶液,并充分反应;
e.滴加②_______ 作指示剂,用 标准溶液滴定,滴定终点的现象是③
标准溶液滴定,滴定终点的现象是③_______ ;
f.平行滴定三次,消耗标准溶液的平均体积为 ;
;
g.计算 纯度:④
纯度:④_______ (用含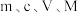 的代数式表示)
的代数式表示) 。
。
 。
。
Ⅰ.废铁屑的处理:取一小烧杯,放入约
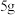 废铁屑,向其中注入
废铁屑,向其中注入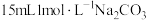 溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。
溶液,浸泡数分钟后,分离出铁屑,洗净、晾干。Ⅱ.
 溶液的制备:将处理后的废铁屑加入装置
溶液的制备:将处理后的废铁屑加入装置 的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含
的三颈烧瓶中,缓慢加入适当过量的稀盐酸,得到含 的混合液。
的混合液。Ⅲ.
 溶液的制备:向
溶液的制备:向 的混合液中缓慢通入足量的氯气。
的混合液中缓慢通入足量的氯气。Ⅳ.
 产品的分离提纯:将三颈烧瓶中的溶液转移出来,经过一系列操作,然后过滤、洗涤、重结晶、干燥,得到
产品的分离提纯:将三颈烧瓶中的溶液转移出来,经过一系列操作,然后过滤、洗涤、重结晶、干燥,得到 产品。
产品。Ⅴ.
 产品的纯度测定:用碘量法滴定并计算。
产品的纯度测定:用碘量法滴定并计算。(1)洗涤废铁屑上的油污时,用热的
 溶液效果会更好,结合离子方程式解释原因:
溶液效果会更好,结合离子方程式解释原因:(2)实验室利用
 和浓盐酸制备
和浓盐酸制备 的离子方程式为
的离子方程式为(3)步骤Ⅳ中的一系列操作是蒸发浓缩、冷却结晶,但蒸发浓缩时要先加入少量盐酸或在
 气流中进行,原因是
气流中进行,原因是(4)已知碘量法的滴定反应:
 。测定
。测定 产品纯度(设
产品纯度(设 的摩尔质量为
的摩尔质量为 ,杂质不参与反应)的步骤:
,杂质不参与反应)的步骤:a.用分析天平称取
 粗产品;
粗产品;b.将粗产品配成
 溶液;
溶液;c.用①
 待测液于锥形瓶中;
待测液于锥形瓶中;d.加入稍过量的KI溶液,并充分反应;
e.滴加②
 标准溶液滴定,滴定终点的现象是③
标准溶液滴定,滴定终点的现象是③f.平行滴定三次,消耗标准溶液的平均体积为
 ;
;g.计算
 纯度:④
纯度:④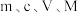 的代数式表示)
的代数式表示) 。
。
您最近半年使用:0次
8 . 下列图示方法能完成相应实验的是

A.用图①配制一定物质的量浓度的 溶液 溶液 |
B.用图②在实验室制取 |
| C.用图③探究碳酸氢钠和碳酸钠的热稳定性 |
D.用图④制备少量 并能较长时间看到其白色时,应先打开止水夹 并能较长时间看到其白色时,应先打开止水夹 C C |
您最近半年使用:0次
9 . 科学探究要实事求是、严谨细致。某化学兴趣小组设计实验进行有关氯化物的探究实验,回答下列问题:
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:___________ 。
(2)装置A中设计g管的作用是___________ 。
(3)装置A中发生反应的离子方程式为___________ 。
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
(4)由实验1、2现象可以得出结论:增大pH,___________ 优先于___________ 放电;
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是___________ ;
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验___________ 作对照实验;
③实验目的ii是___________ ;
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:___________ 。
Ⅰ.FeCl3在工业生产中应用广泛,某化学研究性学习小组模拟工业流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了以Fe粉和Cl2为原料制备无水FeCl3的实验方案,装置示意图如下:
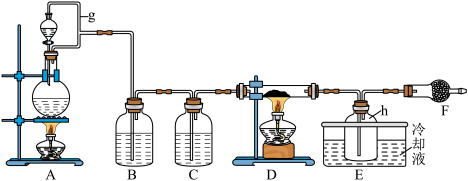
(2)装置A中设计g管的作用是
(3)装置A中发生反应的离子方程式为
Ⅱ.利用惰性电极电解0.1mol/LFeCl2溶液,探究外界条件对电极反应(离子放电顺序)的影响。
实验数据如表所示:
| 实验编号 | 电压/V | pH | 阳极现象 | 阴极现象 |
| 1 | 1.5 | 1.00 | 无气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
| 2 | 1.5 | 5.52 | 无气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 3 | 3.0 | 5.52 | 少量气泡,滴加KSCN显红色 | 无气泡,银白色金属析出 |
| 4 | 4.5 | 5.52 | 大量气泡,滴加KSCN显红色 | 较多气泡,极少量金属析出 |
(4)由实验1、2现象可以得出结论:增大pH,
Ⅲ.为了探究外界条件对氯化铵水解平衡的影响,兴趣小组设计了如下实验方案:
| 实验编号 | c(NH4Cl)/mol·L-1 | 温度/℃ | 待测物理量X | 实验目的 |
| 5 | 0.5 | 30 | a | ___________ |
| 6 | 1.5 | i | b | 探究浓度对氯化铵水解平衡的影响 |
| 7 | 1.5 | 35 | c | ii |
| 8 | 2.0 | 40 | d | 探究温度、浓度同时对氯化铵化解平衡的影响 |
(5)该实验限选药品和仪器:恒温水浴、pH传感器、烧杯、0.1mol/L硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液。
①实验中,“待测物理量X”是
②为了探究浓度对氯化铵水解平衡的影响,实验6可与实验
③实验目的ii是
④氯化铵在生产生活中有很多实用的用途,请写出一种应用:
您最近半年使用:0次
解题方法
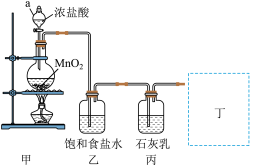
10 . 某兴趣小组模拟工业制漂白粉,设计了如图所示的实验装置。
②温度高时,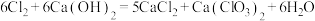 。
。
请回答下列问题:
(1)圆底烧瓶内发生反应的离子方程式为______ ;该反应中的氧化剂是______ ;装置乙中饱和食盐水的作用是______ 。
(2)该小组制得的漂白粉中 的量远大于
的量远大于 的量,其主要原因是
的量,其主要原因是______ ;为提高 的含量,可采取的措施是
的含量,可采取的措施是______ (任写一种即可)。
(3) 是有毒气体,为了防止多余
是有毒气体,为了防止多余 污染空气,可以在丁处用如图装置进行尾气处理,用化学方程式表示该原理
污染空气,可以在丁处用如图装置进行尾气处理,用化学方程式表示该原理______ 。气体应该由______ (填“a”或“b”)口通入。
②温度高时,
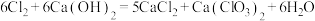 。
。请回答下列问题:
(1)圆底烧瓶内发生反应的离子方程式为
(2)该小组制得的漂白粉中
 的量远大于
的量远大于 的量,其主要原因是
的量,其主要原因是 的含量,可采取的措施是
的含量,可采取的措施是(3)
 是有毒气体,为了防止多余
是有毒气体,为了防止多余 污染空气,可以在丁处用如图装置进行尾气处理,用化学方程式表示该原理
污染空气,可以在丁处用如图装置进行尾气处理,用化学方程式表示该原理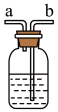
您最近半年使用:0次



