氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
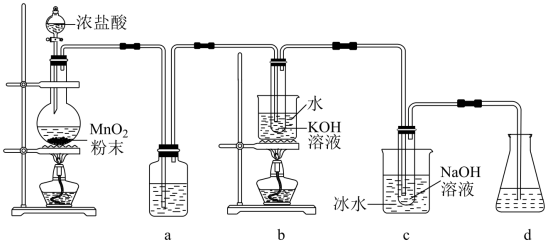
回答下列问题:
(1)盛放MnO2粉末的仪器名称是_______ ,a中的试剂为_______ 。
(2)b中反应的化学方程式为_______ 。
(3)c中反应的离子方程式是_______ ,采用冰水浴冷却的目的是_______ 。
(4)d中可选用试剂_______ (填标号)。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)b中反应的化学方程式为
(3)c中反应的离子方程式是
(4)d中可选用试剂_______ (填标号)。
| A.Na2S溶液 | B.NaCl 溶液 | C.NaOH溶液 | D.H2SO4溶液 |
更新时间:2022-11-19 13:12:20
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】Ⅰ.某化学研究性学习小组为了制取氯气并探究氯水的性质,按图1装置进行实验(加热与夹持装置已略去)。

(1)装置A中仪器a的名称为_______ ;A中发生反应的离子方程式为_______ 。
(2)反应一段时间后,取少量装置C中的溶液于三支试管中,分别进行如下实验:
①向第1支试管中投入有色布条,布条褪色,说明氯水具有_______ 作用;
②向第2支试管中滴入AgNO3溶液,现象为_______ ;
③向第3支试管中加入锌粒,产生气泡的反应的离子方程式为_______ 。
Ⅱ.将图1中A、B装置和图2中的装置(部分夹持装置已略去)连接在一起制备KClO3和NaClO。
已知:常温下氯气与氢氧化钠反应能放出热量。

(3)配平装置D中发生反应的化学方程式:_______
_______Cl2 + _______KOH ______KClO3 + _______KCl + _______H2O。
______KClO3 + _______KCl + _______H2O。
(4)装置E中采用冰水浴冷却的目的为_______ 。
(5)装置F可选用试剂_______ (填标号)。
A.Na2S B.NaCl C.NaOH D.H2SO4

(1)装置A中仪器a的名称为
(2)反应一段时间后,取少量装置C中的溶液于三支试管中,分别进行如下实验:
①向第1支试管中投入有色布条,布条褪色,说明氯水具有
②向第2支试管中滴入AgNO3溶液,现象为
③向第3支试管中加入锌粒,产生气泡的反应的离子方程式为
Ⅱ.将图1中A、B装置和图2中的装置(部分夹持装置已略去)连接在一起制备KClO3和NaClO。
已知:常温下氯气与氢氧化钠反应能放出热量。

(3)配平装置D中发生反应的化学方程式:
_______Cl2 + _______KOH
 ______KClO3 + _______KCl + _______H2O。
______KClO3 + _______KCl + _______H2O。(4)装置E中采用冰水浴冷却的目的为
(5)装置F可选用试剂
A.Na2S B.NaCl C.NaOH D.H2SO4
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】下图表示在没有通风橱的条件下制备氯气时的装置,图中a、b是可控制的弹簧铁夹。(已知:氯气在饱和氯化钠溶液中的溶解度较小。)

(1)仪器A的名称是_________________ ;烧杯中盛放的是___________________ ;烧瓶中发生的反应化学方程式为__________________________ ;
(2)在收集氯气时,应______________________ 。(填:如何操作a、b止水夹,下同),当氯气收集完毕时应____________________ 。
(3)若制得标准状况下的Cl2为0.672L,则被氧化的HCl的物质的量是_________

(1)仪器A的名称是
(2)在收集氯气时,应
(3)若制得标准状况下的Cl2为0.672L,则被氧化的HCl的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组的同学对氯气的制备及性质检验进行了改进。通过下列装置连续完成氯气的制备及漂白性、酸性、氧化性、与金属反应等性质的验证,防止了环境污染,体现了绿色化学思想。

回答下列问题:
(1)按实验设计的意图组装实验仪器,其连接顺序为a______ 。
(2)组装好仪器,检查装置的气密性,并加入相应的化学药品。实验过程中,B中发生反应的化学方程式为______ ;观察到A中的实验现象为______ 。实验结束后,点燃酒精灯加热A,观察到的实验现象可说明氯气水溶液的______ 性是______ (填“可逆”或“不可逆”)的。
(3)实验过程中,D处湿润的石蕊试纸的现象为_____ 。C、D处发生的现象不同,说明______ 。
(4)E处湿润的淀粉KI试纸先变蓝而后变白,由蓝色变白色的化学方程式为______ 。
(5)实验过程中,干燥管G中的实验现象是______ 。
(6)测定实验结束后得到的尾气处理液中NaClO的浓度。实验如下:量取25.00mL实验结束后得到的尾气处理液,加入过量的稀硫酸和过量的KI晶体,振荡,充分反应(已知:ClO-+2I-+2H+=H2O+I2+2Cl-)后稀释至100mL,从中取出25.00mL,加入淀粉溶液作指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点(已知:I2+2S2O =2I-+S4O
=2I-+S4O ),再重复实验两次,测得平均消耗Na2S2O3标准溶液20.00mL。得到的尾气处理液中NaClO的物质的量浓度为
),再重复实验两次,测得平均消耗Na2S2O3标准溶液20.00mL。得到的尾气处理液中NaClO的物质的量浓度为_______ (保留4位小数)。

回答下列问题:
(1)按实验设计的意图组装实验仪器,其连接顺序为a
(2)组装好仪器,检查装置的气密性,并加入相应的化学药品。实验过程中,B中发生反应的化学方程式为
(3)实验过程中,D处湿润的石蕊试纸的现象为
(4)E处湿润的淀粉KI试纸先变蓝而后变白,由蓝色变白色的化学方程式为
(5)实验过程中,干燥管G中的实验现象是
(6)测定实验结束后得到的尾气处理液中NaClO的浓度。实验如下:量取25.00mL实验结束后得到的尾气处理液,加入过量的稀硫酸和过量的KI晶体,振荡,充分反应(已知:ClO-+2I-+2H+=H2O+I2+2Cl-)后稀释至100mL,从中取出25.00mL,加入淀粉溶液作指示剂,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点(已知:I2+2S2O
 =2I-+S4O
=2I-+S4O ),再重复实验两次,测得平均消耗Na2S2O3标准溶液20.00mL。得到的尾气处理液中NaClO的物质的量浓度为
),再重复实验两次,测得平均消耗Na2S2O3标准溶液20.00mL。得到的尾气处理液中NaClO的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】碘单质对动植物的生命极其重要,还可用于医药、照相、染料和系统监测等。某学习小组在实验室中从海藻和油井盐水生产母液中提取碘单质的主要步骤如图1所示:

已知:本实验条件下,氧化性:Cl2>IO >MnO2>I2
>MnO2>I2
回答下列问题:
(1)检验海藻和油井盐水生产母液中含有I-的操作和现象为____ 。
(2)“氧化”时,小组同学选用氯气作氧化剂,装置如图2所示:
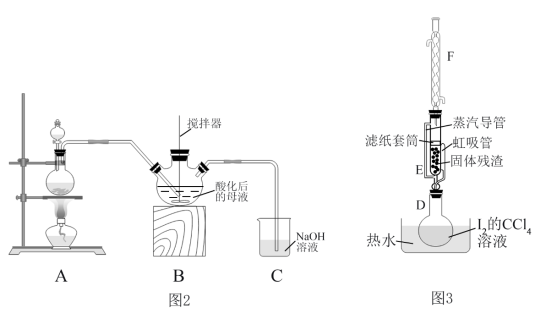
①实验室用装置A制备Cl2时,适合选用的试剂为____ 。
②实验时,控制向装置B中通入Cl2的速率和用量的常用方法为____ ,若Cl2过量,造成的后果为____ (用离子方程式表示),向通入过量Cl2所得的溶液中加入一种试剂,可提高I2的产率,该试剂为____ (填选项字母)。
a.KI b.NaOH c.硝酸
③若用MnO2代替Cl2,优点是____ ,(答出一点即可);缺点是分离出的固体残渣中含有少量I2。小组同学用如图3所示装置进行固体残渣中I2的深度萃取,实验时装置D中溶剂受热蒸发,蒸汽沿蒸汽导管上升至装置F,冷凝后滴入滤纸套筒中,与固体残渣接触进行萃取,液面达到虹吸管顶端时,经虹吸管返回烧瓶。装置F的进水口为____ (填“上口”或“下口”),与常规萃取相比,该萃取装置的优点为____ 。
(3)“蒸馏”时,若加热一段时间后发现忘记加沸石,合理的处理方法为____ 。

已知:本实验条件下,氧化性:Cl2>IO
 >MnO2>I2
>MnO2>I2回答下列问题:
(1)检验海藻和油井盐水生产母液中含有I-的操作和现象为
(2)“氧化”时,小组同学选用氯气作氧化剂,装置如图2所示:

①实验室用装置A制备Cl2时,适合选用的试剂为
②实验时,控制向装置B中通入Cl2的速率和用量的常用方法为
a.KI b.NaOH c.硝酸
③若用MnO2代替Cl2,优点是
(3)“蒸馏”时,若加热一段时间后发现忘记加沸石,合理的处理方法为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某学习小组探究潮湿的Cl2与Na2CO3反应的产物,进行如图实验:

请回答:
(1)试剂X是________ 。
(2)请写出装置A中的化学方程式________ 。
(3)装置C中潮湿的Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和NaCl,试写出该反应化学方程式________ 。
(4)写出氯气进入装置E发生反应的化学方程式________ 。
(5)若将上述装置中的C、D、E部分换成如图所述装置,其中I与III是干燥的有色布条,E中盛装NaOH溶液,请回答下列问题:
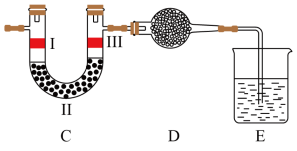
①装置C的作用是验证氯气是否具有漂白性,则装置C中II的作用是________ 。
②D中应装入的物质是________ 。
a.浓硫酸 b.生石灰 c.NaCl固体 d.NaOH固体

请回答:
(1)试剂X是
(2)请写出装置A中的化学方程式
(3)装置C中潮湿的Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和NaCl,试写出该反应化学方程式
(4)写出氯气进入装置E发生反应的化学方程式
(5)若将上述装置中的C、D、E部分换成如图所述装置,其中I与III是干燥的有色布条,E中盛装NaOH溶液,请回答下列问题:

①装置C的作用是验证氯气是否具有漂白性,则装置C中II的作用是
②D中应装入的物质是
a.浓硫酸 b.生石灰 c.NaCl固体 d.NaOH固体
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
(1)由炉渣制备还原铁粉的化学方程式为_______ 。
(2)欲得到更纯的 ,反应①应通入
,反应①应通入_______ (填“过量”或“不足量”)的 气体。
气体。
(3)因为 具有
具有_______ 性(填“氧化”或“还原”),导致商品 中不可避免地存在
中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是_______ 。
(4)一般用 滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准
滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准 溶液滴定其中的
溶液滴定其中的 。反应式:
。反应式: 某次实验称取0.2800g样品,滴定时消耗浓度为0.03000
某次实验称取0.2800g样品,滴定时消耗浓度为0.03000 的
的 溶液25.10mL,则样品中铁含量为
溶液25.10mL,则样品中铁含量为_______ %。
 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
(1)由炉渣制备还原铁粉的化学方程式为
(2)欲得到更纯的
 ,反应①应通入
,反应①应通入 气体。
气体。(3)因为
 具有
具有 中不可避免地存在
中不可避免地存在 。检验其中含有
。检验其中含有 的方法是
的方法是(4)一般用
 滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准
滴定分析法测定还原铁粉纯度。实验步骤:称取一定量样品,用过量稀硫酸溶解,用标准 溶液滴定其中的
溶液滴定其中的 。反应式:
。反应式: 某次实验称取0.2800g样品,滴定时消耗浓度为0.03000
某次实验称取0.2800g样品,滴定时消耗浓度为0.03000 的
的 溶液25.10mL,则样品中铁含量为
溶液25.10mL,则样品中铁含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】自然界地表层存在大量铁、铜的硫化物.现制得含氯化亚铁杂质的氯化铜水溶液,为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按如图步骤进行提纯.
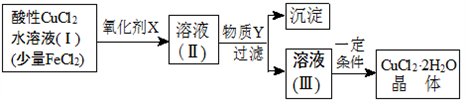
已知Cu2+、Fe3+和Fe2+的氢氧化物开始和完全沉淀时的pH,见表.请回答:
(1)加入氧化剂的目的是___________________________ .
(2)最适合作氧化剂X的是_______ (填序号).
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
在酸性条件下,氧化剂X与Fe2+反应的离子方程式为________________________ .
(3)加入的物质Y以调节溶液pH,Y的化学式是_____ ,pH的范围是 ________ .
(4)只能在HCl气流中加热浓缩才能得到CuCl2•2H2O晶体,HCl气流起的作用是:____________________________
(5)已知Ksp(ZnS)>Ksp(CuS).地表层原生铜的硫化物经氧化、水浸作用后变成CuSO4溶液,再向地下深层渗透,遇到难溶的ZnS慢慢转变为铜蓝(CuS).用离子方程式解释ZnS能转变为CuS的原因__________________________________ .

已知Cu2+、Fe3+和Fe2+的氢氧化物开始和完全沉淀时的pH,见表.请回答:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7 | 4.7 |
| 氢氧化物完全沉淀时的pH | 3.2 | 9 | 6.7 |
(1)加入氧化剂的目的是
(2)最适合作氧化剂X的是
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
在酸性条件下,氧化剂X与Fe2+反应的离子方程式为
(3)加入的物质Y以调节溶液pH,Y的化学式是
(4)只能在HCl气流中加热浓缩才能得到CuCl2•2H2O晶体,HCl气流起的作用是:
(5)已知Ksp(ZnS)>Ksp(CuS).地表层原生铜的硫化物经氧化、水浸作用后变成CuSO4溶液,再向地下深层渗透,遇到难溶的ZnS慢慢转变为铜蓝(CuS).用离子方程式解释ZnS能转变为CuS的原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上常用辉铜矿(主要成分为Cu2S,含有Fe2O3、CaO、SiO2等杂质)制备重要催化剂CuCl。工艺如下:
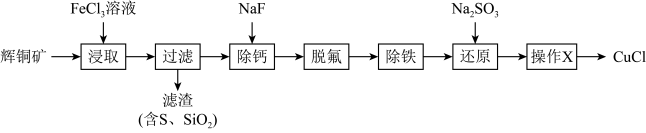
已知:CuCl为难溶于水的白色固体
请回答下列问题:
(1)“浸取”过程中Cu2S转化为可溶性铜盐的离子方程式为:___________ 。
(2)“浸取”是该工艺的第一步,提高浸出率可提高最终产品产率。工程师研究发现单独加入FeCl3溶液时Cu2+浸出率很低,但同时加入FeCl3溶液和H2O2时可提高Cu2+浸出率,其原因可能是_______ 。进一步研究发现,加入H2O2后随温度升高,一定时间后Cu2+浸出率随温度变化的曲线如图。请分析温度高于85℃,Cu2+浸出率下降的原因___________ 。

(3)“除铁”过程为先氧化Fe2+后加入___________ 调节pH于3.2-44之间。
(4)“还原”过程中反应的离子方程式为:___________ 。

已知:CuCl为难溶于水的白色固体
请回答下列问题:
(1)“浸取”过程中Cu2S转化为可溶性铜盐的离子方程式为:
(2)“浸取”是该工艺的第一步,提高浸出率可提高最终产品产率。工程师研究发现单独加入FeCl3溶液时Cu2+浸出率很低,但同时加入FeCl3溶液和H2O2时可提高Cu2+浸出率,其原因可能是

(3)“除铁”过程为先氧化Fe2+后加入
(4)“还原”过程中反应的离子方程式为:
您最近一年使用:0次




