名校
1 . 下列有关物质的分离或鉴别说法正确的是
| A.重结晶法提纯苯甲酸要用的仪器有:漏斗,烧杯,冷凝管 |
| B.分液操作时应先将下层液体从分液漏斗下口放出后再将上层液体继续放出 |
| C.酒精不能萃取水中的溶质,但是能萃取苯中的溶质 |
| D.原子光谱上的特征谱线,可用于元素鉴定 |
您最近一年使用:0次
2024-04-29更新
|
266次组卷
|
2卷引用:名校期中好题汇编-有机物的结构特点
名校
2 . 下列图示的实验装置,不能实现相应实验目的的是
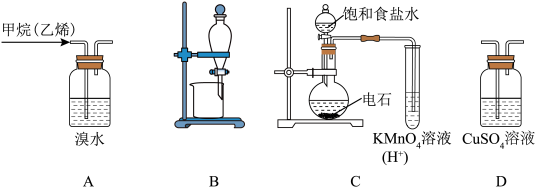
| A.图A:用溴水除去甲烷中的乙烯 |
| B.图B:分离苯和水的混合物 |
| C.图C:检验电石与饱和食盐水的产物乙炔 |
| D.图D:除去乙炔中的硫化氢 |
您最近一年使用:0次
名校
解题方法
3 . 溴苯是一种化工原料,纯净溴苯是一种无色液体,某校学生用如图所示装置进行实验,以探究苯与溴发生反应的原理并分离提纯反应后的产物。请回答下列问题:
(1)装置中冷凝管除导气外,还有___________ 的作用,冷凝水从___________ (填“a”或“b”)口进入。
(2)实验开始时,关闭 ,打开
,打开 和滴液漏斗活塞,滴加
和滴液漏斗活塞,滴加 苯和
苯和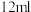 液溴的混合液,反应开始。写出装置Ⅱ发生的主要有机反应的化学方程式
液溴的混合液,反应开始。写出装置Ⅱ发生的主要有机反应的化学方程式___________ ,反应类型___________ ,装置Ⅲ中能说明苯与液溴发生的是此反应类型的现象是___________ 。Ⅲ中小试管内苯的作用是___________ 。
(3)三颈烧瓶内反应后液体呈棕黄色,进行下列实验操作就可得到较纯净的溴苯,正确实验操作顺序是(操作步骤必要时可重复):___________ 。
①用 的
的 溶液洗涤,振荡,分液;
溶液洗涤,振荡,分液;
②通过过滤、蒸馏,可得到无色、较纯净的溴苯 ;
;
③用蒸馏水洗涤,振荡,分液;
④加入无水 粉末干燥
粉末干燥
(4)下列关于苯和溴苯的说法正确的是___________(填字母)。
(5)本实验的产率为___________ (精确到 )。
)。

| 苯 | 溴 | 溴苯 | |
密度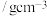 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
| 相对分子量 | 78 | 160 | 157 |
(1)装置中冷凝管除导气外,还有
(2)实验开始时,关闭
 ,打开
,打开 和滴液漏斗活塞,滴加
和滴液漏斗活塞,滴加 苯和
苯和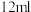 液溴的混合液,反应开始。写出装置Ⅱ发生的主要有机反应的化学方程式
液溴的混合液,反应开始。写出装置Ⅱ发生的主要有机反应的化学方程式(3)三颈烧瓶内反应后液体呈棕黄色,进行下列实验操作就可得到较纯净的溴苯,正确实验操作顺序是(操作步骤必要时可重复):
①用
 的
的 溶液洗涤,振荡,分液;
溶液洗涤,振荡,分液;②通过过滤、蒸馏,可得到无色、较纯净的溴苯
 ;
;③用蒸馏水洗涤,振荡,分液;
④加入无水
 粉末干燥
粉末干燥(4)下列关于苯和溴苯的说法正确的是___________(填字母)。
| A.苯是一种密度比水大、不溶于水、有特殊气味的无色液体 |
| B.仅用水即可鉴别苯和溴苯 |
| C.溴苯中苯是官能团 |
| D.溴苯是非电解质 |
(5)本实验的产率为
 )。
)。
您最近一年使用:0次
名校
解题方法
4 . “中国芯”的发展离不开单晶硅,工业上制高纯硅,先制得粗硅,再制高纯硅。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为___________ 。
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。
① ,
, ;
;
② 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。
请回答下列问题:
(2)装无水氯化钙的仪器名称是___________ 。
(3)若拆去B装置,可能的后果是(写出一个即可)___________ 。
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是___________ (写出一个即可)。 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式:___________ 。利用尾气制备盐酸,宜选择下列装置中的___________ (填序号)。
Ⅰ.请回答:
(1)工业制粗硅反应的化学方程式为
Ⅱ.某小组拟在实验室用如图所示装置模拟探究四氯化硅的制备和应用(夹持装置已省略)。

①
 ,
, ;
;②
 遇水剧烈水解,
遇水剧烈水解, 的熔点、沸点分别为
的熔点、沸点分别为 、
、 。
。请回答下列问题:
(2)装无水氯化钙的仪器名称是
(3)若拆去B装置,可能的后果是(写出一个即可)
(4)有同学最初将E、F、G装置设计成图甲所示装置,图甲装置的主要缺点是


 在高温条件下易分解生成
在高温条件下易分解生成 和
和 。利用
。利用 和
和 制备新型无机非金属材料(
制备新型无机非金属材料( )的装置如图乙,写出该反应的化学方程式:
)的装置如图乙,写出该反应的化学方程式:
您最近一年使用:0次
2024-04-28更新
|
95次组卷
|
2卷引用:四川省内江市威远中学校2023-2024学年高一下学期期中考试化学试题
5 . 氨的常见氢化物有氨 和肼
和肼 。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。
。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。 与水反应可生成
与水反应可生成 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生氢气。
、K)反应产生氢气。 中一个H被
中一个H被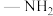 取代,可得
取代,可得 。尿素
。尿素 、
、 和
和 溶液一起反应可制得
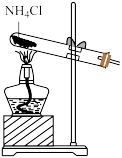
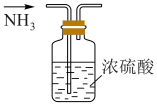
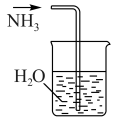
溶液一起反应可制得 。实验室利用下列装置制取收集氨气,能够达到实验目的的是
。实验室利用下列装置制取收集氨气,能够达到实验目的的是
 和肼
和肼 。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。
。氨用于生产硝酸、铵盐、纯碱等。肼具有强还原性,是一种常用的还原剂。 与水反应可生成
与水反应可生成 ,液氨发生微弱电离产生
,液氨发生微弱电离产生 ,液氨能与碱金属(如
,液氨能与碱金属(如 、K)反应产生氢气。
、K)反应产生氢气。 中一个H被
中一个H被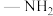 取代,可得
取代,可得 。尿素
。尿素 、
、 和
和 溶液一起反应可制得
溶液一起反应可制得 。实验室利用下列装置制取收集氨气,能够达到实验目的的是
。实验室利用下列装置制取收集氨气,能够达到实验目的的是
|
|
| A.制取氨气 | B.干燥氨气 |
|
|
| C.收集氨气 | D.尾气吸收 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-28更新
|
220次组卷
|
2卷引用:名校期中好题汇编-非金属元素(选择题)
6 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括陶瓷、水泥和玻璃,其中制玻璃的主要原料为_______ 。
(2)下列溶液的存放不能使用磨口玻璃塞的是_______ (填序号)。
①浓硝酸 ② 溶液 ③
溶液 ③ 溶液 ④澄清石灰水 ⑤
溶液 ④澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液
(3)关于硅及其相关化合物的叙述正确的是_______ (填字母)。
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法可知,SiO2+H2O=H2SiO3
C.无机非金属材料AlN熔沸点很高,可作为耐高温材料制作特定仪器
D.保存氢氟酸可用玻璃瓶,但不能用玻璃塞
E. 既能和
既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物
溶液反应,又能和氢氟酸反应,所以是两性氧化物
F.高纯硅可用于制作光导纤维
(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:_______ 。
②上述工艺生产中循环使用的物质除Si、SiHCl3外,还有_______ 。
③整个制备过程必须严格控制无水无氧。 遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式_______ ;在制备高纯硅的过程中若混入 ,可能引起的后果是
,可能引起的后果是_______ 。
(5)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下: 3SiO2+6C+2N2 Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为
Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为_______  。
。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括陶瓷、水泥和玻璃,其中制玻璃的主要原料为
(2)下列溶液的存放不能使用磨口玻璃塞的是
①浓硝酸 ②
 溶液 ③
溶液 ③ 溶液 ④澄清石灰水 ⑤
溶液 ④澄清石灰水 ⑤ 溶液 ⑥
溶液 ⑥ 溶液 ⑦
溶液 ⑦ 溶液
溶液(3)关于硅及其相关化合物的叙述正确的是
A.自然界中存在天然游离的硅单质
B.已知C与Si的最高正价都是正四价,由于CO2+H2O=H2CO3,用类比法可知,SiO2+H2O=H2SiO3
C.无机非金属材料AlN熔沸点很高,可作为耐高温材料制作特定仪器
D.保存氢氟酸可用玻璃瓶,但不能用玻璃塞
E.
 既能和
既能和 溶液反应,又能和氢氟酸反应,所以是两性氧化物
溶液反应,又能和氢氟酸反应,所以是两性氧化物F.高纯硅可用于制作光导纤维
(4)硅单质可作为硅半导体材料。三氯甲硅烷(SiHCl3)还原法是当前制备高纯硅的主要方法,生产过程如图:

②上述工艺生产中循环使用的物质除Si、SiHCl3外,还有
③整个制备过程必须严格控制无水无氧。
 遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式
遇水剧烈反应生成H2SiO3、HCl和一种气体单质,写出发生反应的化学方程式 ,可能引起的后果是
,可能引起的后果是(5)新型陶瓷材料氮化硅(Si3N4)可应用于原子反应堆,一种制备氮化硅的反应如下: 3SiO2+6C+2N2
 Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为
Si3N4+6CO,若生成标准状况下33.6LCO时,反应过程中转移的电子数为 。
。
您最近一年使用:0次
2024-04-27更新
|
82次组卷
|
2卷引用:名校期中好题汇编-非金属元素(非选择题)
7 . 兴趣小组查阅文献后,设计实验对苯酚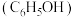 的性质进行探究,回答以下问题。
的性质进行探究,回答以下问题。
已知:ⅰ. 25℃,相关弱酸的电离平衡常数如下:Ka1(H2CO3)=4.2×10−7,Ka2(H2CO3)=5.6×10−11,Ka(C6H5OH)=1.3×10−10。
ⅱ.苯酚与 显色反应的化学方程式为:Fe3++6C6H5OH
显色反应的化学方程式为:Fe3++6C6H5OH [Fe(C6H5O)6]3−(紫色)+6H+。
[Fe(C6H5O)6]3−(紫色)+6H+。
Ⅰ.探究苯酚酸性的强弱
(1)苯酚的电离方程式为___________ 。
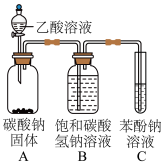
(2)兴趣小组按如图装置进行实验,证明酸性强弱顺序为CH3COOH>H2CO3> C6H5OH,所依据的实验现象为___________ ,C中反应的化学方程式为___________ 。
兴趣小组对以上实验的现象提出猜想。
猜想1: 对铁离子与苯酚的反应有促进作用。
对铁离子与苯酚的反应有促进作用。
猜想2: 对铁离子与苯酚的反应有抑制作用。
对铁离子与苯酚的反应有抑制作用。
(3)向实验1反应后溶液中继续加入 固体,若溶液颜色无变化,则可得出的结论是
固体,若溶液颜色无变化,则可得出的结论是___________ 。
(4)向实验1反应后溶液中加入___________ 固体(填化学式),若溶液颜色变为浅紫色,说明猜想2成立。
(5)兴趣小组同学提出猜想3:溶液的 会影响显色效果,并设计如下实验进行验证。
会影响显色效果,并设计如下实验进行验证。
①实验4中生成的红褐色沉淀是___________ (填化学式)。
②实验5中滴加盐酸至过量,溶液由紫色变为浅黄色,结合平衡移动原理解释原因___________ 。
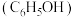 的性质进行探究,回答以下问题。
的性质进行探究,回答以下问题。已知:ⅰ. 25℃,相关弱酸的电离平衡常数如下:Ka1(H2CO3)=4.2×10−7,Ka2(H2CO3)=5.6×10−11,Ka(C6H5OH)=1.3×10−10。
ⅱ.苯酚与
 显色反应的化学方程式为:Fe3++6C6H5OH
显色反应的化学方程式为:Fe3++6C6H5OH [Fe(C6H5O)6]3−(紫色)+6H+。
[Fe(C6H5O)6]3−(紫色)+6H+。Ⅰ.探究苯酚酸性的强弱
(1)苯酚的电离方程式为
(2)兴趣小组按如图装置进行实验,证明酸性强弱顺序为CH3COOH>H2CO3> C6H5OH,所依据的实验现象为
| 实验1 | 实验2 |
|
|
猜想1:
 对铁离子与苯酚的反应有促进作用。
对铁离子与苯酚的反应有促进作用。猜想2:
 对铁离子与苯酚的反应有抑制作用。
对铁离子与苯酚的反应有抑制作用。(3)向实验1反应后溶液中继续加入
 固体,若溶液颜色无变化,则可得出的结论是
固体,若溶液颜色无变化,则可得出的结论是(4)向实验1反应后溶液中加入
(5)兴趣小组同学提出猜想3:溶液的
 会影响显色效果,并设计如下实验进行验证。
会影响显色效果,并设计如下实验进行验证。| 实验 | 操作 | 现象 |
| 3 | 向2mL苯酚溶液(调节 )中滴加0.1mol/LFeCl3溶液 )中滴加0.1mol/LFeCl3溶液 | 溶液显紫色 |
| 4 | 向2mL苯酚溶液(调节 )中滴加0.1mol/LFeCl3溶液 )中滴加0.1mol/LFeCl3溶液 | 生成红褐色沉淀 |
| 5 | 向实验4所得悬浊液中逐滴加入0.1mol/L盐酸至过量 | 沉淀逐渐溶解,溶液变为紫色;继续滴加盐酸,溶液由紫色变为浅黄色 |
②实验5中滴加盐酸至过量,溶液由紫色变为浅黄色,结合平衡移动原理解释原因
您最近一年使用:0次
2024-04-26更新
|
157次组卷
|
2卷引用:北京市北京大学附属中学2023-2024学年高二下学期期中考试化学试题
名校
8 . 海洋资源丰富,从海水中获取镁和溴的流程示意图如下:

| A.从经济效益角度考虑,工业上使用的试剂X是氢氧化钠 |
B.可用 代替 代替 吸收含溴的空气 吸收含溴的空气 |
C.直接将 溶液加热蒸干得无水 溶液加热蒸干得无水 |
| D.虚线框内流程的主要目的是减少环境污染 |
您最近一年使用:0次
2024-04-26更新
|
395次组卷
|
3卷引用:2024届内蒙古自治区赤峰市高三一模化学试题
2024届内蒙古自治区赤峰市高三一模化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)河南省郑州市宇华实验学校2024届高三下学期第三次模拟考试化学试题
9 . 实验小组探究银氨溶液与甲酸(HCOOH,其中C为 价)的反应及银镜产生的原因。
价)的反应及银镜产生的原因。
(1)配制银氨溶液。在洁净的试管中加入适量2% 溶液,逐滴滴入2%氨水,边滴边振荡,至
溶液,逐滴滴入2%氨水,边滴边振荡,至________ ,制得银氨溶液,测得溶液pH略大于7。
(2)进行甲酸的银镜反应实验。
查阅资料:i.银氨溶液中存在平衡: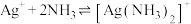

ii.白色AgOH沉淀不稳定,极易分解生成棕黑色
iii.含银元素的部分难溶物(如 、AgCl、
、AgCl、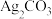 等)可溶于浓氨水,生成
等)可溶于浓氨水,生成
①与实验ii对照,实验i的目的是________ 。
②经检验,实验ii中白色浑浊的主要成分为甲酸银(HCOOAg),推断是甲酸银分解产生银镜,则甲酸银分解的产生的气体中一定含________ 。
③实验iii和实验iv是为了探究pH较高时的银镜反应。实验iv的现象________ (填“能”或“不能”)证明pH较高时是甲酸发生反应产生了银镜。
④甲同学认为实验iii、实验iv中,水浴前的棕黑色浊液中含有银单质,乙同学通过实验排除了这种可能性,其实验操作及实验现象是________ 。
(3)探究实验iv中的含碳产物。取实验iv试管中的产物静置后,取上层清液继续实验:________ 。
②根据上述实验可知,实验iv中银氨溶液与甲酸反应的化学方程式为________ 。
(4)综合以上实验,小组同学得出以下结论:
a.银氨溶液与甲酸反应时,若溶液pH较低,产生银镜的主要原因是甲酸银的分解。
b.银氨溶液与甲酸反应时,若溶液pH较高,产生银镜的原因可能有________________ (写出两点)。
 价)的反应及银镜产生的原因。
价)的反应及银镜产生的原因。(1)配制银氨溶液。在洁净的试管中加入适量2%
 溶液,逐滴滴入2%氨水,边滴边振荡,至
溶液,逐滴滴入2%氨水,边滴边振荡,至(2)进行甲酸的银镜反应实验。
| 编号 | 溶液X | 现象 |
i | 始终无明显现象 | ||
ii | 10滴5%HCOOH溶液 | 加HCOOH后立即产生白色浑浊,测得溶液pH略小于7;水浴开始时白色浊液变为土黄色,随后变黑,有气体产生;最终试管壁附着少量银镜,冷却测得溶液pH略小于5 | |
iii | 5滴10%NaOH溶液和5滴蒸馏水 | 加NaOH后立即产生棕黑色浑浊。最终试管壁附着光亮银镜,冷却测得溶液 | |
iv | 5滴10%NaOH溶液和5滴5%HCOOH溶液 | 加NaOH后立即产生棕黑色浑浊,加HCOOH后沉淀部分溶解。最终试管壁附着光亮银镜,冷却测得溶液 |
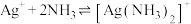

ii.白色AgOH沉淀不稳定,极易分解生成棕黑色

iii.含银元素的部分难溶物(如
 、AgCl、
、AgCl、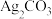 等)可溶于浓氨水,生成
等)可溶于浓氨水,生成
①与实验ii对照,实验i的目的是
②经检验,实验ii中白色浑浊的主要成分为甲酸银(HCOOAg),推断是甲酸银分解产生银镜,则甲酸银分解的产生的气体中一定含
③实验iii和实验iv是为了探究pH较高时的银镜反应。实验iv的现象
④甲同学认为实验iii、实验iv中,水浴前的棕黑色浊液中含有银单质,乙同学通过实验排除了这种可能性,其实验操作及实验现象是
(3)探究实验iv中的含碳产物。取实验iv试管中的产物静置后,取上层清液继续实验:

②根据上述实验可知,实验iv中银氨溶液与甲酸反应的化学方程式为
(4)综合以上实验,小组同学得出以下结论:
a.银氨溶液与甲酸反应时,若溶液pH较低,产生银镜的主要原因是甲酸银的分解。
b.银氨溶液与甲酸反应时,若溶液pH较高,产生银镜的原因可能有
您最近一年使用:0次
2024-04-26更新
|
83次组卷
|
2卷引用:北京市清华大学附属中学2023-2024学年高二下学期期中考试化学试题
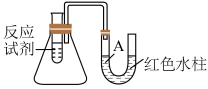
10 . 下图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应。___________ 。
(2)该反应是___________ (填“放热”或“吸热”)反应,结合实验现象写出判断依据___________ 。
(2)该反应是
您最近一年使用:0次
2024-04-25更新
|
59次组卷
|
2卷引用:上海市松江二中2023-2024学年高一下学期期中测试 化学试卷