下图是一个简易测量物质反应是吸热还是放热的实验装置,利用此装置可以很方便地测得某反应是放热反应还是吸热反应。___________ 。
(2)该反应是___________ (填“放热”或“吸热”)反应,结合实验现象写出判断依据___________ 。
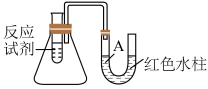
(2)该反应是
更新时间:2024-04-25 16:30:03
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】现有金属单质A(灼烧时,火焰颜色为黄色)与水反应生成物质C和气体甲,甲与黄绿色气体在光照下可反应生成气体丙,丙极易溶于水,且溶液显酸性。请根据以上信息回答下列问题:
(1)写出下列物质的化学式:
A:___________ 、丙:___________ 、C:___________ 。
(2)写出A与水反应的化学方程式:___________ 。
(1)写出下列物质的化学式:
A:
(2)写出A与水反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】按要求回答下列问题。
(1)写出N2的结构式_____ 。
(2)写出氟的原子结构示意图_____ 。
(3)写出钠与水反应的化学方程式_____ 。
(4)写出Na2SO4的电离方程式_____ 。
(5)用电子式表示MgCl2的形成过程_____ 。
(1)写出N2的结构式
(2)写出氟的原子结构示意图
(3)写出钠与水反应的化学方程式
(4)写出Na2SO4的电离方程式
(5)用电子式表示MgCl2的形成过程
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】下列变化中属于吸热反应的是________ . ①液态水汽化 ②将胆矾加热变为白色粉末 ③苛性钠固体溶于水 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰 ⑥干冰升华.
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】原电池是化学对人类的一项重大贡献。实验室为研究原电池原理,将a和b用导线连接,设计如图所示装置。
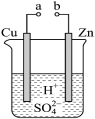
(1)Cu电极为原电池_______ 极(填“正”或“负”),电极反应式为_______ 。
(2)溶液中 移向
移向_______ 极(填“Cu”或“Zn”)。
(3)若工作前两极质量相等,工作一段时间后,导线中通过了1mol 电子,则两极的质量差为_______ g。
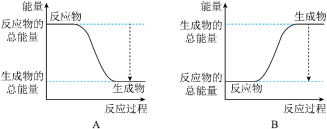
(4)下图能正确表示反应2H2+O2=2H2O中能量变化的是_______ ( 填序号)。

(1)Cu电极为原电池
(2)溶液中
 移向
移向(3)若工作前两极质量相等,工作一段时间后,导线中通过了1mol 电子,则两极的质量差为
(4)下图能正确表示反应2H2+O2=2H2O中能量变化的是

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学反应伴随着能量变化是化学反应的基本特征之一。
(1)已知拆开1molH-H键、1moll-I键、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1molH2和1molI2,反应生成HI会___ (填“放出”或“吸收”)___ kJ的热量。
(2)下列反应中属于放热反应的是___ ,属于吸热反应的是___ 。
①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳⑤食物因氧化而腐败⑥Ba(OH)2•8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
(3)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如图所示。
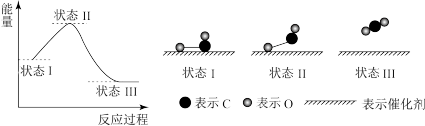
下列说法中正确的是___ 。
A.CO和O生成CO2是放热反应
B.CO和O生成了具有极性共价键的CO2
C.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
(1)已知拆开1molH-H键、1moll-I键、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ。则由1molH2和1molI2,反应生成HI会
(2)下列反应中属于放热反应的是
①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳⑤食物因氧化而腐败⑥Ba(OH)2•8H2O与NH4Cl反应⑦铁粉与稀盐酸反应
(3)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如图所示。

下列说法中正确的是
A.CO和O生成CO2是放热反应
B.CO和O生成了具有极性共价键的CO2
C.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】以下是用MnO2和浓HCl制纯净干燥的Cl2的装置。
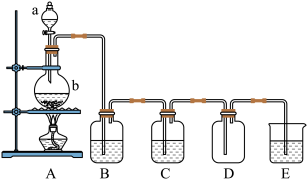
问:
(1)a中盛有___________ b中盛有___________ 。
(2)A中化学方程式____________ 。
(3)B中适宜盛有__________ ,作用是__________ 。
(4)C中盛有_____________ ,作用是_________ 。
(5)E中盛有___________ ,作用___________ 。化学方程式_________ 。

问:
(1)a中盛有
(2)A中化学方程式
(3)B中适宜盛有
(4)C中盛有
(5)E中盛有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】Ⅰ.实验室用下图所示的装置制备并收集纯净、干燥的 。
。

(1)实验室制取 的化学方程式是
的化学方程式是_______ 。
(2)除杂装置①中的试剂是_______ 。
(3)除杂装置②中盛放浓硫酸,其作用是_______ 。
(4)请将收集装置的导气管补充完整。
(5)尾气处理装置中的试剂是_______ 。
Ⅱ.某实验小组用收集到到的氯气制得氯水并对氯水成分和性质进行研究,实验如下:
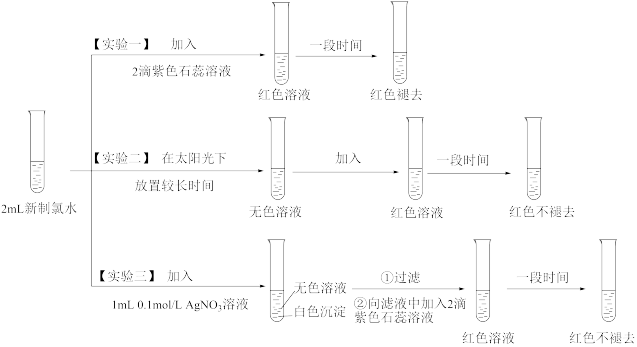
(6)实验一的现象表明,氯水具有酸性和_______ 性。
(7)氯气与水反应的化学方程式为_______ 。
(8)用化学用语说明实验二中“红色不褪去”的原因_______ 。
【实验四】
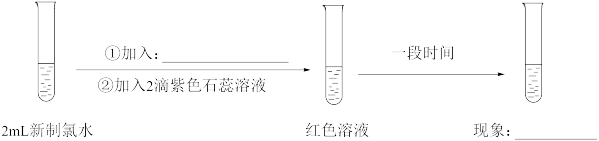
(9)实验四证明了实验三中“红色不褪去”不是因为氯水被稀释,补充所加试剂和现象_______ 。
进一步探究实验三中“红色不褪去”的原因。
【实验五】取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
(10)写出氯水和硝酸银溶液反应的化学方程式_______ 。
 。
。
(1)实验室制取
 的化学方程式是
的化学方程式是(2)除杂装置①中的试剂是
(3)除杂装置②中盛放浓硫酸,其作用是
(4)请将收集装置的导气管补充完整。
(5)尾气处理装置中的试剂是
Ⅱ.某实验小组用收集到到的氯气制得氯水并对氯水成分和性质进行研究,实验如下:

(6)实验一的现象表明,氯水具有酸性和
(7)氯气与水反应的化学方程式为
(8)用化学用语说明实验二中“红色不褪去”的原因
【实验四】

(9)实验四证明了实验三中“红色不褪去”不是因为氯水被稀释,补充所加试剂和现象
进一步探究实验三中“红色不褪去”的原因。
【实验五】取实验三的白色沉淀,洗涤,用饱和氯化钠溶液浸泡,取上层清液,滴加2滴紫色石蕊溶液,一段时间后,颜色褪去。
(10)写出氯水和硝酸银溶液反应的化学方程式
您最近一年使用:0次

 ;②复合膨松剂;③
;②复合膨松剂;③ ;④
;④ 胶体;⑤液态氯化氢;⑥澄清石灰水;⑦
胶体;⑤液态氯化氢;⑥澄清石灰水;⑦ ;⑧金属钠;⑨氨气;⑩酒精,回答下列问题:
;⑧金属钠;⑨氨气;⑩酒精,回答下列问题:

