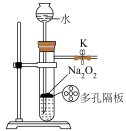
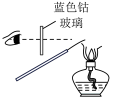
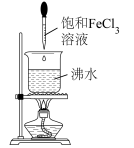
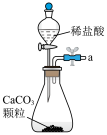
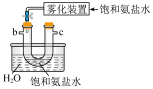
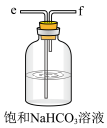
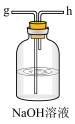
1 . 下列实验设计,不能达到实验目的的是
A.制备少量 | B.除去 中的HCl气体 中的HCl气体 |
|
|
| C.观察钾元素的焰色 | D.制备 胶体 胶体 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
2 . 我国化工专家侯德榜提出“侯氏制碱法”为国际制碱工业做出了重大贡献。他以NaCl、 、
、 等为原料先制得
等为原料先制得 ,进而生产出
,进而生产出 。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备
。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 。实验流程如图:
。实验流程如图:
(1)整个实验流程需要___________ 次过滤操作;能够循环利用的是___________ ;
(2)制备 的总反应的化学方程式为
的总反应的化学方程式为___________ ;
(3)模拟实验时使用下列装置制备 ,请正确的连接装置顺序是
,请正确的连接装置顺序是___________ (按气流方向,用小写字母表示):
(4)上述装置A中反应的离子方程式___________ ,装置B中使用雾化装置的优点是___________ ;装置D的作用是___________ 。
 、
、 等为原料先制得
等为原料先制得 ,进而生产出
,进而生产出 。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备
。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和
和 。实验流程如图:
。实验流程如图: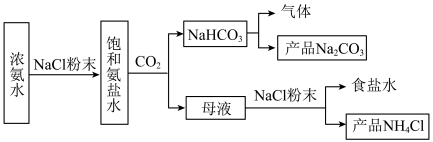
(1)整个实验流程需要
(2)制备
 的总反应的化学方程式为
的总反应的化学方程式为(3)模拟实验时使用下列装置制备
 ,请正确的连接装置顺序是
,请正确的连接装置顺序是
|
|
| |
| A | B | C | D |
您最近一年使用:0次
3 . 某化学课外小组的同学通过实验探究温度和浓度对反应速率的影响。实验原理及方案:在酸性溶液中,KIO3和Na2SO3可发生反应生成I2,生成的I2可用淀粉溶液检验,根据出现蓝色的时间来衡量该反应的速率。
回答下列问题:
(1)实验①③中V1=_______ ,V2=_______ 。
(2)出现蓝色的时间t1与t3大到小关系_______ 。
(3)实验②③的目的是_______ 。
(4)实验中加水的目的是_______ 。
(5)资料显示序号①的反应进行至10 s时,测得Na2SO3溶液的浓度为0.02 mol·L-1,则5 s内消耗Na2SO3的平均速率v(Na2SO3)=_______ 。
| 实验序号 | 0.1 mol·L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.1 mol·L-1Na2SO3溶液的体积/mL | 水的体积/mL | 实验温度/℃ | 出现蓝色的时间/s |
| ① | 5 | 5 | V1 | 5 | t1 |
| ② | 5 | 5 | 30 | 25 | t2 |
| ③ | 5 | V2 | 20 | 25 | t3 |
(1)实验①③中V1=
(2)出现蓝色的时间t1与t3大到小关系
(3)实验②③的目的是
(4)实验中加水的目的是
(5)资料显示序号①的反应进行至10 s时,测得Na2SO3溶液的浓度为0.02 mol·L-1,则5 s内消耗Na2SO3的平均速率v(Na2SO3)=
您最近一年使用:0次
名校
解题方法
4 . 室温下,某同学用下图中装置在通风棚中进行如下实验:
下列说法不正确的是
| 实验 | 现象 |
| 试管Ⅰ中开始无明显现象,后逐渐有微小气泡生成,反应越来越剧烈,试管口上方出现红棕色气体,溶液呈蓝色 |
| 试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色,之后向溶液中持续通入N2,溶液又变为蓝色 |
| A.试管Ⅰ中浅红棕色气体为NO2,由铜还原硝酸生成 |
| B.等质量的Cu完全溶解时,Ⅰ中消耗的HNO3更少 |
| C.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,可能是由于溶有NO2 |
| D.新制的Cu(OH)2悬浊液可用于检验醛基 |
您最近一年使用:0次
5 . 实验室用少量的溴和足量的乙醇制备1,2—二溴乙烷的装置如下图所示:有关数据列表如下:
(1)写出该实验过程中发生的主要反应的化学方程式A处___________ ,D处___________ 。
(2)在装置C中应加入___________ 。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断D处反应已经结束的最简单方法是___________ (填实验现象)。装置B的作用是___________ 。
(4)若产物中有少量未反应的Br2,最好用___________ 洗涤除去。
a.水 b.亚硫酸钠溶液 c.碘化钠溶液 d.乙醇
(5)若产物中有少量副产物乙醚。可用___________ 的方法除去。
(6)反应过程中应用冷水冷却装置D,其主要目的是___________ ;但又不能过度冷却(如用冰水),其原因是___________ 。
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
密度/ | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ |  130 130 | 9 |  116 116 |

(1)写出该实验过程中发生的主要反应的化学方程式A处
(2)在装置C中应加入
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断D处反应已经结束的最简单方法是
(4)若产物中有少量未反应的Br2,最好用
a.水 b.亚硫酸钠溶液 c.碘化钠溶液 d.乙醇
(5)若产物中有少量副产物乙醚。可用
(6)反应过程中应用冷水冷却装置D,其主要目的是
您最近一年使用:0次
名校
6 . 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
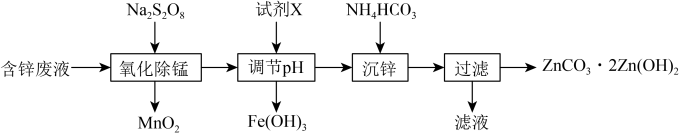
| A.溶液中的Fe2+可以用KSCN溶液检验 |
B.氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、SO |
| C.调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质 |
D.沉锌时的离子方程式为3Zn2++6HCO = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O = ZnCO3·2Zn(OH)2↓+5CO2↑+H2O |
您最近一年使用:0次
名校
7 . 下列对文献的化学解读正确的是
| 选项 | 文献摘录 | 化学解读 |
| A | 《本草纲目拾遗》中记载:“粤中洋行有舶上铁丝……日久起销,用刀刮其销……所刮下之销末,名铁线粉” | 铁在潮湿空气中发生腐蚀形成“铁线粉”,“铁线粉”主要成分是FeO·xH2O |
| B | 《格物粗谈》中记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味” | “气”能使溴水、酸性KMnO4溶液褪色且发生得反应类型相同 |
| C | 《本草衍义》中记载:“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。” | 涉及主要操作是升华 |
| D | 《天工开物》中记载:“凡埏泥造瓦,掘地二尺余,择取无沙粘土而为之”。 | 造瓦过程中只涉及物理变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
8 . 下图是某同学配制 溶液的过程:
溶液的过程:
 溶液的过程:
溶液的过程: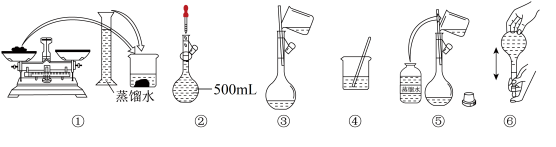
A.如图所示,用托盘直接称量 烧碱 烧碱 |
| B.配制的正确顺序为①④③⑤②⑥ |
| C.②中定容时仰视刻线会导致溶液浓度偏高 |
| D.能用容量瓶贮存配制好的溶液 |
您最近一年使用:0次
名校
解题方法
9 . 实验室以锈蚀程度很大的废铁屑为原料制备 晶体的流程如下:
晶体的流程如下: 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀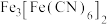 。回答下列问题:
。回答下列问题:
(1)“酸溶”过程中发生的主要反应有:① ;
;
②___________ (用离子方程式表示)
③___________ (用离子方程式表示)
(2)“酸溶”需控制温度在 左右,最佳的加热方式为
左右,最佳的加热方式为___________ 。
(3)“过滤”需要的玻璃仪器除烧杯外还有___________ 。
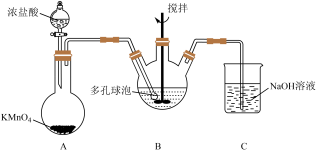
(4)“氧化”过程可在下图所示装置中进行。___________ 。
②装置 中发生的反应离子方程式为
中发生的反应离子方程式为___________ 。
③B中使用多孔球泡的作用是___________ 。
④证明装置 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是___________ 。
 晶体的流程如下:
晶体的流程如下:
 能与
能与 反应生成蓝色沉淀
反应生成蓝色沉淀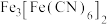 。回答下列问题:
。回答下列问题:(1)“酸溶”过程中发生的主要反应有:①
 ;
;②
③
(2)“酸溶”需控制温度在
 左右,最佳的加热方式为
左右,最佳的加热方式为(3)“过滤”需要的玻璃仪器除烧杯外还有
(4)“氧化”过程可在下图所示装置中进行。
②装置
 中发生的反应离子方程式为
中发生的反应离子方程式为③B中使用多孔球泡的作用是
④证明装置
 溶液中
溶液中 已完全被氧化成
已完全被氧化成 的实验方案是
的实验方案是
您最近一年使用:0次
名校
10 . Ⅰ.淀粉是人类膳食中糖类主要来源,在体内被酶水解为葡萄糖( )供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
)供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
(1)该病人血清葡萄糖GLU的物质的量浓度为__________  。
。
(2)27g葡萄糖中含氢原子数为__________ 。
(3)0.5mol葡萄糖在人体内完全转化为二氧化碳的体积(标准状况)是__________ L。
Ⅱ.现需500mL 0.2mol/L的KI溶液,用KI固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒。
(4)还缺少的仪器有______________________________ (写名称),所需KI固体的质量为__________ g。
(5)在配制过程中,下列操作会导致所配制溶液的浓度偏小的是 。
 )供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:
)供机体利用。某病人血液化验单如图所示,其中葡萄糖测定值明显高于正常值(参考范围)。请回答下列问题:项目 | 测定值 | 单位 | 参考范围 |
血清葡萄糖GLU | 2.16↑ | g/L | 0.65~1.10 |
甘油三酯TG | 2.25↑ | g/L | 5~2.17 |
总胆固醇TCH | 1.79 | g/L | 1.5~2.2 |
 。
。(2)27g葡萄糖中含氢原子数为
(3)0.5mol葡萄糖在人体内完全转化为二氧化碳的体积(标准状况)是
Ⅱ.现需500mL 0.2mol/L的KI溶液,用KI固体配制该溶液时,提供的仪器有:托盘天平、药匙、玻璃棒、烧杯、量筒。
(4)还缺少的仪器有
(5)在配制过程中,下列操作会导致所配制溶液的浓度偏小的是 。
| A.未洗涤烧杯和玻璃棒 |
| B.使用前,容量瓶中有少量蒸馏水 |
| C.定容时俯视凹液面 |
| D.定容摇匀后静置,液面低于刻度线,继续加水至刻度线 |
您最近一年使用:0次