解题方法
1 . 二氧化氯(ClO2)是国内外公认的高效、广谱、快速、安全无毒的杀菌消毒剂,电解法是目前研究最为热门的生产ClO2的方法之一。如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO2的装置。下列说法
不正确的是
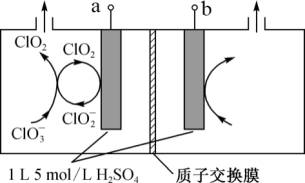
不正确的是

| A.a接电源负极 | B.b极发生氧化反应 |
| C.H从电解池左侧通过质子交换膜移向右侧 | D.阴极的电极反应式为 |
您最近半年使用:0次
名校
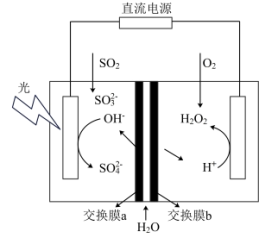
2 . 一种如图所示的光电催化体系,该体系在实现烟气脱 的同时,获得
的同时,获得 。下列说法不正确的是
。下列说法不正确的是
 的同时,获得
的同时,获得 。下列说法不正确的是
。下列说法不正确的是
A.阳极反应为: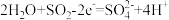 |
| B.该装置将光能和电能转化为化学能 |
C.每生成  ,伴随着 ,伴随着  的生成 的生成 |
| D.交换膜a为阴离子交换膜,b为阳离子交换膜 |
您最近半年使用:0次
3 . 下列叙述正确的是
| A.CO2、NO2、P2O5均为酸性氧化物,CaO、Fe2O3、Na2O2均为碱性氧化物 |
| B.Fe2O3不可与水反应得到Fe(OH)3,但Fe(OH)3能通过化合反应和复分解反应来制取 |
| C.CO2 、SiO2、NO、NO2、SO2都能与强碱反应 |
| D.电解、电泳、电离过程均需要通电才能发生 |
您最近半年使用:0次
4 . 化学与生活密切相关,下列说法错误的是
| A.电动汽车使用的磷酸铁锂电池属于二次电池 |
| B.合成氨工业的原料气须净化以防催化剂“中毒” |
C.浑浊的泥水可用适量饱和 溶液净化 溶液净化 |
D.可直接电解海水获得Mg和 等单质 等单质 |
您最近半年使用:0次
5 . 甲烷是一种能量密度低、难液化、运输成本较高的能源。将甲烷转化成能量密度较高的液体燃料已成为重要的课题。
Ⅰ.直接氧化法制甲醇
(1)已知下列反应的热化学方程式:
反应1: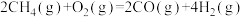

反应2: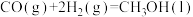
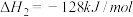
写出甲烷氧化法制甲醇的热化学方程式:______ 。
(2)甲烷氧化过程中的活化能垒如图所示。该方法制备CH3OH产率较低,其原因是______ 。
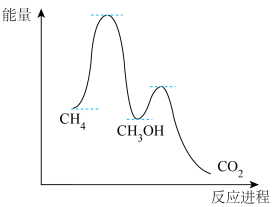
Ⅱ.甲烷的电催化氧化
(3)Hibino科学团队在阳极进行甲烷转化研究,其装置图如图所示,其阳极电极反应式为______ 。

(4)钒(V)物种被认为是形成活性氧物质(如 )的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
)的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是______ 。
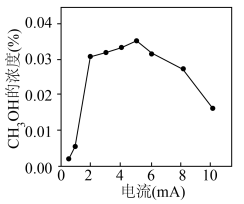
Ⅲ.多相催化剂氧化甲烷法
光照条件下,TiO2负载的Fe2O3多相催化剂合成甲醇时,可将甲醇的选择性(选择性 )提升至90%以上,其反应机理如图所示。
)提升至90%以上,其反应机理如图所示。
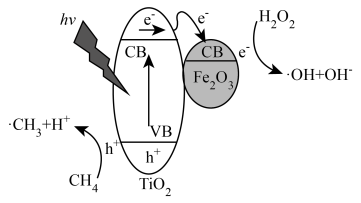
(5)光照时,表面形成的空穴(h+)具有强______ (填“氧化性”或“还原性”)。
(6)写出甲烷通过多相催化剂法制取甲醇的化学方程式______ 。
(7)从反应过程中产生的微粒角度分析,TiO2负载的Fe2O3多相催化剂能将甲醇的选择性提升至90%以上的原因是______ 。
Ⅰ.直接氧化法制甲醇
(1)已知下列反应的热化学方程式:
反应1:
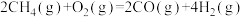

反应2:
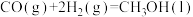
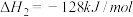
写出甲烷氧化法制甲醇的热化学方程式:
(2)甲烷氧化过程中的活化能垒如图所示。该方法制备CH3OH产率较低,其原因是

Ⅱ.甲烷的电催化氧化
(3)Hibino科学团队在阳极进行甲烷转化研究,其装置图如图所示,其阳极电极反应式为

(4)钒(V)物种被认为是形成活性氧物质(如
 )的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
)的活性位点,V2O5/SnO2作阳极材料时,CH3OH的浓度与电流的关系如图所示,当电流>5mA时,CH3OH的浓度随电流的增加而下降的原因是
Ⅲ.多相催化剂氧化甲烷法
光照条件下,TiO2负载的Fe2O3多相催化剂合成甲醇时,可将甲醇的选择性(选择性
 )提升至90%以上,其反应机理如图所示。
)提升至90%以上,其反应机理如图所示。
(5)光照时,表面形成的空穴(h+)具有强
(6)写出甲烷通过多相催化剂法制取甲醇的化学方程式
(7)从反应过程中产生的微粒角度分析,TiO2负载的Fe2O3多相催化剂能将甲醇的选择性提升至90%以上的原因是
您最近半年使用:0次
名校
6 . 化学与社会、生活息息相关。下列有关叙述错误的是
| A.成都世界大学生运动会大量使用新能源汽车,新能源包括太阳能、生物质能等 |
| B.第19届杭州亚运会主火炬首次采用甲醇作燃料,实现了零碳排放 |
| C.健康生活方式提倡“细嚼慢咽”,唾液酶与食物充分接触,能提高食物转化速率 |
| D.手机成为人们日常生活的必备工具,手机充电过程是将电能转化成化学能的过程 |
您最近半年使用:0次
名校
7 . 通过化学的方法实现 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径。
减排途径。
Ⅰ.利用酸性水溶液电解池在铂电极上捕集 制储氢物质
制储氢物质 。
。
(1) 被
被___________ (填“氧化”或“还原”)为 ,该铂电极为
,该铂电极为___________ 极。
(2)写出该铂电极的电极方程式___________ 。
(3)当电路中转移 电子时,理论上可生成
电子时,理论上可生成
___________ g。
Ⅱ.利用 制备CO
制备CO
一定温度下,在恒容密闭容器中投入一定量 和
和 进行反应:
进行反应:

(4)在恒定温度与容积下,可以提高 平衡转化率的措施有___________。
平衡转化率的措施有___________。
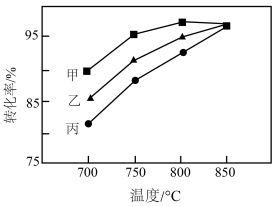
(5)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是___________。
(6)恒容密闭容器中发生上述反应,在投料比 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度T(B)
平衡转化率如图所示。则B和D两点的温度T(B)___________ T(D)(填“<”、“>”或“=”),其原因是___________ 。

Ⅲ.利用制备甲醇
一定条件下,向恒容密闭容器中通入一定量和 ,实际可能发生以下两个反应:
,实际可能发生以下两个反应:
主反应:
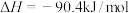
副反应:
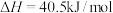
(7)其他条件相同,不同压强下,平衡时 转化率随温度的变化关系如图所示。
转化率随温度的变化关系如图所示。

①压强
___________  (填“<”或“>”)。
(填“<”或“>”)。
②如图中温度高于 时,两条曲线重叠的原因是:
时,两条曲线重叠的原因是:___________ 。
 的资源化利用是一种理想的
的资源化利用是一种理想的 减排途径。
减排途径。Ⅰ.利用酸性水溶液电解池在铂电极上捕集
 制储氢物质
制储氢物质 。
。(1)
 被
被 ,该铂电极为
,该铂电极为(2)写出该铂电极的电极方程式
(3)当电路中转移
 电子时,理论上可生成
电子时,理论上可生成
Ⅱ.利用
 制备CO
制备CO一定温度下,在恒容密闭容器中投入一定量
 和
和 进行反应:
进行反应:

(4)在恒定温度与容积下,可以提高
 平衡转化率的措施有___________。
平衡转化率的措施有___________。A.向反应容器中充入 | B.向反应容器中充入 |
| C.添加更有效的催化剂 | D.利用合适试剂干燥混合气体 |
(5)其他条件相同,在甲、乙、丙三种不同催化剂作用下,相同时间内测得氢气转化率随温度变化如图所示。下列说法错误的是___________。

| A.850℃下,该时间段内甲、乙、丙可能均达到平衡 |
| B.700℃下,甲对应的活化能最大 |
| C.一般催化剂既能降低活化能,又能降低过渡态的能量 |
| D.其它条件一定时,随着温度升高,单位体积内活化分子数占比增大 |
(6)恒容密闭容器中发生上述反应,在投料比
 不同、温度不同时,测得相应的
不同、温度不同时,测得相应的 平衡转化率如图所示。则B和D两点的温度T(B)
平衡转化率如图所示。则B和D两点的温度T(B)
Ⅲ.利用制备甲醇
一定条件下,向恒容密闭容器中通入一定量和
 ,实际可能发生以下两个反应:
,实际可能发生以下两个反应:主反应:

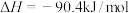
副反应:

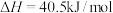
(7)其他条件相同,不同压强下,平衡时
 转化率随温度的变化关系如图所示。
转化率随温度的变化关系如图所示。
①压强

 (填“<”或“>”)。
(填“<”或“>”)。②如图中温度高于
 时,两条曲线重叠的原因是:
时,两条曲线重叠的原因是:
您最近半年使用:0次
名校
8 . 依据《第四章化学反应与电能》所学知识填空。
(1)把___________ 的装置叫做电解池。
(2)金属冶炼就是使矿石中的金属离子___________ 的过程。
(3)金属与其表面接触的一些物质(如O2、Cl2、SO2等)___________ 而引起的腐蚀,叫做化学腐蚀。当___________ 时会发生原电池反应,比较活泼的金属发生氧化反应而被腐蚀,这种腐蚀叫做电化学腐蚀。
(4)由于条件不同,钢铁腐蚀可分为___________ 和___________ 。金属的防护措施包括改变金属材料的组成、___________ 、电化学保护法,其中电化学保护法包括___________ 和___________ 。
(1)把
(2)金属冶炼就是使矿石中的金属离子
(3)金属与其表面接触的一些物质(如O2、Cl2、SO2等)
(4)由于条件不同,钢铁腐蚀可分为
您最近半年使用:0次
9 . 电化学知识在生活中应用广泛,但形成原电池和电解池均需要一定的条件。
(1)现有下列装置:

其中,能构成原电池的是______ (填字母代号),能构成电解池的是______ (填字母代号)。
(2)下列化学方程式正确且能设计成原电池的有______(填字母代号)。
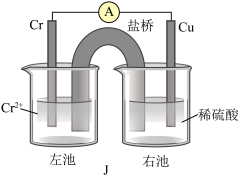
(3)已知Cr比Fe的金属性稍活泼,铜铬构成原电池如装置J所示(盐桥中装的是饱和KCl琼脂溶液)。
则Cr为______ 极(填“正”或“负”),盐桥中 移向
移向______ (填“左池”或“右池”),盛稀硫酸烧杯中的现象为______ 。
(4)甲、乙两同学利用原电池反应检测金属的活动性顺序,设计如下实验装置。
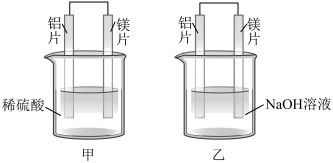
甲装置用______ (填“铝片”或“镁片”)作负极,两同学实验现象的不同之处为______ ,由此得出不能简单根据金属的活动性来判断原电池的正负极的结论,正确的判断方法是______ 。
(1)现有下列装置:

其中,能构成原电池的是
(2)下列化学方程式正确且能设计成原电池的有______(填字母代号)。
A. |
B.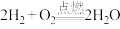 |
C.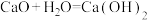 |
D. |
则Cr为
 移向
移向
(4)甲、乙两同学利用原电池反应检测金属的活动性顺序,设计如下实验装置。

甲装置用
您最近半年使用:0次
10 . 下列装置或过程能实现化学能转化为电能的是
 | 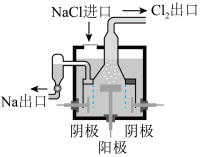 |  |  |
| A.银锌纽扣电池 | B.冶炼金属钠 | C.太阳能电池 | D.天然气燃烧 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



