名校
1 . 化学与生活生产密切相关。下列叙述正确的是
| A.漂白粉与盐酸混合使用可以提升消毒效果 | B.实验室电解水常加入少量稀盐酸增强导电性 |
C.核电站反应堆所用轴棒中含有的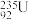 与 与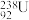 互为同素异形体 互为同素异形体 | D.常用含氟牙膏刷牙可坚周牙齿、预防龋齿 |
您最近半年使用:0次
名校
2 . 我国科研人员研究出了通过电耦合直接将空气转化为硝酸的方法,其反应原理如图所示( 表示自由基,具有强氧化性),下列说法不正确的是
表示自由基,具有强氧化性),下列说法不正确的是
 表示自由基,具有强氧化性),下列说法不正确的是
表示自由基,具有强氧化性),下列说法不正确的是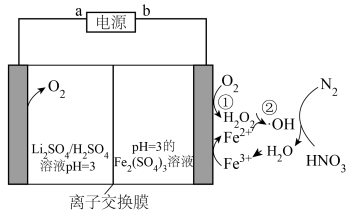
A.与a相连的电极上发生的反应为: |
| B.离子交換膜是阴离子交换膜 |
C.反应②为: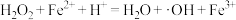 |
D.每生成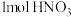 ,阳极产生 ,阳极产生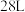 (标准状况下) (标准状况下) |
您最近半年使用:0次
名校
3 . 利用丙酮酸与废水中的 电催化耦合,可在温和条件下去除
电催化耦合,可在温和条件下去除 并生产丙氨酸,其工作原理如图。
并生产丙氨酸,其工作原理如图。 ,丙氨酸主要以
,丙氨酸主要以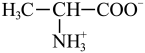 形式存在于溶液中。下列说法错误的是
形式存在于溶液中。下列说法错误的是
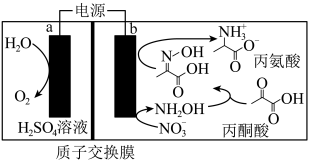
A.电极 连接电源的正极 连接电源的正极 |
B.阴极的电极反应有: |
C.反应一段时间后,阴极区溶液的 基本不变 基本不变 |
D. 极区生成 极区生成 丙氨酸时, 丙氨酸时, 极区至少生成了 极区至少生成了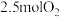 |
您最近半年使用:0次
4 . 甲醇(CH3OH)在化学工业、农业生产等领域有着广泛应用。回答下列问题:
(1)CH3OH的电子式为___________ 。
(2)工业上可将煤先转化为CO(g)和H2(g),然后在催化剂作用下合成CH3OH(l),该过程称为煤的___________ 。已知相关物质的燃烧热数值如下表,则反应CO(g)+2H2(g) CH3OH(l)的∆H=
CH3OH(l)的∆H=___________ 。
(3)常温下,将一定量CH3OH(1)放入真空的恒容密闭中,发生CH3OH(l) CH3OH(g) ∆H=+1109.0kJ·mol-1。
CH3OH(g) ∆H=+1109.0kJ·mol-1。
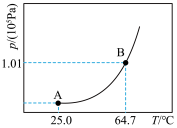
①某温度下,甲醇达到液气平衡状态时的压强称为甲醇在该温度下的饱和蒸气压,记为p*。p*与温度T的关系如图所示,B点蒸气压大于A点蒸气压的原因是___________ 。
i.如图所示,甲烧杯中盛有甲醇,乙烧杯盛有NaOH的甲醇溶液,常温下将两烧杯置于真空密闭容器中,足够长的时间后,可能会观察到___________ (填字母)所示的现象。___________ kPa,馏分中甲醇的物质的量分数为___________ 。
(4)CH3OH可用于制备甲醇燃料电池。
①单位质量燃料所输出电能的多少称为燃料电池的比能量,若某甲醇燃料电池的输出电压为3.60V,其比能量为___________ kW⋅h⋅kg-1(结果保留一位小数)。已知: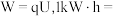 3.6×10⁶J,1mol电子的电量为96500C。
3.6×10⁶J,1mol电子的电量为96500C。
②在实验室中用甲醇燃料电池模拟铝制品在稀硫酸溶液中进行的表面钝化处理,Al电极应与甲醇燃料电池的___________ 极相连,Al电极上发生的电极反应方程式为___________ 。
(1)CH3OH的电子式为
(2)工业上可将煤先转化为CO(g)和H2(g),然后在催化剂作用下合成CH3OH(l),该过程称为煤的
 CH3OH(l)的∆H=
CH3OH(l)的∆H=| 物质 | CO(g) | H2(g) | CH3OH(l) |
| 燃烧热/kJ·mol-1 | -283.0 | -285.8 | -726.5 |
(3)常温下,将一定量CH3OH(1)放入真空的恒容密闭中,发生CH3OH(l)
 CH3OH(g) ∆H=+1109.0kJ·mol-1。
CH3OH(g) ∆H=+1109.0kJ·mol-1。①某温度下,甲醇达到液气平衡状态时的压强称为甲醇在该温度下的饱和蒸气压,记为p*。p*与温度T的关系如图所示,B点蒸气压大于A点蒸气压的原因是
i.如图所示,甲烧杯中盛有甲醇,乙烧杯盛有NaOH的甲醇溶液,常温下将两烧杯置于真空密闭容器中,足够长的时间后,可能会观察到

| 物质 | CH3OH(l) | H2O(1) |
| p*(64.7℃)/kPa | 101.30 | 23.90 |
(4)CH3OH可用于制备甲醇燃料电池。
①单位质量燃料所输出电能的多少称为燃料电池的比能量,若某甲醇燃料电池的输出电压为3.60V,其比能量为
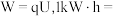 3.6×10⁶J,1mol电子的电量为96500C。
3.6×10⁶J,1mol电子的电量为96500C。②在实验室中用甲醇燃料电池模拟铝制品在稀硫酸溶液中进行的表面钝化处理,Al电极应与甲醇燃料电池的
您最近半年使用:0次
5 . 某种离子型铁的氧化物晶胞如图所示,它由A、B两种正方体单元构成,且两种正方体单元中氧离子的空间位置相同。通过Li+嵌入或脱嵌该晶胞的棱心和体心,可将该晶体设计为纳米硅基锂电池的正极材料 (m、n为正整数)。已知:脱嵌率=
(m、n为正整数)。已知:脱嵌率=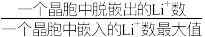 ×100%。
×100%。
 (m、n为正整数)。已知:脱嵌率=
(m、n为正整数)。已知:脱嵌率=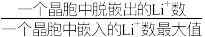 ×100%。
×100%。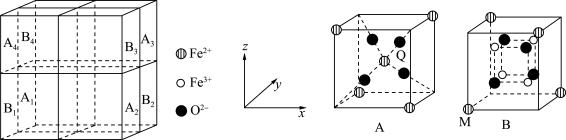
| A.当Li+嵌入晶胞体心和所有棱心,则该锂电池正极材料的化学式为LiFe6O8 |
| B.若该锂电池正极材料中n(Fe2+):n(Fe3+)=5:7则Li+的脱嵌率为75% |
C.该锂电池充电时正极发生的反应为 |
| D.该锂电池放电时,每转移2mol e-,正极材料增重14g |
您最近半年使用:0次
名校
解题方法
6 . 活性氧化锌能对太阳光线和其他大气物质形成防护,常用于敏感皮肤的面霜和化妆品。工业上用菱锌矿(主要成分为ZnCO3,还含有Ni、Cd、Fe、Cu等元素及少量不溶于水的杂质)制备ZnO,工艺流程图所示:___________ ,常温下Fe2+比Fe3+更容易被氧化变质,请从结构角度加以解释___________ 。
(2)加入H2O2的目的是___________ ;“调pH”时除ZnO外还可以选用的物质是___________ 。
a.氨水 b.氢氧化铁 c.氢氧化锌
(3)常温下、pH=5时,Fe3+的浓度降到了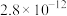 mol/L,此时Fe(OH)3的溶度积常数的数值为
mol/L,此时Fe(OH)3的溶度积常数的数值为___________ 。证明Fe3+已除尽的化学方法是___________ 。
(4)已知沉锌时固体产物是Zn2(OH)2CO3,请写出该过程的离子方程式:___________ 。
(5)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。

(2)加入H2O2的目的是
a.氨水 b.氢氧化铁 c.氢氧化锌
(3)常温下、pH=5时,Fe3+的浓度降到了
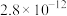 mol/L,此时Fe(OH)3的溶度积常数的数值为
mol/L,此时Fe(OH)3的溶度积常数的数值为(4)已知沉锌时固体产物是Zn2(OH)2CO3,请写出该过程的离子方程式:
(5)粗锌中含有少量Al、Fe、Cu等杂质,可用电解法制备高纯度锌,下列叙述正确的是___________。
| A.粗锌作阳极,纯锌作阴极,电解质溶液是硫酸锌溶液 |
| B.电解过程中,阳极质量的减少与阴极质量的增加相等 |
| C.电解后,溶液中存在的金属阳离子只有Al3+、Fe2+和Zn2+ |
| D.电解后,电解槽底部的阳极泥中只有Cu |
您最近半年使用:0次
7 . 天然气、石油钻探过程会释放出 、
、 等气体。
等气体。
Ⅰ.某种将 和
和 共活化的工艺涉及反应如下:
共活化的工艺涉及反应如下:
①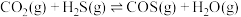

②

③
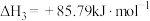
④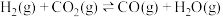
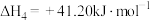
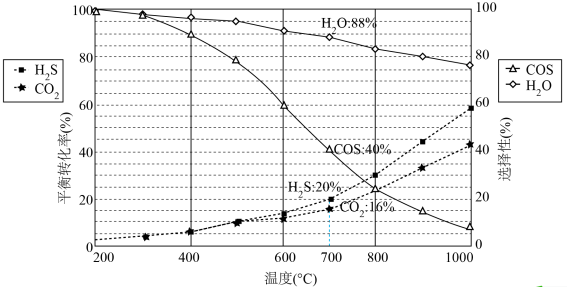
恒压密闭容器中,反应物的平衡转化率、部分生成物的选择性与温度关系如图所示。
已知:ⅰ. 和
和 的初始物质的量相等;
的初始物质的量相等;
ⅱ.COS的选择性 ,
, 的选择性
的选择性 ;
;
ⅲ.产率=转化率×选择性。
(1)
_______ 。
(2)温度高于 时,
时, 的转化率大于
的转化率大于 ,原因是
,原因是_______ 。
(3) 达到平衡时,反应体系中
达到平衡时,反应体系中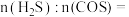
_______ 。
(4)催化剂 对反应②具有高选择性,通过理论计算得到反应的主要路径如下图。
对反应②具有高选择性,通过理论计算得到反应的主要路径如下图。请在答题纸对应区域绘出 过渡态 的示意图
的示意图_______ 。 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,其中电极分别为
的高效去除,其中电极分别为 石墨烯(石墨烯包裹的
石墨烯(石墨烯包裹的 )和石墨烯。过程如图所示:
)和石墨烯。过程如图所示:_______ 。
(6)阳极区发生反应为:
①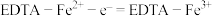 ;
;
②_______ 。
(7)工作时, 石墨烯电极区的
石墨烯电极区的 基本保持不变,原因是
基本保持不变,原因是_______ 。
 、
、 等气体。
等气体。Ⅰ.某种将
 和
和 共活化的工艺涉及反应如下:
共活化的工艺涉及反应如下:①
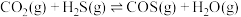

②


③

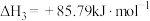
④
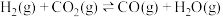
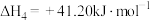
恒压密闭容器中,反应物的平衡转化率、部分生成物的选择性与温度关系如图所示。
已知:ⅰ.
 和
和 的初始物质的量相等;
的初始物质的量相等;ⅱ.COS的选择性
 ,
, 的选择性
的选择性 ;
;ⅲ.产率=转化率×选择性。
(1)

(2)温度高于
 时,
时, 的转化率大于
的转化率大于 ,原因是
,原因是(3)
 达到平衡时,反应体系中
达到平衡时,反应体系中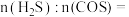
(4)催化剂
 对反应②具有高选择性,通过理论计算得到反应的主要路径如下图。
对反应②具有高选择性,通过理论计算得到反应的主要路径如下图。 的示意图
的示意图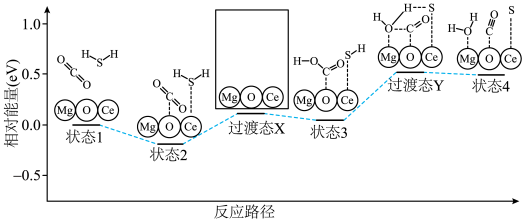
 协同转化装置,实现对天然气中
协同转化装置,实现对天然气中 和
和 的高效去除,其中电极分别为
的高效去除,其中电极分别为 石墨烯(石墨烯包裹的
石墨烯(石墨烯包裹的 )和石墨烯。过程如图所示:
)和石墨烯。过程如图所示: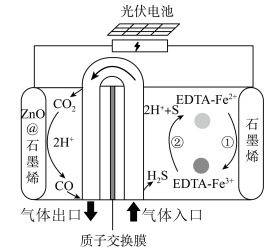
(6)阳极区发生反应为:
①
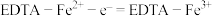 ;
;②
(7)工作时,
 石墨烯电极区的
石墨烯电极区的 基本保持不变,原因是
基本保持不变,原因是
您最近半年使用:0次
解题方法
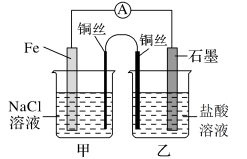
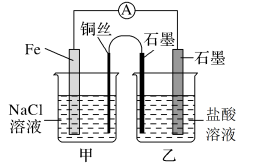
8 . 某化学兴趣小组同学对电化学原理进行了一系列探究活动。
(1)如图,为某化学兴趣小组依据氧化还原反应:___________ (用离子方程式表示)设计的原电池装置,当导线中通过0.5mol电子的电量时,理论上石墨电极上产生气体体积为___________ L(标准状况下)。

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了___________ 腐蚀(填“吸氧”或“析氢”),试写出使酚酞溶液变红的电极反应式为___________ 。
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为___________ 极(填“正”、“负”、“阴”或“阳”),乙装置中总反应的离子方程式为___________ ,该反应为___________ (填“自发”或“非自发”)的氧化还原反应。___________ ,产物常用___________ 检验,一段时间后,乙装置中溶液pH___________ (填“变大”、“变小”或“不变”)。
(1)如图,为某化学兴趣小组依据氧化还原反应:

(2)该实验小组的同学发现,用吸管吸出铁片附近溶液少许置于试管中,滴加几滴酚酞试剂,溶液变红,针对这一现象,某同学的假设是:铁电极材料不纯(材料中含有碳杂质),所以发生了
(3)如图其他条件不变,若将盐桥换成n型铜丝,一段时间后,乙装置中石墨为
您最近半年使用:0次
解题方法
9 . 以次氯酸盐为有效成分的消毒剂应用广泛。电解 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生
①生成 的反应包括:
的反应包括: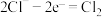 、
、 、
、___________ 。
②测所得溶液 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是___________ 。
(2)相同温度下,在不同初始 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:
Ⅰ. 时,
时, 的溶解度减小
的溶解度减小
Ⅱ. 时,___________
时,___________
①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是___________ 。
②补全猜想Ⅱ,经过检验,推测Ⅱ成立___________ 。
根据上述实验,说明电解法制备 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。
(3)用同样方法电解 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:___________ 。
【测量】
(4)取 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用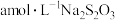 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
___________  。
。
 溶液制备
溶液制备 溶液的装置示意如下。
溶液的装置示意如下。
(1)产生

①生成
 的反应包括:
的反应包括: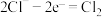 、
、 、
、②测所得溶液
 ,试纸先变蓝
,试纸先变蓝 后褪色,说明溶液具有的性质是
后褪色,说明溶液具有的性质是(2)相同温度下,在不同初始
 下电解
下电解 溶液,
溶液, 对
对 浓度影响如下所示。
浓度影响如下所示。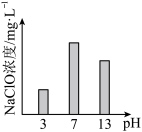
 浓度在
浓度在 为3或13时较小的原因:
为3或13时较小的原因:Ⅰ.
 时,
时, 的溶解度减小
的溶解度减小Ⅱ.
 时,___________
时,___________①根据化学平衡移动原理,推测Ⅰ合理。依据的化学平衡是
②补全猜想Ⅱ,经过检验,推测Ⅱ成立
根据上述实验,说明电解法制备
 溶液,初始
溶液,初始 不宜过小或过大。
不宜过小或过大。(3)用同样方法电解
 溶液制备
溶液制备 ,电解难以持续,推测原因:
,电解难以持续,推测原因:【测量】
(4)取
 所得
所得 样液,加水稀释。依次加入
样液,加水稀释。依次加入 溶液、稀
溶液、稀 。析出的
。析出的 用
用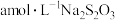 标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗
标准溶液滴定至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗 溶液
溶液 。(已知:
。(已知: )样液中
)样液中
 。
。
您最近半年使用:0次
10 . 国家主席习近平提出了中国应对气候变化的两个目标:二氧化碳排放力争于2030年前达到峰值,于2060年前实现碳中和。杭州亚运会火炬使用的燃料为“零碳甲醇”,是利用焦炉气中的H2与从工业尾气中捕集的二氧化碳反应合成,实现废碳再生、循环内零碳排放。
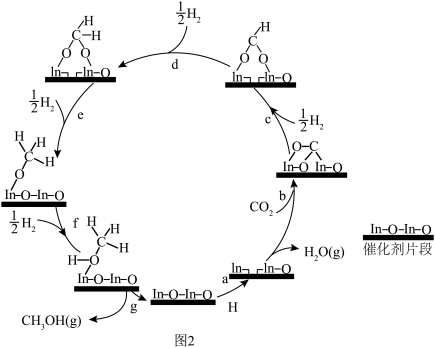
(1)已知:某温度下物质的相对能量如下图1所示,在In2O3催化下用CO2(g)和H2(g)制备CH3OH(g)的反应原理如图2。___________ 。
①该反应在___________ (填“高温”或“低温”)下能自发进行。
②向一绝热恒容密闭容器中充入等物质的量的H2和CO2进行反应,下面不能判断该反应已达到平衡状态的是___________ 。
A混合气体的密度保持不变 B.总压强不变
C.平衡常数不变 D.H2的转化率保持不变
(2)煤制甲醇的生产工艺中,由合成气(组成为H2、CO和少量的CO2)可直接制备甲醇,主要包括以下三个反应:
ⅰ.CO2(g)+H2(g) CO(g)+H2O(g) △H1=+41.1kJ/mol
CO(g)+H2O(g) △H1=+41.1kJ/mol
ⅱ.CO(g)+2H2(g) CH3OH(g) △H1=+90.1kJ/mol
CH3OH(g) △H1=+90.1kJ/mol
ⅲ.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
t℃、100kPa下,将3molH2(g)、1molCO2(g)和6molKr(g)投入一恒容密闭容器中发生反应。反应达到平衡时,测得容器中CH3OH(g)为0.5mol、CO(g)为0.2mol。
①CO2的平衡转化率为___________ 。
②反应ⅱ的平衡常数Kx=___________ (保留位小数)[对于反应aM(g)+bN(g) cZ(g)+dQg),Kx=
cZ(g)+dQg),Kx=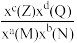 ,x为物质的量分数]。
,x为物质的量分数]。
(3)2023年11月20日,福岛核电站第三批次核污水排放结束,从8月24日正式开启排污,不到三个月的时间,己有超2.3万吨核污水流入太平洋,引发了国际社会的广泛关注和担忧。铀(U)可用作核燃料,核废料中+6价的铀[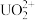 ]可以通过电化学还原法处理,+6价的铀被还原为U4+的电化学装置如图所示:
]可以通过电化学还原法处理,+6价的铀被还原为U4+的电化学装置如图所示:___________ 。
②阴极上可能发生副反应: +3H++2e-=HNO2+H2O、2HNO2+U4+=
+3H++2e-=HNO2+H2O、2HNO2+U4+=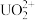 +2NO↑+2H+,为了减少副反应造成的影响,可向阴极区溶液中加入N2H5NO3,发生的反应为:2HNO2+
+2NO↑+2H+,为了减少副反应造成的影响,可向阴极区溶液中加入N2H5NO3,发生的反应为:2HNO2+ =N2O↑+N2↑+3H2O+H+,溶液中加入N2H5NO3的具体作用是
=N2O↑+N2↑+3H2O+H+,溶液中加入N2H5NO3的具体作用是___________ 。
③电还原处理+6价的铀转移1rnole-,阴极区H+减少___________ mol(不考虑副反应)。
(1)已知:某温度下物质的相对能量如下图1所示,在In2O3催化下用CO2(g)和H2(g)制备CH3OH(g)的反应原理如图2。

①该反应在
②向一绝热恒容密闭容器中充入等物质的量的H2和CO2进行反应,下面不能判断该反应已达到平衡状态的是
A混合气体的密度保持不变 B.总压强不变
C.平衡常数不变 D.H2的转化率保持不变
(2)煤制甲醇的生产工艺中,由合成气(组成为H2、CO和少量的CO2)可直接制备甲醇,主要包括以下三个反应:
ⅰ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H1=+41.1kJ/mol
CO(g)+H2O(g) △H1=+41.1kJ/molⅱ.CO(g)+2H2(g)
 CH3OH(g) △H1=+90.1kJ/mol
CH3OH(g) △H1=+90.1kJ/mol ⅲ.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3t℃、100kPa下,将3molH2(g)、1molCO2(g)和6molKr(g)投入一恒容密闭容器中发生反应。反应达到平衡时,测得容器中CH3OH(g)为0.5mol、CO(g)为0.2mol。
①CO2的平衡转化率为
②反应ⅱ的平衡常数Kx=
 cZ(g)+dQg),Kx=
cZ(g)+dQg),Kx=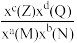 ,x为物质的量分数]。
,x为物质的量分数]。(3)2023年11月20日,福岛核电站第三批次核污水排放结束,从8月24日正式开启排污,不到三个月的时间,己有超2.3万吨核污水流入太平洋,引发了国际社会的广泛关注和担忧。铀(U)可用作核燃料,核废料中+6价的铀[
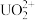 ]可以通过电化学还原法处理,+6价的铀被还原为U4+的电化学装置如图所示:
]可以通过电化学还原法处理,+6价的铀被还原为U4+的电化学装置如图所示: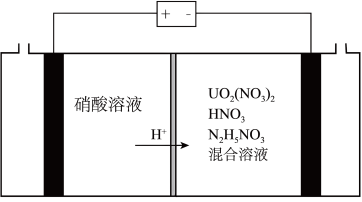
②阴极上可能发生副反应:
 +3H++2e-=HNO2+H2O、2HNO2+U4+=
+3H++2e-=HNO2+H2O、2HNO2+U4+=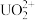 +2NO↑+2H+,为了减少副反应造成的影响,可向阴极区溶液中加入N2H5NO3,发生的反应为:2HNO2+
+2NO↑+2H+,为了减少副反应造成的影响,可向阴极区溶液中加入N2H5NO3,发生的反应为:2HNO2+ =N2O↑+N2↑+3H2O+H+,溶液中加入N2H5NO3的具体作用是
=N2O↑+N2↑+3H2O+H+,溶液中加入N2H5NO3的具体作用是③电还原处理+6价的铀转移1rnole-,阴极区H+减少
您最近半年使用:0次



