某化学兴趣小组在探究次氯酸钠溶液的性质时发现:往过量 FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。请你协助他们完成该反应还原产物的部分探究过程。
(1)溶液变黄,说明反应生成了_________ (离子符号),可以通过加入____________ (试剂名称)进行检验。
(2)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为________ (填微粒)。
(3)你认为甲同学的推测是否正确?____________ (填“正确”或“不正确”).
(4)假设乙同学的推测是正确。写出过量 FeSO4溶液中,滴入几滴NaClO溶液,并加入适量硫酸的离子方程式:___________________________________________________ 。
(1)溶液变黄,说明反应生成了
(2)甲同学推测该反应的还原产物为Cl2;乙同学推测该反应的还原产物为
(3)你认为甲同学的推测是否正确?
(4)假设乙同学的推测是正确。写出
更新时间:2018-12-07 13:30:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】回答问题。
(1)补齐物质与其用途的连线_________ 。
(2)上述 的用途,利用了它的
的用途,利用了它的___________ (填“物理”或“化学”)性质。
(3) 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:___________ 。
| 用途 物质 |
| A.去除某些有机溶剂中的水分 ———— a.Na B.84消毒液的有效成分 b.Na2CO3 C.厨房中的食用䂸 c.Fe3O4 D.打印机墨粉中的磁性成分 d.NaClO E.自来水消毒剂 e.Fe2O3 F.治疗酸酸过多 f.Na2O2 G.用于处理废旧铜板 g.ClO2 H.红色油漆涂料 h.FeCl3 I.呼吸面罩供氧剂 i.NaHCO3 |
(2)上述
 的用途,利用了它的
的用途,利用了它的(3)
 可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
可以去除某些有机溶剂中的水分,用化学方程式解释其原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】数形结合思想是化学学科的重要思维模式,请结合所学知识和图象作答:
I.完成下列问题
(1)如图为含氯元素物质的“价类二维图”,下列说法正确的是___________。

II.某实验小组向100mLFeI2溶液中通入Cl2,溶液中Fe3+、I2的物质的量随通入的Cl2的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:

(2)从开始通入Cl2到n(Cl2)=0.12 mol时,溶液中: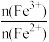 =
=___________ 。
(3)通入足量氯气反应的化学方程式为:___________ 。
III.把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:

(4)A点的沉淀物的化学式为___________ 。
(5)C点消耗HCl溶液的体积为___________ mL。
I.完成下列问题
(1)如图为含氯元素物质的“价类二维图”,下列说法正确的是___________。

| A.乙、丁均属于电解质 |
| B.丙的酸性强于碳酸 |
| C.乙是一种广谱型的消毒剂,可取代甲成为自来水的消毒剂 |
| D.戊→己必须加还原剂才能实现 |
II.某实验小组向100mLFeI2溶液中通入Cl2,溶液中Fe3+、I2的物质的量随通入的Cl2的物质的量变化如图所示(不考虑与水的反应)。请回答下列问题:

(2)从开始通入Cl2到n(Cl2)=0.12 mol时,溶液中:
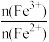 =
=(3)通入足量氯气反应的化学方程式为:
III.把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16g白色沉淀,再向所得悬浊液中逐滴加入1.00mol/LHCl溶液,加入HCl溶液的体积与生成沉淀的关系如图。试回答:

(4)A点的沉淀物的化学式为
(5)C点消耗HCl溶液的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯气是一种重要的化工原料,在生产和生活中的应用十分广泛,可用于制漂白剂等。
(1)实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为_____ 。
(2)氯气的氧化性较强,可以氧化 ,该反应的离子方程式为
,该反应的离子方程式为_____ 。
(3)新制氯水成分复杂,其中含有的离子有_____ ,新制氯水具有漂白性的原因是含有_____ 。
(4)工业上将 通入
通入 溶液中可制备次氯酸钠。
溶液中可制备次氯酸钠。 属于
属于_____ (填“酸”“盐”“氧化物”),制备 的化学方程式为
的化学方程式为_____ 。
(5)氯气可在高温下与焦炭、 发生反应,生成
发生反应,生成 与一种可燃性气体,该反应的化学方程式为
与一种可燃性气体,该反应的化学方程式为_____ ,该反应中氧化产物与还原产物的物质的量之比为_____ 。
(1)实验室可用二氧化锰与浓盐酸制备氯气,反应的离子方程式为
(2)氯气的氧化性较强,可以氧化
 ,该反应的离子方程式为
,该反应的离子方程式为(3)新制氯水成分复杂,其中含有的离子有
(4)工业上将
 通入
通入 溶液中可制备次氯酸钠。
溶液中可制备次氯酸钠。 属于
属于 的化学方程式为
的化学方程式为(5)氯气可在高温下与焦炭、
 发生反应,生成
发生反应,生成 与一种可燃性气体,该反应的化学方程式为
与一种可燃性气体,该反应的化学方程式为
您最近一年使用:0次
【推荐1】以氧化还原反应为主题的高中化学是化学学科中的一大重要内容,通过深入研究氧化还原反应,可以更好地理解和应用化学知识,为实际生活和工程技术的发展提供支持。
(1)人体正常的血红蛋白中含有 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 则导致血红蛋白中的
则导致血红蛋白中的 转换为
转换为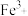 而中毒,可以服用维生素C解毒,下列对此过程叙述错误的是________
而中毒,可以服用维生素C解毒,下列对此过程叙述错误的是________
(2)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,以永远会激励着我们去奋发图强.黑火药在发生爆炸时,发生如下的反应: .其中被还原的元素是
.其中被还原的元素是_________ ,还原剂是____________ ,
(3)已知铜在常温下能被稀 溶解,反应为
溶解,反应为 ,上述反应的离子方程式是
,上述反应的离子方程式是__________ ,在参加反应的硝酸中,起氧化作用的 与起酸性作用的
与起酸性作用的 的质量比为
的质量比为________________ 。
(1)人体正常的血红蛋白中含有
 ,若误食亚硝酸盐(如
,若误食亚硝酸盐(如 则导致血红蛋白中的
则导致血红蛋白中的 转换为
转换为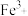 而中毒,可以服用维生素C解毒,下列对此过程叙述错误的是________
而中毒,可以服用维生素C解毒,下列对此过程叙述错误的是________| A.亚硝酸盐被还原 |
| B.亚硝酸盐是还原剂 |
C.维生素C将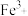 还原为 还原为 |
| D.维生素C被氧化 |
 .其中被还原的元素是
.其中被还原的元素是(3)已知铜在常温下能被稀
 溶解,反应为
溶解,反应为 ,上述反应的离子方程式是
,上述反应的离子方程式是 与起酸性作用的
与起酸性作用的 的质量比为
的质量比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】甲同学计划探究+2价铁的化合物的性质。
(1)实验前甲同学预测:Fe2+肯定既有还原性又有氧化性。你认为甲同学预测的依据是_____ 。
(2)甲同学取少量FeSO4溶液,并滴入几滴酸性 溶液,观察到
溶液,观察到_______ 的现象;若加入活泼金属锌,则溶液颜色会_____ 。
(3)实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质。保存FeCl2溶液的方法是加入_______ 。
(4)乙同学对+2价的 很感兴趣,他查阅到
很感兴趣,他查阅到 应为
应为_____ 色沉淀,但是他将FeSO4溶液与NaOH溶液混合后,该颜色的沉淀现象转瞬即逝,分析原因是(用化学方程式表示)_____ 。
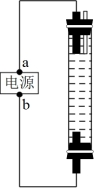
(5)乙同学为了长时间观察到 的生成现象,设计了如图的电解装置。有关该装置说法不正确的是_______。
的生成现象,设计了如图的电解装置。有关该装置说法不正确的是_______。
(1)实验前甲同学预测:Fe2+肯定既有还原性又有氧化性。你认为甲同学预测的依据是
(2)甲同学取少量FeSO4溶液,并滴入几滴酸性
 溶液,观察到
溶液,观察到(3)实际上Fe2+的还原性较强,实验室的FeCl2溶液常因氧化而变质。保存FeCl2溶液的方法是加入
(4)乙同学对+2价的
 很感兴趣,他查阅到
很感兴趣,他查阅到 应为
应为(5)乙同学为了长时间观察到
 的生成现象,设计了如图的电解装置。有关该装置说法不正确的是_______。
的生成现象,设计了如图的电解装置。有关该装置说法不正确的是_______。
| A.a为电源正极,b为电源负极 | B.电解液一定是NaOH溶液 |
| C.两个电极都必须使用铁作电极 | D.阳极发生的电极反应为Fe-2e-=Fe2+ |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】过氧化钠、过氧化镁、过氧化氢都是重要的过氧化物。回答下列问题:
(1)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象:再滴加H2O2,发现溶液变红色,其中包括的反应_____________________ ,_____________________ 。(写离子方程式);继续加H2O2,红色逐渐褪去且有气泡产生,反应原理为:H2O2+SCN-—SO42-+CO2↑+N2↑+H2O+_______ (将方程式补充完成并配平)
(2)过氧化镁不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式__________________________________ 。
(3)高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成含FeO42-高铁酸盐,该反应的化学方程式为_________________________________ 。
(1)取少量含Fe2+、H+溶液于试管中,滴加几滴硫氰酸钾溶液,无明显现象:再滴加H2O2,发现溶液变红色,其中包括的反应
(2)过氧化镁不溶于水,但易溶于稀酸。广泛用作胃药,治疗胃酸过多。试写出过氧化镁与胃酸反应的离子方程式
(3)高温下,过氧化钠在隔绝空气环境中可以将铁单质氧化成含FeO42-高铁酸盐,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某小组同学设计实验实现几种价态硫元素的转化。
任务I:从以下试剂中选择合适的试剂实现S (+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红
(1)写出实现转化的化学方程式_______________
(2)设计实验,证明实现了该转化(写出操作和现象)_______________ 。
II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。
(3)i中加入的物质是__________ ,该转化利用的是SO2的_______ 性质。
(4)写出iii的离子方程式_____________ 。
任务I:从以下试剂中选择合适的试剂实现S (+6)→S(+4)的转化。
试剂清单:①浓H2SO4 ②稀H2SO4 ③酸性KMnO4溶液 ④Na2SO3溶液 ⑤Cu ⑥品红
(1)写出实现转化的化学方程式
(2)设计实验,证明实现了该转化(写出操作和现象)
II:实现硫元素在0、+2、+4价之间的转化。
查阅资料:+2价硫在酸性条件下不稳定,易发生自身氧化还原反应。

(3)i中加入的物质是
(4)写出iii的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】肼(N2H4)是一种重要的液态火箭燃料,具有弱碱性和强还原性.工业上利用尿素[CO(NH2)2]、NaClO在NaOH溶液中发生反应生成水合肼(N2H4•H2O)、Na2CO3等产物.请回答:
(1)上述生成水合肼的反应中尿素是________ ( 填“氧化剂”或“还原剂”),反应的化学方程式为________ .
(2)肼与盐酸反应可生成N2H6Cl2 , N2H6Cl2的水溶液显________ 性( 填“酸”或“碱”或“中”),用离子方程式表示其原因________ .
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式________ .
若要设计实验方案检验上述反应生成固体产物中的金属阳离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中; ②________
(1)上述生成水合肼的反应中尿素是
(2)肼与盐酸反应可生成N2H6Cl2 , N2H6Cl2的水溶液显
(3)查资料得,在高温下肼可将锅炉内壁表面的铁锈转化为致密的氧化膜.取3.2g肼与96g该铁锈样品(可看作是Fe2O3)在高温下恰好完全反应生成氮气等产物,写出该反应的化学方程式
若要设计实验方案检验上述反应生成固体产物中的金属阳离子,补充完整下列实验步骤:
①所得固体溶入浓盐酸中; ②
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验室制备少量硫酸亚铁晶体的实验步骤如下:取过量洁净的铁屑,加入20%~30%的稀硫酸溶液,在50℃~80℃水浴中加热至不再产生气泡.将溶液趁热过滤,滤液移至试管中,用橡胶塞塞紧试管口、静置、冷却一段时间后有浅绿色晶体析出,收集产品。
(1)写出该实验制备硫酸亚铁的化学方程式:________________ ;
(2)采用水浴加热的原因是___________________ ;
(3)反应时铁屑过量的目的是(用离子方程式表示)_________________ ;
(4)溶液趁热过滤的原因是__________________ ;
(5)塞紧试管口的目的是______________________ 。
(1)写出该实验制备硫酸亚铁的化学方程式:
(2)采用水浴加热的原因是
(3)反应时铁屑过量的目的是(用离子方程式表示)
(4)溶液趁热过滤的原因是
(5)塞紧试管口的目的是
您最近一年使用:0次



