海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是( ) (填序号)
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。
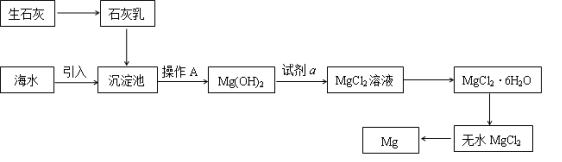
①操作A是_______________________ 。
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为____________________________ 。
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?_____________________________________________ 。
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是( ) (填序号)
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式________________________________ 。
③用CCl4提取碘时除了用CCl4还可以选用的试剂是( ) (填字母序号)
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:________ 。
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为__________________ 。
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
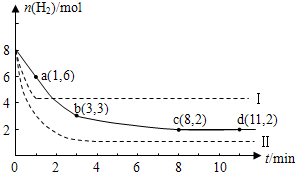
①a点正反应速率_________ (填“大于、等于或小于”)a点逆反应速率。
②平衡时CO2的物质的量浓度是___________ mol/L。
③能够说明该反应达到化学平衡状态的标志是_______ (双选)。
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
(1)无需经过化学变化就能从海水中获得的物质是
A.Cl2 B.淡水 C.烧碱 D.食盐
(2)下图是从海水中提取镁的简单流程。

①操作A是
②无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为
③海水提镁的过程,为什么要将海水中的氯化镁转变为氢氧化镁,再转变为氯化镁?
(3)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
a.坩埚 b.试管 c.蒸发皿 d.烧杯
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
③用CCl4提取碘时除了用CCl4还可以选用的试剂是
a.苯 b.乙醇 c.乙酸
④为检验用CCl4提取碘后的水溶液中是否还含有碘单质。请写出该实验的实验步骤、现象及结论:
(4)利用海底的“可燃冰”制作的燃料电池的总反应式为CH4+2O2+2KOH = K2CO3+3H2O,则该燃料电池的负极的电极反应为
(5)海底的煤经综合利用开发的副产物CO2能生产甲醇燃料,其反应的方程式为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
CH3OH(g)+H2O(g)。某科学实验将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如图实线所示。a,b,c,d括号内数据表示坐标。
①a点正反应速率
②平衡时CO2的物质的量浓度是
③能够说明该反应达到化学平衡状态的标志是
A.单位时间内消耗1molCO2,同时生成3mol H2 B.混合气体的密度不随时间变化
C.CH3OH、H2的浓度不再随时间变化 D.CH3OH和H2O浓度相等
更新时间:2017-07-01 11:52:47
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】有如下化学反应:2A(g)+B(g) 2C(g),△H<0。
2C(g),△H<0。
(1)若将4 mol A和2 mol B在2 L的容器中混合,经2 s后测得C的浓度为0.6 mol/L,用物质A表示的平均反应速率为_____ ;2s时物质B的浓度为__________ ;
(2)若将4 mol A和2 mol B加入体积不变的容器中,一定温度下达到平衡状态,测得气体总物质的量为4.2 mol。此时,混合气体中C的体积分数为__________ ;若再通入少量B气体,体系中A的物质的量_________ (填“增大”、“减小”或“不变”),若要使A的物质的量再达到与原平衡状态相同,可采取的三种措施有__________ 、__________ 、__________
 2C(g),△H<0。
2C(g),△H<0。(1)若将4 mol A和2 mol B在2 L的容器中混合,经2 s后测得C的浓度为0.6 mol/L,用物质A表示的平均反应速率为
(2)若将4 mol A和2 mol B加入体积不变的容器中,一定温度下达到平衡状态,测得气体总物质的量为4.2 mol。此时,混合气体中C的体积分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一定温度下,在2L的密闭容器中,M、N两种气体的物质的量随时间变化的曲线如图所示:
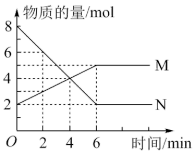
(1)反应的化学方程式为___________ 。
(2)反应达到平衡状态的时间是_______ min,该时间内的平均反应速率v(N)=_______ 。
(3)判断该反应达到平衡状态的依据是___________(填序号)。
(4)能加快反应速率的措施是___________(填序号)。

(1)反应的化学方程式为
(2)反应达到平衡状态的时间是
(3)判断该反应达到平衡状态的依据是___________(填序号)。
| A.该条件下,正、逆反应速率都为零 |
| B.该条件下,混合气体的密度不再发生变化 |
| C.该条件下,混合气体的压强不再发生变化 |
| D.条件下,单位时间内消耗2molN的同时,生成1molM |
| A.升高温度 |
| B.容器容积不变,充入惰性气体Ar |
| C.容器压强不变,充入惰性气体He |
| D.使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学反应的速率和限度对人类生产生活有重要的意义。
I.已知 Na2S2O3H2SO4=Na 2SO4 SSO2H2O 。某同学通过测定该反应发生时溶液变 浑浊的时间,研究外界条件对化学反应速率的影响,进行表中 A、B、C、D 四次实验:
(1)利用此反应进行浓度或温度对反应速率影响的实验中,实验以_______(填选项)时开始计 时,到溶液出现浑浊将锥形瓶底部的“+”字完全遮盖时结束计时。
A.放入水浴中 B.溶液混合 C.开始出现浑浊
(2)其中最先变浑浊的是_______
(3)B 与 D 实验_______ (填“能”或“否”)说明温度对反应速率的影响
(4)在恒温下,向容积为 2L 的恒容容器中加入一定量的碳单质和 2mol H2O (g),发生反应:CsH2OgCOgH2g。2min后,容器的压强增加了20%,则 2min内H2O 的平 均反应速率为_______ mol/( Lmin)。经过一段时间后达到平衡,下列说法正确的是_______ 。
A.增加碳单质的量,可以加快该反应速率
B.2min 时,CO 的体积分数为 1/6
C.2min 时, H2O 的转化率为 20%
D.当混合气体的平均摩尔质量不再变化时可以判断该反应达到了平衡
I.已知 Na2S2O3H2SO4=Na 2SO4 SSO2H2O 。某同学通过测定该反应发生时溶液变 浑浊的时间,研究外界条件对化学反应速率的影响,进行表中 A、B、C、D 四次实验:
| 反应温度 | Na2S2O3 | H2SO4 | H2O | |||
| ℃ | V(mL) | c(mol·L-1) | v(mL) | c(mol·L-1) | V(mL) | |
| A | 10 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 10 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 10 |
(1)利用此反应进行浓度或温度对反应速率影响的实验中,实验以_______(填选项)时开始计 时,到溶液出现浑浊将锥形瓶底部的“+”字完全遮盖时结束计时。
A.放入水浴中 B.溶液混合 C.开始出现浑浊
(2)其中最先变浑浊的是
(3)B 与 D 实验
(4)在恒温下,向容积为 2L 的恒容容器中加入一定量的碳单质和 2mol H2O (g),发生反应:CsH2OgCOgH2g。2min后,容器的压强增加了20%,则 2min内H2O 的平 均反应速率为
A.增加碳单质的量,可以加快该反应速率
B.2min 时,CO 的体积分数为 1/6
C.2min 时, H2O 的转化率为 20%
D.当混合气体的平均摩尔质量不再变化时可以判断该反应达到了平衡
您最近一年使用:0次
【推荐1】已知:A(g)+2B(g)  2C(g),恒温恒压下,在密闭容器中充入1 mol A和2 mol B后的容积为3L。
2C(g),恒温恒压下,在密闭容器中充入1 mol A和2 mol B后的容积为3L。
(1)下列能用于判断该反应达到平衡的是(填字母):__________________ 。
a.A、B的浓度之比为1∶2 b.容器内气体的总物质的量不变
c.容器内气体密度不再变化 d.生成0.2 mol A的同时生成0.2 mol C
(2)平衡后,再向容器中通入1 mol氦气,A的转化率___________ (填“增大”、“不变”、“减小”)。
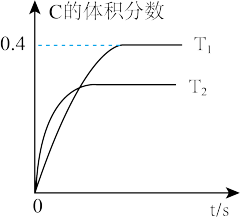
(3)在T1、T2不同温度下,C的体积分数与时间关系如图所示。则T1______ T2(填“大于”或“小于”,下同 ),该反应的△H __________ 0。若在T1下达到平衡,K(T1)=_____ 。(计算结果)
 2C(g),恒温恒压下,在密闭容器中充入1 mol A和2 mol B后的容积为3L。
2C(g),恒温恒压下,在密闭容器中充入1 mol A和2 mol B后的容积为3L。(1)下列能用于判断该反应达到平衡的是(填字母):
a.A、B的浓度之比为1∶2 b.容器内气体的总物质的量不变
c.容器内气体密度不再变化 d.生成0.2 mol A的同时生成0.2 mol C
(2)平衡后,再向容器中通入1 mol氦气,A的转化率
(3)在T1、T2不同温度下,C的体积分数与时间关系如图所示。则T1

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】甲醇是一种重要的化工原料,具有开发和应用的广阔前景。工业上使用水煤气( 与
与 的混合气体)转化成甲醇,反应为
的混合气体)转化成甲醇,反应为 。
。
(1)CO的平衡转化率与温度,压强的关系如图所示:
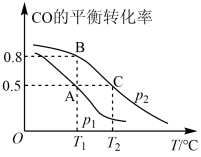
①p1、p2的大小关系是p1________ p2 (填“>、<或=”)。
②下列叙述能说明上述反应能达到化学平衡状态的是________ (填代号)。
a.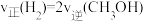
b. 的体积分数不再改变
的体积分数不再改变
c.混合气体的密度不再改变
d.同一时间内,消耗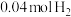 ,生成
,生成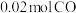
(2)在 ℃、p2压强时,往一容积为
℃、p2压强时,往一容积为 的密闭容器内,充入
的密闭容器内,充入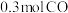 与
与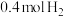 发生反应。
发生反应。
①此时的浓度平衡常数K=________ ;平衡后再加入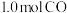 后重新到达平衡,则
后重新到达平衡,则 的转化率
的转化率________ (填“增大,不变或减小”); 与
与 的浓度比
的浓度比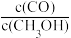
________ (填“增大,不变或减小”)。
②若 压强恒定为
压强恒定为 ,则平衡常数
,则平衡常数
________ ( 用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含
用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含 的最简表达式)。
的最简表达式)。
 与
与 的混合气体)转化成甲醇,反应为
的混合气体)转化成甲醇,反应为 。
。(1)CO的平衡转化率与温度,压强的关系如图所示:

①p1、p2的大小关系是p1
②下列叙述能说明上述反应能达到化学平衡状态的是
a.
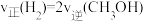
b.
 的体积分数不再改变
的体积分数不再改变c.混合气体的密度不再改变
d.同一时间内,消耗
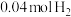 ,生成
,生成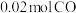
(2)在
 ℃、p2压强时,往一容积为
℃、p2压强时,往一容积为 的密闭容器内,充入
的密闭容器内,充入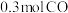 与
与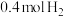 发生反应。
发生反应。①此时的浓度平衡常数K=
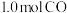 后重新到达平衡,则
后重新到达平衡,则 的转化率
的转化率 与
与 的浓度比
的浓度比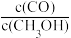
②若
 压强恒定为
压强恒定为 ,则平衡常数
,则平衡常数
 用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含
用气体平衡分压代替气体平衡浓度计算,分压=总压×气体的物质的量分数,整理出含 的最简表达式)。
的最简表达式)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在2L密闭容器内,800℃时在反应2NO(g)+O2(g) 2NO2(g)体系中,
2NO2(g)体系中,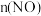 随时间的变化如下:
随时间的变化如下:
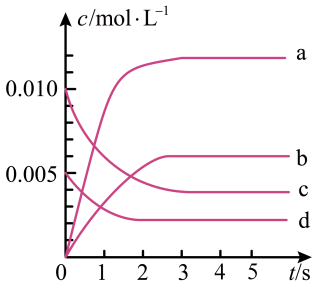
(1)下图表示NO的变化的曲线是___________ 。
(2)达平衡时NO的转化率为___________ 。
(3)用NO2表示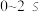 内该反应的平均速率ν(NO2)=
内该反应的平均速率ν(NO2)=___________ 。
(4)能说明该反应已达到平衡状态的有___________ (填序号)。
a. 2n (NO2) = n (NO) b. ν(NO2) = 2ν(O2)
c.容器内压强保持不变 d. 容器内密度保持不变
e.容器内颜色保持不变 f. 容器内混合气体的平均相对分子质量不变
(5)为使该反应的反应速率增大,下列措施正确的有___________ 。
a. 适当升高温度 b. 增大 的浓度
的浓度
c. 及时分离出NO2 d. 选择高效催化剂
 2NO2(g)体系中,
2NO2(g)体系中,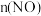 随时间的变化如下:
随时间的变化如下:时间/ | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)下图表示NO的变化的曲线是

(2)达平衡时NO的转化率为
(3)用NO2表示
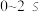 内该反应的平均速率ν(NO2)=
内该反应的平均速率ν(NO2)=(4)能说明该反应已达到平衡状态的有
a. 2n (NO2) = n (NO) b. ν(NO2) = 2ν(O2)
c.容器内压强保持不变 d. 容器内密度保持不变
e.容器内颜色保持不变 f. 容器内混合气体的平均相对分子质量不变
(5)为使该反应的反应速率增大,下列措施正确的有
a. 适当升高温度 b. 增大
 的浓度
的浓度c. 及时分离出NO2 d. 选择高效催化剂
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】用二氧化氯(ClO2)可制备用途广泛的亚氯酸钠(NaClO2),实验室可用下列装置(略去部分夹持仪器)制备少量的亚氯酸钠
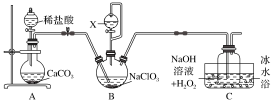
已知:①ClO2沸点为9.9 ℃,可溶于水,有毒,浓度较高时易发生爆炸
②NaClO2饱和溶液低于38 ℃时析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解为NaClO3和NaCl
③B装置为ClO2发生装置,所用试剂NaClO3、H2SO4(浓)、CH3OH
请回答下列问题:
实验过程中需持续通入一定量的CO2,其目的是_______ ;反应结束后需再通入一定量的CO2,其目的是_______

已知:①ClO2沸点为9.9 ℃,可溶于水,有毒,浓度较高时易发生爆炸
②NaClO2饱和溶液低于38 ℃时析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解为NaClO3和NaCl
③B装置为ClO2发生装置,所用试剂NaClO3、H2SO4(浓)、CH3OH
请回答下列问题:
实验过程中需持续通入一定量的CO2,其目的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】检查装置气密性是化学实验中的重要操作之一。试按要求回答下列问题:
(1)下列仪器或装置在使用前一定要检查气密性的是___(填序号,下同)。
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是___。
(3)检查下图所示简易气体发生装置的气密性操作是:___________
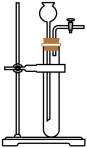
(4)该装置能做到关闭活塞,随后反应停止。它的原理是:_________
(1)下列仪器或装置在使用前一定要检查气密性的是___(填序号,下同)。
| A.容量瓶 | B.洗气瓶 | C.分液漏斗 | D.酸(碱)式滴定管 |
(2)下列关于不进行气密性检查可能导致后果的叙述中,正确的是___。
| A.收集不到气体 |
| B.造成环境污染 |
| C.观察到的实验现象有误 |
| D.引发爆炸事故 |

(4)该装置能做到关闭活塞,随后反应停止。它的原理是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:
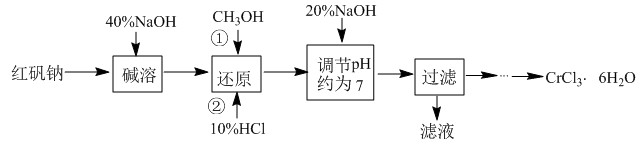
已知:① Cr2O +H2O
+H2O 2CrO
2CrO +2H+;
+2H+;
② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体___________ ,蒸发浓缩,___________ ,过滤, ___________ ,低温干燥,得到CrCl3·6H2O(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)。

已知:① Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+;
+2H+;② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯化铬晶体(CrCl3·6H2O)是一种重要的工业原料,工业上常用铬酸钠(Na2CrO4)来制备。实验室以红矾钠(Na2Cr2O7)为原料制备CrCl3·6H2O的流程如下:

已知:① Cr2O +H2O
+H2O 2CrO
2CrO +2H+;
+2H+;
② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体___________ ,蒸发浓缩,___________ ,过滤, ___________ ,低温干燥,得到CrCl3·6H2O(实验中可供选择的试剂:盐酸、硫酸、蒸馏水、乙醇、乙醚)。

已知:① Cr2O
 +H2O
+H2O 2CrO
2CrO +2H+;
+2H+;② CrCl3·6H2O不溶于乙醚,易溶于水、乙醇,易水解。
请补充完整由过滤后得到的固体Cr(OH)3制备CrCl3·6H2O的实验方案:将过滤后所得的洁净固体
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】要分离下列四组混合物:
①食盐与沙子 ②从KNO3和NaCl的混合溶液中获得KNO3 ③水和汽油的混合物 ④CCl4液体与甲苯液体的混合物 (已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
(1)分离①、②的操作分别为________ 、________ 。
(2)分离③时所使用的仪器中有一种在其他组分分离时无需使用,这种仪器是________ 。
①食盐与沙子 ②从KNO3和NaCl的混合溶液中获得KNO3 ③水和汽油的混合物 ④CCl4液体与甲苯液体的混合物 (已知CCl4与甲苯互溶,沸点分别为76.75℃和110.6℃)
(1)分离①、②的操作分别为
(2)分离③时所使用的仪器中有一种在其他组分分离时无需使用,这种仪器是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】海洋是一个巨大的宝藏,海水淡化是重要的化学研究课题。
(1)蒸馏法获取淡水,历史悠久,操作简单,图中符合模拟蒸馏海水的装置是___ (填序号)。
a.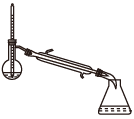 b.
b.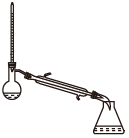
c.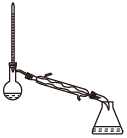 d.
d.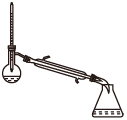
蒸馏前,应向烧瓶中加入沸石或碎瓷片,目的是___ ,冷凝水一般不采用“上进下出”,其原因是____ 。
(2)电渗析法的技术原理如图(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过):
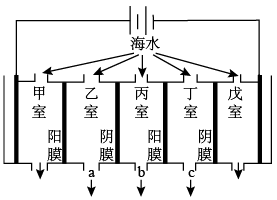
某地海水中主要含Na+、K+、Ca2+、Mg2+、Cl-、HCO 、SO
、SO 等,则淡化过程中,甲室的电极反应式为
等,则淡化过程中,甲室的电极反应式为___ ,产生水垢最多的是___ 室,淡水的出口为____ (填“a”、“b”或“c”)。
(3)离子交换法获取淡水模拟图如图:

经过阳离子交换树脂后水中阳离子数目____ (填“增加”“不变”或“减少”),阴离子交换树脂中发生了离子反应,其离子方程式为___ 。
(1)蒸馏法获取淡水,历史悠久,操作简单,图中符合模拟蒸馏海水的装置是
a.
 b.
b.
c.
 d.
d.
蒸馏前,应向烧瓶中加入沸石或碎瓷片,目的是
(2)电渗析法的技术原理如图(两端为惰性电极,阳膜只允许阳离子通过,阴膜只允许阴离子通过):

某地海水中主要含Na+、K+、Ca2+、Mg2+、Cl-、HCO
 、SO
、SO 等,则淡化过程中,甲室的电极反应式为
等,则淡化过程中,甲室的电极反应式为(3)离子交换法获取淡水模拟图如图:

经过阳离子交换树脂后水中阳离子数目
您最近一年使用:0次



