新型储氢材料是开发利用氢能的重要研究方向.
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为_____ ,该能层具有的原子轨道数为_____ .
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是_____ ,B原子的杂化轨道类型是_____ .
Li、B、H元素的电负性由大到小排列顺序为_____ .
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+_____ H﹣(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
M是_____ (填元素符号).
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为_____ ,NaH的理论密度是___________ g•cm﹣3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
①基态Cl原子中,电子占据的最高能层符号为
②LiBH4由Li+和BH4﹣构成,BH4﹣的立体结构是
Li、B、H元素的电负性由大到小排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+
| I1/kJ•mol﹣1 | I2/kJ•mol﹣1 | I3/kJ•mol﹣1 | I4/kJ•mol﹣1 | I5/kJ•mol﹣1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H﹣的半径为
更新时间:2016-12-09 16:35:24
|
相似题推荐
填空题
|
适中
(0.65)
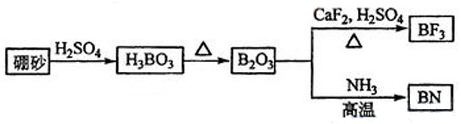
【推荐1】氮化硼(BN)是一种重要的功能陶瓷材料以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如下图所示:
请回答下列问题:
(1)写出B2O3与NH3反应生成BN的方程式___________________________
(2)基态N原子的价层电子排布式为_________ 。
(3)B、N、O相比,第一电离能最大的是_______ ,BN中B元素的化合价为_____
(4)SO42–中S原子的杂化轨道类型为_______ ,O—S—O的键角是_______ ,写出一个与SO42–等电子体的微粒_______ 。
(5)BF3能与NH3反应生成BF3•NH3,BF3分子的分子构型为_______ ,BF3•NH3中BF3与NH3之间通过___________ (填“离子键”、“ 配位键”或“氢键”) 结合。
请回答下列问题:
(1)写出B2O3与NH3反应生成BN的方程式
(2)基态N原子的价层电子排布式为
(3)B、N、O相比,第一电离能最大的是
(4)SO42–中S原子的杂化轨道类型为
(5)BF3能与NH3反应生成BF3•NH3,BF3分子的分子构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
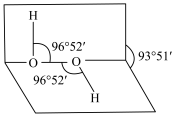
【推荐2】过氧化氢(H2O2)又叫双氧水,其水溶液可用于制备工业上的漂白剂,特殊环境里燃料燃烧的助燃剂,医疗上的消毒剂,实验室里的制氧剂等。过氧化氢分子中的1个过氧原子团“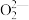 ”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。
”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。

(1)写出过氧化氢分子的电子式:___________ 。
(2)下列关于过氧化氢的说法中正确的是___________ (填序号)。
①分子中有极性键
②分子中有非极性键
③氧原子的轨道发生了sp2杂化
④O—O共价键是p-p σ键
⑤分子是非极性分子
(3)过氧化氢难溶于二硫化碳,主要原因是___________ ;过氧化氢易溶于水,主要原因是___________ 。
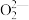 ”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。
”由2个氧原子共用1对电子形成,过氧化氢的空间结构如图所示。

(1)写出过氧化氢分子的电子式:
(2)下列关于过氧化氢的说法中正确的是
①分子中有极性键
②分子中有非极性键
③氧原子的轨道发生了sp2杂化
④O—O共价键是p-p σ键
⑤分子是非极性分子
(3)过氧化氢难溶于二硫化碳,主要原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硼氢化钠(NaBH4)是一种储氢密度较高、价格低廉、兼具安全性与稳定性的固态储氢材料。
(1)基态B原子中电子占据最高能级的符号是_______ ,占据该能级电子的电子云轮廓图为_______ 形。基态B原子中,核外存在_______ 对自旋相反的电子。
(2)在周期表中,与B元素的化学性质最相似的邻族元素是_______ 。
(3)将物质的量之比为3∶1的NaBH4固体和ScF3固体混合研磨,得到的复合储氢体系可以显著降低放氢温度。基态21Sc原子的简化电子排布式为_______ 。
(1)基态B原子中电子占据最高能级的符号是
(2)在周期表中,与B元素的化学性质最相似的邻族元素是
(3)将物质的量之比为3∶1的NaBH4固体和ScF3固体混合研磨,得到的复合储氢体系可以显著降低放氢温度。基态21Sc原子的简化电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题
(1) 在水溶液中与
在水溶液中与 发生如下反应:
发生如下反应: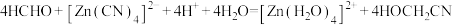 。
。
①在 中含有
中含有 键的数目为
键的数目为___________ 。
② 中
中 与
与 的C原子形成配位键。不考虑空间构型,
的C原子形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为___________ 。
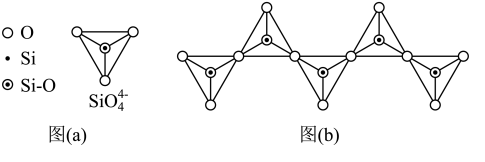
(2)在硅酸盐中, 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为___________ 。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为___________ ,微粒之间存在的作用力是___________ 。
(4)硫酸镍溶于氨水形成 蓝色溶液。在
蓝色溶液。在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为___________ ,提供孤电子对的成键原子是___________ 。
(5)氨的沸点___________ (填“高于”或“低于”)膦 ,原因是
,原因是___________ 。
(6)氮元素是植物生长所需的元素,常见氮肥有铵盐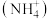 、尿素(
、尿素(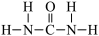 )等,
)等, 中
中 键角
键角___________ (填“>”“<”或“=”) 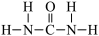 中
中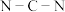 键角。
键角。
(7)硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用。硫单质有多种同素异形体,其中一种单质分子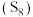 的结构为
的结构为 ,其熔点和沸点要比二氧化硫的高很多,主要原因为
,其熔点和沸点要比二氧化硫的高很多,主要原因为___________ 。
(8)在气体分析中,常用 的盐酸溶液吸收并定量测定
的盐酸溶液吸收并定量测定 的含量,其化学反应:
的含量,其化学反应: ;
; 是一种配合物,其结构如图所示:
是一种配合物,其结构如图所示:
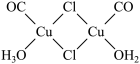
该配合物中, 作配体时配位原子是C而不是O的原因是
作配体时配位原子是C而不是O的原因是___________ 。
(1)
 在水溶液中与
在水溶液中与 发生如下反应:
发生如下反应: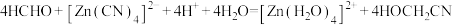 。
。①在
 中含有
中含有 键的数目为
键的数目为②
 中
中 与
与 的C原子形成配位键。不考虑空间构型,
的C原子形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为(2)在硅酸盐中,
 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(4)硫酸镍溶于氨水形成
 蓝色溶液。在
蓝色溶液。在 中
中 与
与 之间形成的化学键称为
之间形成的化学键称为(5)氨的沸点
 ,原因是
,原因是(6)氮元素是植物生长所需的元素,常见氮肥有铵盐
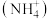 、尿素(
、尿素(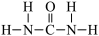 )等,
)等, 中
中 键角
键角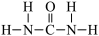 中
中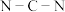 键角。
键角。(7)硫元素和人类的生存与发展联系密切,在战国时期,我国的炼丹家们就开始了对硫单质及含硫化合物的研究应用。硫单质有多种同素异形体,其中一种单质分子
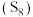 的结构为
的结构为 ,其熔点和沸点要比二氧化硫的高很多,主要原因为
,其熔点和沸点要比二氧化硫的高很多,主要原因为(8)在气体分析中,常用
 的盐酸溶液吸收并定量测定
的盐酸溶液吸收并定量测定 的含量,其化学反应:
的含量,其化学反应: ;
; 是一种配合物,其结构如图所示:
是一种配合物,其结构如图所示:
该配合物中,
 作配体时配位原子是C而不是O的原因是
作配体时配位原子是C而不是O的原因是
您最近一年使用:0次
【推荐2】根据已学知识,请回答下列问题:
(1)基态N原子中,核外电子占据的最高能层的符号是_______ ,占据该能层电子的原子轨道形状为_______ 。
(2)写出3p轨道上有2个未成对电子的元素的符号:_______ 。
(3)已知铁是26号元素,写出Fe的价层电子排布式:_______ ;
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为_______ ,电负性由大到小的顺序是_______ 。
(5)Zn2+的核外电子排布式为_______ 。
(1)基态N原子中,核外电子占据的最高能层的符号是
(2)写出3p轨道上有2个未成对电子的元素的符号:
(3)已知铁是26号元素,写出Fe的价层电子排布式:
(4)从原子结构的角度分析B、N和O的第一电离能由大到小的顺序为
(5)Zn2+的核外电子排布式为
您最近一年使用:0次
【推荐3】开发新型储氢材料是开发利用氢能的重要研究方向。
(1) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。
①基态Cl原子中,电子占据的最高电子层符号为______ ,该电子层具有的原子轨道数为 _______ 。
②Li、B、H元素的电负性由大到小的排列顺序为___________ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+___________ (填“>”“=”或“<”)H-。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
则M是______________ (填元素名称)。
(1)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。
反应制得。①基态Cl原子中,电子占据的最高电子层符号为
②Li、B、H元素的电负性由大到小的排列顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如表所示:
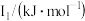 | 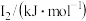 | 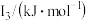 | 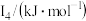 | 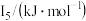 |
| 738 | 1451 | 7733 | 10540 | 13630 |
则M是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下图是某金属氧化物的晶体结构示意图。图中,小球代表金属原子,大球代表氧原子,细线框出其晶胞。
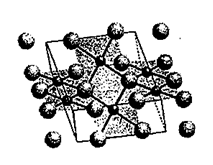
(1)金属原子的配位数是_______ ,氧原子的配位数是_______ ;
(2)晶胞中金属原子数是_______ ,氧原子数是_______ ;
(3)该金属氧化物的化学式(金属用M表示)为_______ 。

(1)金属原子的配位数是
(2)晶胞中金属原子数是
(3)该金属氧化物的化学式(金属用M表示)为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高温超导材料是科学家研究的重点物质之一。
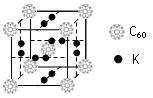
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的K原子和C60分子的个数比为________ 。
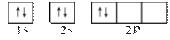
⑵某同学画出的C的核外电子排布(轨道表示式)如上右图所示,该电子排布图(轨道表示式)违背了________ ,请你画出正确的电子排布图(轨道表示式)_______ 。
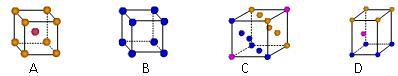
⑶金属钾采用的是下列_________ (填字母代号)堆积方式。
⑷富勒烯(C60)的结构如图。
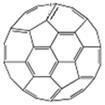
①1 mol C60分子中σ键的数目为__________ 。
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:_________ 。
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的K原子和C60分子的个数比为

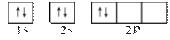
⑵某同学画出的C的核外电子排布(轨道表示式)如上右图所示,该电子排布图(轨道表示式)违背了
⑶金属钾采用的是下列

⑷富勒烯(C60)的结构如图。

①1 mol C60分子中σ键的数目为
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】物质的微观结构对于生命科学的发展有着重要的作用。
(1)磷化铝(AlP)通常作为一种广谱熏蒸杀虫剂,其晶胞如图甲所示
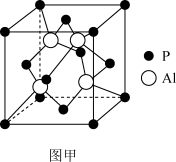
①P的配位数为_______ ;
②其中与P的含氧酸根PO 互为等电子体的非极性分子是
互为等电子体的非极性分子是_______ 。
(2)图乙所示是一种超分子,其中Mo处于第五周期第ⅥB族,核外电子排布与Cr相似,它的基态价电子排布式是_______ 。

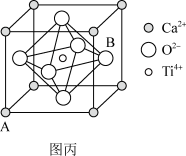
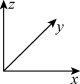
(3)①如图丙所示,钙钛矿晶胞的Ti4+处于6个O2-组成的_______ 空隙中(填几何空间构型)。其中A的坐标参数为(0,0,0),则B的坐标参数为_______ 。
②与Ti相关化合物性质如下表:
TiC的熔沸点明显高于TiCl4的原因为_______ 。
(1)磷化铝(AlP)通常作为一种广谱熏蒸杀虫剂,其晶胞如图甲所示

①P的配位数为
②其中与P的含氧酸根PO
 互为等电子体的非极性分子是
互为等电子体的非极性分子是(2)图乙所示是一种超分子,其中Mo处于第五周期第ⅥB族,核外电子排布与Cr相似,它的基态价电子排布式是

(3)①如图丙所示,钙钛矿晶胞的Ti4+处于6个O2-组成的


②与Ti相关化合物性质如下表:
| 物质 | 性质 |
| TiC | 质硬,熔点:3140℃,沸点:4820℃ |
| TiCl4 | 熔点:-25℃,沸点:136.4℃,具有挥发性 |
您最近一年使用:0次



