①~5五种元素在元素周期表中的位置关系如图:
回答下列问题:
(1)①的元素名称是_______ 。
(2)④的基态原子的电子排布式是_______ 。
(3)②和③中,电负性较大的是_______ (填元素符号)。
(4)②和⑤中,第一电离能较大的是_______ (填元素符号)。
(5)②、③、⑤分别与①形成的最简单化合物中,热稳定性最强的是_______ (填化学式)。
| 族周期 | IA | II A | III A | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ||||||
| 3 | ④ | ⑤ |
(1)①的元素名称是
(2)④的基态原子的电子排布式是
(3)②和③中,电负性较大的是
(4)②和⑤中,第一电离能较大的是
(5)②、③、⑤分别与①形成的最简单化合物中,热稳定性最强的是
更新时间:2023-01-10 10:58:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】联合国将2019年定为“国际化学元素周期表年”,2018年中国化学会制作了新版周期表,包含118种元素。回答下列问题:
(1)写出硅元素在周期表中的位置是______ 。
(2)化合物W是由AB两种元素构成的,用电子式表示其形成过程______________ 。
(3)用M单质作阳极,J单质作阴极,Ca(HCO3)2溶液作电解液,进行电解,阴极生成的气体和沉淀分别是______ ,阳极也生成气体和沉淀,写出阳极的电极反应式 ______ 。
(4)从原子结构角度解释碳化硅中碳元素显负价的原因______ 。
(5)第118号元素为Og(中文名“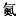 ”,ào),下列说法
”,ào),下列说法正确 的是______ 。
a.Og是第七周期0族元素 b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强 d.中子数为179的Og核素符号是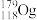
(6)已知X与Y是位于相邻周期的同主族元素。某温度下,X、Y的单质与H2化合生成气态氢化物的平衡常数分别为KX =9.7×1012、KY =5.6×107。Y是______ (填元素符号),判断理由是______ 。
| J | B | ||||||||||||||||
| M | x | ||||||||||||||||
| A | |||||||||||||||||
(2)化合物W是由AB两种元素构成的,用电子式表示其形成过程
(3)用M单质作阳极,J单质作阴极,Ca(HCO3)2溶液作电解液,进行电解,阴极生成的气体和沉淀分别是
(4)从原子结构角度解释碳化硅中碳元素显负价的原因
(5)第118号元素为Og(中文名“
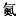 ”,ào),下列说法
”,ào),下列说法a.Og是第七周期0族元素 b.Og原子的核外有118个电子
c.Og在同周期元素中非金属性最强 d.中子数为179的Og核素符号是
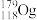
(6)已知X与Y是位于相邻周期的同主族元素。某温度下,X、Y的单质与H2化合生成气态氢化物的平衡常数分别为KX =9.7×1012、KY =5.6×107。Y是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ 。
(2)氨气分子的结构式为_______ ,N2的电子式为_______ 。
(3)CN-中N元素显-3价,说明非金属性N_______ C(填“>”或“<”),请写出一个能比较N和C非金属性强弱的化学事实:_______ 。
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是_______ (用电离方程式解释),常见氮肥种类有_______ (列举两个)。
(1)氮元素在周期表中的位置是
(2)氨气分子的结构式为
(3)CN-中N元素显-3价,说明非金属性N
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为_______ ;反应③中被破坏的化学键属于_______ 键(填“极性”或“非极性”)。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是_______ (用元素符号表示)。与氯元素同周期且金属性最强的元素位于周期表的第_______ 周期_______ 族。
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是_______
a卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:
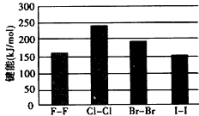
①非金属性强的卤素,其单质分子的化学键_______ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:_______
(1)在光照条件下,氯气和氢气反应过程如下:
①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl……
反应②中形成的化合物的电子式为
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是
(3)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是
a卤化银的颜色按AgCl、AgBr、AgI的顺序依次加深
b卤化氢的键长按H-F、H-Cl、H-Br、H-I的顺序依次减小
c卤化氢的还原性按HF、HCl、HBr、HI的顺序依次减弱
d卤素单质与氢气化合按F2、Cl2、Br2、I2的顺序由难变易
(4)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键
②卤素单质键能大小与键长的关系为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素周期表中第四周期的某些过渡元素(如Ti、Co等)在生产、生活中有着广泛的应用。Co2+能与水杨醛缩对氯苯胺形成具有发光性的配合物,水杨醛缩对氯苯胺制备反应方程式如下:
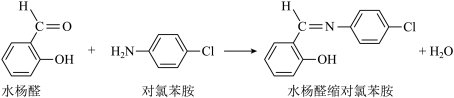
(1)基态Co2+核外电子排布式_______ ;C原子的轨道表示式为_______ ;C、N、O元素的电负性由大到小的顺序为_______ 。
(2)水杨醛所含的官能团为_______ 。
(3)1mol水杨醛最多与_______ H2发生加成反应。
(4)一定条件下,水杨醛缩对氯苯胺与足量NaOH溶液反应的化学方程式_______ 。

(1)基态Co2+核外电子排布式
(2)水杨醛所含的官能团为
(3)1mol水杨醛最多与
(4)一定条件下,水杨醛缩对氯苯胺与足量NaOH溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是_________________ 。
(2)①硫单质的一种结构为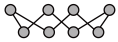 ,杂化方式为
,杂化方式为______________ ,该物质___________ (填“可溶”或“难溶”)于水,该晶体中存在的作用力___________ 、_____________ 。
②SO42-、CS2、CO32-键角由大到小的顺序是_________________ 。
(3)含硫的物质的特殊性质与其结构相关。
①熔点:SF6_______ A1F3(填“>”或“<”),原因是___________________ 。
②分析并比较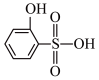 与
与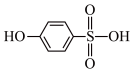 的沸点高低:
的沸点高低:___________________ 。
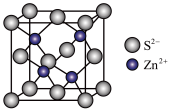
(4)ZnS晶胞如图所示:
①由图可知,Zn2+填在了S2-形成的______________ 空隙中。
②已知晶胞密度为, g/cm3,阿伏伽德罗常数为NA,则晶胞边长为
g/cm3,阿伏伽德罗常数为NA,则晶胞边长为__________ pm。
(1)基态硫原子的价层电子排布图是
(2)①硫单质的一种结构为
 ,杂化方式为
,杂化方式为②SO42-、CS2、CO32-键角由大到小的顺序是
(3)含硫的物质的特殊性质与其结构相关。
①熔点:SF6
②分析并比较
 与
与 的沸点高低:
的沸点高低:(4)ZnS晶胞如图所示:
①由图可知,Zn2+填在了S2-形成的
②已知晶胞密度为,
 g/cm3,阿伏伽德罗常数为NA,则晶胞边长为
g/cm3,阿伏伽德罗常数为NA,则晶胞边长为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】表为周期表的一部分,其中的编号代表对应的元素。
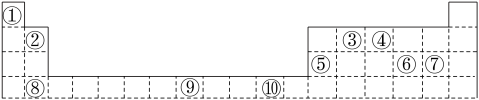
请回答下列问题:
(1)表中属于d区的元素是________ (填编号)。
(2)写出元素⑧的基态原子的电子排布式__________________________ 。
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为________ 对。
(4)元素④的氢化物的分子构型为________ ,中心原子的杂化形式为________ 。
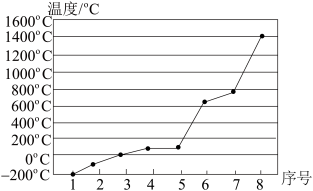
(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表________ (填元素符号);其中电负性最大的是________ (填图中的序号)。

请回答下列问题:
(1)表中属于d区的元素是
(2)写出元素⑧的基态原子的电子排布式
(3)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子为
(4)元素④的氢化物的分子构型为

(5)第三周期8种元素按单质熔点高低的顺序如图,其中序号“8”代表
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有_______ 种运动状态不同的电子,能量最高的电子,其电子云在空间有_______ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式_______ 。
(3)F在元素周期表中属于_______ 区元素,其基态原子核外共有_______ 个未成对电子。
(4)D、E两元素的第一电离能大小关系是_______ (用元素符号表示,下同),B、D两元素的电负性大小关系是_______ 。
(5)写出DA3的电子式:_______ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)D、E两元素的第一电离能大小关系是
(5)写出DA3的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】元素的第一电离能变化规律
(1)同主族元素的原子_______________ 相同,随着核电荷数的增大,原子半径逐渐_____ ,失电子能力逐渐_____ ,第一电离能逐渐_____ 。
(2)同一周期的主族元素具有相同的__________ ,随着核电荷数的递增,最外层电子数_____ ,原子半径逐渐_____ ,失电子能力逐渐_____ ,第一电离能呈现_____ 的趋势。
对同周期元素来说,__________ 的第一电离能最小,__________ 的第一电离能最大。
(1)同主族元素的原子
(2)同一周期的主族元素具有相同的
对同周期元素来说,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是_______ ,其原子核外有_______ 个未成对电子,能量最高的电子所在的轨道呈_______ 形。B为周期表中第29号元素,B的电子排布式为_______ 。
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为: ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为_______ ;此反应中涉及物质中互为等电子体的是_______ ; 的结构式为
的结构式为_______ 。
(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:_______ 。
(1)A是在地壳中含量最多的元素,该元素原子的电子排布图是
(2)汽车尾气含有CO和NO等有毒气体,净化有毒气体的反应方程式为:
 ,此反应中涉及元素的第一电离能大小关系为
,此反应中涉及元素的第一电离能大小关系为 的结构式为
的结构式为(3)元素周期表中除放射性元素外,电负性最小的元素与电负性最大的元素形成的化合物的电子式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有机物种类繁多,应用广泛。
(1)邻氨基吡啶(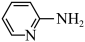 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为______ (填元素符号)。1mol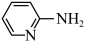 中含有σ键的数目为
中含有σ键的数目为______ mol。
(2)一种鸟嘌呤和吡咯的结构如图。
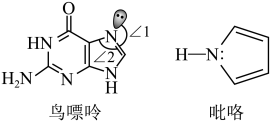
①鸟嘌呤中轨道之间的夹角∠1______ ∠2(填“>”或“<”)。
②分子中的大π键可以用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为______ 。
(3)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
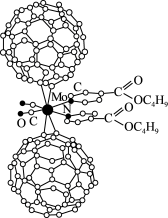
①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布式是______ ,该超分子中存在的化学键类型有______ (填选项字母)。
A.离子键 B.氢键 C.σ键 D.π键
②该超分子中,配体CO提供孤电子对的原子是______ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有_______ 。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为 中含有σ键的数目为
中含有σ键的数目为(2)一种鸟嘌呤和吡咯的结构如图。

①鸟嘌呤中轨道之间的夹角∠1
②分子中的大π键可以用符号π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为(3)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布式是
A.离子键 B.氢键 C.σ键 D.π键
②该超分子中,配体CO提供孤电子对的原子是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】3-乙基吡啶(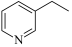 )是一种重要的有机合成中间体,具有芳香性。回答下列问题:
)是一种重要的有机合成中间体,具有芳香性。回答下列问题:
(1)3-乙基吡啶中所含元素电负性由大到小的顺序为____ ;其中碳原子的杂化方式为____ 。
(2)3-乙基吡的沸点高于2,6-二甲基吡啶(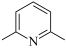 ),分析可能的原因为
),分析可能的原因为____ 。
(3)吡啶(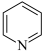 )的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与
)的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与____ molH2发生加成反应;3-乙基吡啶与浓硫酸、浓硝酸混合,在一定条件下发生硝化反应的方程式为___ 。
(4)3-乙基吡啶有多种同分异构体,其中含苯环的同分异构体有____ 种(不考虑立体异构),其中核磁共振氢谱有4组峰的结构简式为____ 。
 )是一种重要的有机合成中间体,具有芳香性。回答下列问题:
)是一种重要的有机合成中间体,具有芳香性。回答下列问题:(1)3-乙基吡啶中所含元素电负性由大到小的顺序为
(2)3-乙基吡的沸点高于2,6-二甲基吡啶(
 ),分析可能的原因为
),分析可能的原因为(3)吡啶(
 )的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与
)的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与(4)3-乙基吡啶有多种同分异构体,其中含苯环的同分异构体有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据元素周期表中完整周期元素的性质,填写下列空白。
(1)在第三周期中,第一电离能最小的元素符号是_______ ,其原子的结构示意图为_______ ,第一电离能最大的元素符号是_______ ,其电子排布式为_______ 。
(2)在元素周期表中,电负性最大的元素名称是_______ ,其价电子排布图为_______ 。
(3)第四周期元素中未成对电子数最多的元素符号是_______ ,其基态原子的简化电子排布式为_______ ,有_______ 个未成对电子,有_______ 个能级,能量最高的能级符号为_______ 。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_______ ,原子中所有电子占有_______ 个轨道,核外共有_______ 个不同运动状态的电子。
(5)某元素的正三价离子的3d能级为半充满,其硫酸盐水溶液显_______ 性(填“酸”、“碱”或“中”),用离子方程式解释其原因_______ 。
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为_______ 。电解一段时间后,阴极区pH_______ (填“增大”、“减小”或“不变”)
(1)在第三周期中,第一电离能最小的元素符号是
(2)在元素周期表中,电负性最大的元素名称是
(3)第四周期元素中未成对电子数最多的元素符号是
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是
(5)某元素的正三价离子的3d能级为半充满,其硫酸盐水溶液显
(6)用惰性电极电解第三周期原子半径最大的元素的氯化物的水溶液,其阳极反应的电极方程式为
您最近一年使用:0次



