硫是一种重要的非金属元素,广泛存在于自然界,回答下列问题:
(1)基态硫原子的价层电子排布图是_________________ 。
(2)①硫单质的一种结构为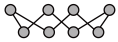 ,杂化方式为
,杂化方式为______________ ,该物质___________ (填“可溶”或“难溶”)于水,该晶体中存在的作用力___________ 、_____________ 。
②SO42-、CS2、CO32-键角由大到小的顺序是_________________ 。
(3)含硫的物质的特殊性质与其结构相关。
①熔点:SF6_______ A1F3(填“>”或“<”),原因是___________________ 。
②分析并比较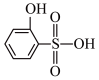 与
与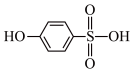 的沸点高低:
的沸点高低:___________________ 。
(4)ZnS晶胞如图所示:
①由图可知,Zn2+填在了S2-形成的______________ 空隙中。
②已知晶胞密度为, g/cm3,阿伏伽德罗常数为NA,则晶胞边长为
g/cm3,阿伏伽德罗常数为NA,则晶胞边长为__________ pm。
(1)基态硫原子的价层电子排布图是
(2)①硫单质的一种结构为
 ,杂化方式为
,杂化方式为②SO42-、CS2、CO32-键角由大到小的顺序是
(3)含硫的物质的特殊性质与其结构相关。
①熔点:SF6
②分析并比较
 与
与 的沸点高低:
的沸点高低:(4)ZnS晶胞如图所示:
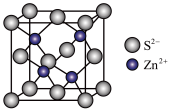
①由图可知,Zn2+填在了S2-形成的
②已知晶胞密度为,
 g/cm3,阿伏伽德罗常数为NA,则晶胞边长为
g/cm3,阿伏伽德罗常数为NA,则晶胞边长为
更新时间:2017-03-04 15:49:54
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】请回答下列问题:
(1)写出N2H 的电子式
的电子式___________ 。
(2)CH4、H2O、H2S沸点由低到高的顺序是___________ 。
(3)判断2H2(g)+O2(g)=2H2O(l)反应的自发性并说明理由___________ 。
(1)写出N2H
 的电子式
的电子式(2)CH4、H2O、H2S沸点由低到高的顺序是
(3)判断2H2(g)+O2(g)=2H2O(l)反应的自发性并说明理由
您最近一年使用:0次
【推荐2】全球一半左右的碘是以智利硝石提取硝酸钠后的母液为原料,加入亚硫酸氢钠制取,相关反应如下:
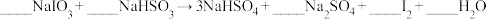 (未配平)
(未配平)
完成下列填空:
(1)配平上述化学方程式,单线桥标出电子转移的方向和数目_______ 。
(2)该反应实质是两步反应:①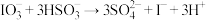 ,则第二步反应的离子方程式为②
,则第二步反应的离子方程式为②_______ ;若要使碘酸钠的利用率最高,碘酸钠在第一步和第二步反应中的用量之比是_______ 。
(3)过滤反应析出的碘沉淀得到粗碘,再用升华法即可得到99%左右的碘产品.碘升华克服的微粒间作用力为_______ 。
(4)检验亚硫酸钠固体是否氧化变质的方法是_______ 。
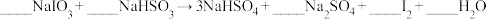 (未配平)
(未配平)完成下列填空:
(1)配平上述化学方程式,单线桥标出电子转移的方向和数目
(2)该反应实质是两步反应:①
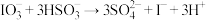 ,则第二步反应的离子方程式为②
,则第二步反应的离子方程式为②(3)过滤反应析出的碘沉淀得到粗碘,再用升华法即可得到99%左右的碘产品.碘升华克服的微粒间作用力为
(4)检验亚硫酸钠固体是否氧化变质的方法是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硫及其化合物有许多用途,相关物质的物理常数如下表所示:
回答下列问题:
(1)根据价层电子对互斥理论, 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是___________ 。
(2)图(a)为 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为___________ 。
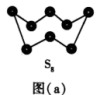
(3)气态三氧化硫以单分子形式存在,其分子的空间结构为___________ 形,其中共价键的类型有___________ 种;固体三氧化硫中存在如图(b)所示的三聚分子,该分子中S原子的杂化轨道类型为___________ 。
 |  |  |  |  |  | |
| 熔点/℃ | -85.5 | 115.2 | >600(分解) | -75.5 | 16.8 | 10.3 |
| 沸点/℃ | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
(1)根据价层电子对互斥理论,
 、
、 、
、 的气态分子中,中心原子价层电子对数不同于其他分子的是
的气态分子中,中心原子价层电子对数不同于其他分子的是(2)图(a)为
 的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
的结构,其熔点和沸点要比二氧化硫的熔点和沸点高很多,主要原因为
(3)气态三氧化硫以单分子形式存在,其分子的空间结构为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碳形成的化合物种类繁多,硅是构成地壳岩石的主要元素。碳在自然界有两种稳定的同位素,有关数据如下表:
请列出碳元素近似相对原子质量的计算式_____________________________________ 。
(1)Si原子的14个电子排布在_______ 个能级上;与硅元素同周期、其原子核外有2个未成对电子的元素的最外层电子排布式为_____________ 。
(2)SiO2用途广泛,以下叙述错误的是______________ 。
a.SiO2是二氧化硅的分子式 b.SiO2中1个Si原子结合4个O原子
c.SiO2是酸性氧化物 d.SiO2熔沸点较高,属于原子晶体
(3)通常状况下,SiF4呈气态。以下叙述正确的是___________ 。
a.Si原子难以形成Si4+ b.SiF4是有极性键的非极性分子
c.固态SiF4是原子晶体 d.相同压强时,SiF4的沸点高于SiCl4
(4)Fe3O4可以写成FeO•Fe2O3,也可写成盐的形式:Fe[Fe2O4]。Pb3O4中含+2价的Pb和+4价的Pb,请将Pb3O4写成两种氧化物的形式___________ ,写成盐的形式__________ 。
(5)Pb的+2价化合物稳定,+4价的Pb能氧化浓盐酸生成Cl2。写出Pb3O4与盐酸反应的化学方程式____________________________________________ 。
| 同位素 | 相对原子质量 | 丰度(原子分数) |
| 12C | 12(整数,相对原子质量的基准) | 0.9893 |
| 13C | 13.003354826 | 0.0107 |
请列出碳元素近似相对原子质量的计算式
(1)Si原子的14个电子排布在
(2)SiO2用途广泛,以下叙述错误的是
a.SiO2是二氧化硅的分子式 b.SiO2中1个Si原子结合4个O原子
c.SiO2是酸性氧化物 d.SiO2熔沸点较高,属于原子晶体
(3)通常状况下,SiF4呈气态。以下叙述正确的是
a.Si原子难以形成Si4+ b.SiF4是有极性键的非极性分子
c.固态SiF4是原子晶体 d.相同压强时,SiF4的沸点高于SiCl4
(4)Fe3O4可以写成FeO•Fe2O3,也可写成盐的形式:Fe[Fe2O4]。Pb3O4中含+2价的Pb和+4价的Pb,请将Pb3O4写成两种氧化物的形式
(5)Pb的+2价化合物稳定,+4价的Pb能氧化浓盐酸生成Cl2。写出Pb3O4与盐酸反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料。 LiFePO4可用FeCl3、NH4H2PO4、LiCl和苯胺(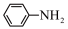 )等作为原料制备。
)等作为原料制备。
(1) Fe2+基态核外电子排布式为________ ,PO43-的空间构型为________ (用文字描述)。
(2) NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是____ (填元素符号)。
(3) 1 mol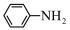 含有的σ键数目为
含有的σ键数目为___ ,苯胺的沸点高于甲苯的主要原因是________ 。
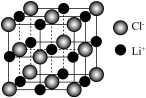
(4) 一个LiCl晶胞(如图)中,Li+数目为________ 。
 )等作为原料制备。
)等作为原料制备。(1) Fe2+基态核外电子排布式为
(2) NH4H2PO4中,除氢元素外,其余三种元素第一电离能最大的是
(3) 1 mol
 含有的σ键数目为
含有的σ键数目为(4) 一个LiCl晶胞(如图)中,Li+数目为

您最近一年使用:0次
【推荐3】A、B、C、D、E代表前4周期的五种元素,原子序数依次增大。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其电子轨道表示式为___________ 。
(2)B元素的负一价离子的电子层结构与氩相同,B离子的结构示意图为___________ 。
(3)C元素的正三价离子的3d能级为半充满,C的元素符号为___________ ,该元素在周期表中的位置为___________ 。
(4)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的元素基态原子的电子排布式为___________ ,在元素周期表中的位置为___________ 。
(5)E元素基态原子中没有未成对电子,E的外围电子排布式是___________ 。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其电子轨道表示式为
(2)B元素的负一价离子的电子层结构与氩相同,B离子的结构示意图为
(3)C元素的正三价离子的3d能级为半充满,C的元素符号为
(4)D元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,D的元素基态原子的电子排布式为
(5)E元素基态原子中没有未成对电子,E的外围电子排布式是
您最近一年使用:0次
填空题
|
适中
(0.65)
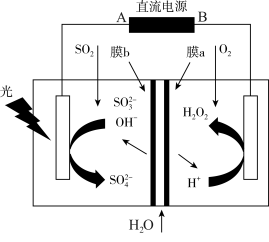
【推荐1】我国科学家设计如图所示的光电催化体系,可以实现烟气脱SO2。
2.SO2的价层电子对空间构型为___________ 结构, 的立体构型为
的立体构型为___________ 。
A. 平面三角形 B. 角形 C. 三角锥形 D. 正四面体形
3.若参与反应的O2为0.2mol,可以实现烟气脱SO2的体积(标准状况)为___________ L。
| A.阳极 | B.阴极 | C.正极 | D.负极 |
 的立体构型为
的立体构型为A. 平面三角形 B. 角形 C. 三角锥形 D. 正四面体形
3.若参与反应的O2为0.2mol,可以实现烟气脱SO2的体积(标准状况)为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】转化 的方法主要有电催化、热还原等。
的方法主要有电催化、热还原等。
(1) 电催化制CO。在电解过程中向电解质中加入离子导体(
电催化制CO。在电解过程中向电解质中加入离子导体( )可以提高CO的选择性(CO是指
)可以提高CO的选择性(CO是指 转化生成CO的百分比,下同)。
转化生成CO的百分比,下同)。
①离子导体M中含有H、B、C、N、F等元素,其中B、C、N、F四种元素的第一电离能由小到大的顺序为_______ 。 的空间构型是
的空间构型是_______ 。
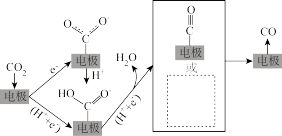
②电催化还原 制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图_______ 。
(2) 热还原制
热还原制 和CO。在常压、
和CO。在常压、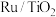 催化下,
催化下, 和
和 混和气体(体积比1:4)进行反应,测得
混和气体(体积比1:4)进行反应,测得 转化率、
转化率、 和CO的选择性随温度变化如图所示。
和CO的选择性随温度变化如图所示。
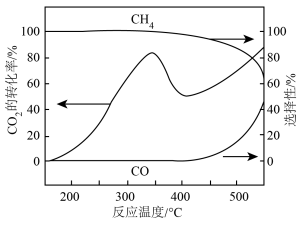
反应I:

反应II:

①400℃后,随温度升高 转化率不断上升的原因是
转化率不断上升的原因是_______ 。
②反应II中 和
和 在
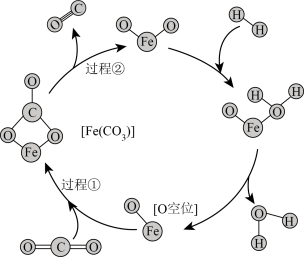
在 (存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是
(存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是_______ 。
 的方法主要有电催化、热还原等。
的方法主要有电催化、热还原等。(1)
 电催化制CO。在电解过程中向电解质中加入离子导体(
电催化制CO。在电解过程中向电解质中加入离子导体( )可以提高CO的选择性(CO是指
)可以提高CO的选择性(CO是指 转化生成CO的百分比,下同)。
转化生成CO的百分比,下同)。①离子导体M中含有H、B、C、N、F等元素,其中B、C、N、F四种元素的第一电离能由小到大的顺序为
 的空间构型是
的空间构型是②电催化还原
 制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
制CO的示意图如下图所示。请在虚线框中画出还有可能得到的中间体的结构示意图
(2)
 热还原制
热还原制 和CO。在常压、
和CO。在常压、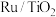 催化下,
催化下, 和
和 混和气体(体积比1:4)进行反应,测得
混和气体(体积比1:4)进行反应,测得 转化率、
转化率、 和CO的选择性随温度变化如图所示。
和CO的选择性随温度变化如图所示。
反应I:


反应II:


①400℃后,随温度升高
 转化率不断上升的原因是
转化率不断上升的原因是②反应II中
 和
和 在
在 (存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是
(存在O空位)催化剂的作用下,可以提高CO的选择性,反应机理如图所示。从电负性的角度,过程①和②能发生的原因是
您最近一年使用:0次
【推荐3】元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。
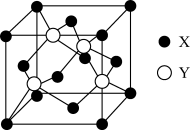
①在1个晶胞中,X离子的数目为________ 。
②该化合物的化学式为________ 。
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是_________ 。
(3)Y与Z可形成YZ42-,YZ42-的空间构型为________ (用文字描述)。
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为________ 。
(5)请比较亚氯酸(HClO2)和氯酸(HClO3)的酸性强弱:HClO2________ HClO3(填“>”“<”或“=”),试从分子结构与性质的关系解释原因_______ 。
(1)X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为
②该化合物的化学式为
(2)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(3)Y与Z可形成YZ42-,YZ42-的空间构型为
(4)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1 mol该配合物中含有σ键的数目为
(5)请比较亚氯酸(HClO2)和氯酸(HClO3)的酸性强弱:HClO2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】干冰、石墨、C60、氟化钙和金刚石的结构模型如下(石墨仅表示其中的一层结构):
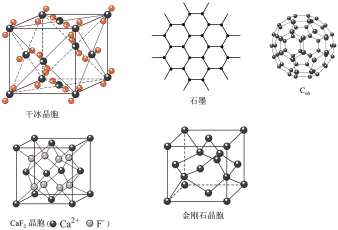
回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有________ 个与之紧邻且等距的CO2分子。
(2)由金刚石晶胞可知,每个金刚石晶胞占有________ 个碳原子。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是________ 。
(4)在CaF2晶体中,Ca2+的配位数是________ ,F-的配位数是________ 。
(5)固态时,C60属于________ (填“共价”或“分子”)晶体。

回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有
(2)由金刚石晶胞可知,每个金刚石晶胞占有
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是
(4)在CaF2晶体中,Ca2+的配位数是
(5)固态时,C60属于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一种由Cu、In、Te组成的高熵合金具有优良的热电性能,其四方晶胞如图所示:
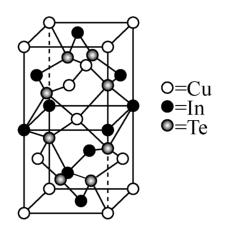
In的配位数为_______ ;晶体中Te原子填充在Cu、In围成的四面体空隙中,则四面体空隙的占有率为_______ 。

In的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是_____ 。与钛同周期的过渡元素中,基态原子的成对电子数与钛相同的有_____ 种。
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为_____ 。
(3)单晶衍射实验证实,配合物[Cr3O(CH3COO)6(H2O)3]Cl•8H2O的阳离子的结构如图甲所示:
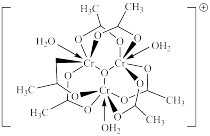
该配合物中中心离子的配位数是_____ ,铬元素的化合价为_____ 。
(4)某科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是_____ (填字母)。
(5)“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),写出该合金的化学式:_____ 。
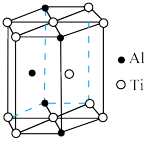
(1)金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为
(3)单晶衍射实验证实,配合物[Cr3O(CH3COO)6(H2O)3]Cl•8H2O的阳离子的结构如图甲所示:

该配合物中中心离子的配位数是
(4)某科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是
A. | B. | C.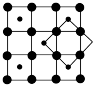 | D. |

您最近一年使用:0次



