过渡金属及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是_____ 。与钛同周期的过渡元素中,基态原子的成对电子数与钛相同的有_____ 种。
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为_____ 。
(3)单晶衍射实验证实,配合物[Cr3O(CH3COO)6(H2O)3]Cl•8H2O的阳离子的结构如图甲所示:
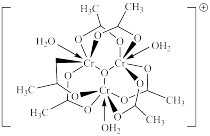
该配合物中中心离子的配位数是_____ ,铬元素的化合价为_____ 。
(4)某科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是_____ (填字母)。
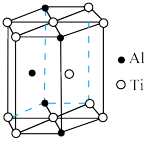
(5)“嫦娥五号”某核心部件主要成分为纳米钛铝合金,其结构单元如图所示(Al、Ti原子各有一个原子在结构单元内部),写出该合金的化学式:_____ 。
(1)金属钛是一种新兴的结构材料,其硬度比金属镁和铝大的原因是
(2)在浓的TiCl3的盐酸中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3•6H2O的晶体,该晶体中两种配体的物质的量之比为2∶4,则由该配合离子组成的晶体化学式还可以写为
(3)单晶衍射实验证实,配合物[Cr3O(CH3COO)6(H2O)3]Cl•8H2O的阳离子的结构如图甲所示:

该配合物中中心离子的配位数是
(4)某科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图所示,小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是
A. | B. | C.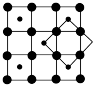 | D. |

更新时间:2022-12-16 22:18:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。(已知阿伏加德罗常数的值为NA)
(1)基态Zn原子核外的最高能层符号是___________ ,基态Zn2+最外层电子排布式为___________ 。
(2)乳酸锌[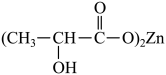 ]是一种很好的食品锌强化剂,其中存在的作用力有
]是一种很好的食品锌强化剂,其中存在的作用力有___________ (填字母)。1 mol乳酸锌中含有___________ 个σ键。
A.离子键 B.极性共价键
C.金属键 D.配位键
E.范德华力
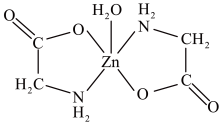
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是___________ ,H2O分子的立体构型为___________ 形,Zn2+的配位数为___________ 。甘氨酸(H2N—CH2—COOH)中N原子的杂化轨道类型为___________ ;甘氨酸易溶于水,试从结构角度解释___________ 。
(1)基态Zn原子核外的最高能层符号是
(2)乳酸锌[
 ]是一种很好的食品锌强化剂,其中存在的作用力有
]是一种很好的食品锌强化剂,其中存在的作用力有A.离子键 B.极性共价键
C.金属键 D.配位键
E.范德华力
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】以下元素均为第4周期元素,请回答相关问题。
(1)钾、锰分别位于___________ 族、___________ 族。
(2)基态铁原子的电子排布式为___________ 。
(3)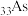 、
、 、
、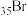 三种非金属元素的电负性由大到小的顺序为
三种非金属元素的电负性由大到小的顺序为___________ ;Br可与第三周期Cl元素形成化合物BrCl,其中显正价的元素为___________ ,原因是___________ 。
(1)钾、锰分别位于
(2)基态铁原子的电子排布式为
(3)
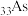 、
、 、
、 三种非金属元素的电负性由大到小的顺序为
三种非金属元素的电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】明代宋应星所著《天工开物》中已经记载了我国古代用炉甘石(主要成分ZnCO3)和煤冶锌工艺,锌的主要用途是制造锌合金和作为其他金属的保护层。回答下列问题:
(1) Zn原子基态核外电子排布式为___________________ 。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①SO42-中心原子的轨道杂化类型为_____ ,与它互为等电子体的阴离子化学式为____ (写出一种)。
②在[Zn(NH3)4]2+中Zn2+与NH3之间形成的化学键为___ ,提供孤电子对的成键原子是____ 。 ③氨的热稳定性强于膦(PH3),原因是_______ 。
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为:ICu=746kJ/mol,Izn=906 kJ/mol,ICu < Izn的原因是_____________ 。
(4)《本草纲目》中记载炉甘石(主要成分ZnCO3)可止血,消肿毒,生肌,明目……。
Zn、C、O电负性由大至小的顺序是________ 。ZnCO3中阴离子的立体构型是______ 。
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶胞结构如图所示,每个Zn原子周围最近的Zn原子数目为____________ 。
晶胞边长为a pm,阿伏伽德罗常数为NA,则ZnS晶体的密度为_____ g/cm3 (列出计算式即可)
(1) Zn原子基态核外电子排布式为
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①SO42-中心原子的轨道杂化类型为
②在[Zn(NH3)4]2+中Zn2+与NH3之间形成的化学键为
(3)黄铜是由铜和锌所组成的合金,元素铜与锌的第一电离能分别为:ICu=746kJ/mol,Izn=906 kJ/mol,ICu < Izn的原因是
(4)《本草纲目》中记载炉甘石(主要成分ZnCO3)可止血,消肿毒,生肌,明目……。
Zn、C、O电负性由大至小的顺序是
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶胞结构如图所示,每个Zn原子周围最近的Zn原子数目为
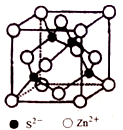
晶胞边长为a pm,阿伏伽德罗常数为NA,则ZnS晶体的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】如图是由Q、R、G三种元素组成的一种高温超导体的晶胞结构,其中R为+2价,G为-2价,则Q的化合价为______ 。


您最近一年使用:0次
【推荐2】已知CaF2的熔点为1402℃,可作电冶金的助熔剂。CaF2的晶胞图以及晶胞的投影图(晶胞所有面的投影均相同)。
(1)下列说法正确的是______ 。(不定项)
(2)已知CaF2的晶胞边长为5.4626×10-10m。则萤石的密度为______ g•cm-3。(保留两位小数)
(1)下列说法正确的是

| A.CaF2属于共价晶体 | B.晶胞中有4个Ca2+ |
| C.与Ca2+最近的F-有8个 | D.与F-最近的Ca2+有6个 |
(2)已知CaF2的晶胞边长为5.4626×10-10m。则萤石的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】科学工作者合成了含镁、镍、碳3种元素的超导材料,具有良好的应用前景。回答下列问题:
在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中,晶胞如图所示。

①组成该晶体的化学式为___________ 。
②完全由镍原子构成的八面体空隙与由镍原子和镁原子共同构成的八面体空隙的数量比为___________ ,由镍原子和镁原子共同构成的八面体空隙中镍原子和镁原子的数量比为___________ 。
③若取碳原子为晶胞顶点,则镍原子位于晶胞的___________ 位置。
在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中,晶胞如图所示。

①组成该晶体的化学式为
②完全由镍原子构成的八面体空隙与由镍原子和镁原子共同构成的八面体空隙的数量比为
③若取碳原子为晶胞顶点,则镍原子位于晶胞的
您最近一年使用:0次
填空题
|
适中
(0.65)
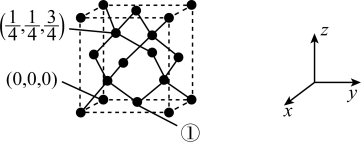
【推荐1】晶体硅的晶胞如下,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。则图中原子①的原子坐标是_______ ,晶体中硅原子的空间利用率为_______ (用含π的式子表示)。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为______ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下图为几种晶体或晶胞的示意图:

请回答下列问题:
(1)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为_____ 。
(2)MgO晶体中,距每个O2-最近且距离相等的O2-有_____ 个。
(3)每个Cu晶胞中实际占有_____ 个Cu原子;CaCl2晶体中Ca2+的配位数为_____ 。
(4)冰的熔点远高于干冰,除 H2O 是极性分子、CO2是非极性分子外, 还有一个重要的原因是____ 。
(5)金刚石晶胞含有_________ 个碳原子;若碳原子半径为 r,根据硬球接触模型,列式表示碳原子在晶胞中的空间占有率_____ (计算结果为含π的分数,不要化为小数或百分数)。

请回答下列问题:
(1)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为
(2)MgO晶体中,距每个O2-最近且距离相等的O2-有
(3)每个Cu晶胞中实际占有
(4)冰的熔点远高于干冰,除 H2O 是极性分子、CO2是非极性分子外, 还有一个重要的原因是
(5)金刚石晶胞含有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】金属的常见堆积方式有三种,配位数为8的是________ 堆积,铜属于________ 堆积.
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】干冰、石墨、C60、氟化钙和金刚石的结构模型如下(石墨仅表示其中的一层结构):
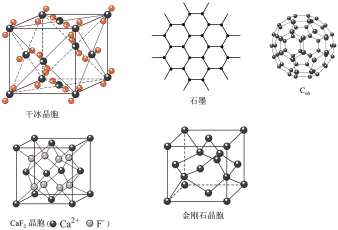
回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有________ 个与之紧邻且等距的CO2分子。
(2)由金刚石晶胞可知,每个金刚石晶胞占有________ 个碳原子。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是________ 。
(4)在CaF2晶体中,Ca2+的配位数是________ ,F-的配位数是________ 。
(5)固态时,C60属于________ (填“共价”或“分子”)晶体。

回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有
(2)由金刚石晶胞可知,每个金刚石晶胞占有
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是
(4)在CaF2晶体中,Ca2+的配位数是
(5)固态时,C60属于
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】干冰、石墨、C60、氟化钙和金刚石的结构模型如图所示(石墨仅表示出其中的一层结构):
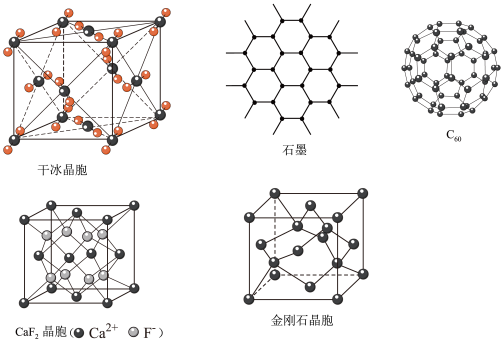
回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有________ 个与之紧邻且等距的CO2分子。
(2)由金刚石晶胞可知,每个金刚石晶胞占有________ 个碳原子。
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是________ 。
(4)在CaF2晶体中,Ca2+的配位数是________ ,F-的配位数是________ 。
(5)固态时,C60属于________ (填“原子”或“分子”)晶体。

回答下列问题:
(1)干冰晶胞中,每个CO2分子周围有
(2)由金刚石晶胞可知,每个金刚石晶胞占有
(3)石墨层状结构中,平均每个正六边形占有的碳原子数是
(4)在CaF2晶体中,Ca2+的配位数是
(5)固态时,C60属于
您最近一年使用:0次



