氮及其化合物在自然界中存在循环,请回答下列问题:
(1)氮元素在周期表中的位置是_______ 。
(2)氨气分子的结构式为_______ ,N2的电子式为_______ 。
(3)CN-中N元素显-3价,说明非金属性N_______ C(填“>”或“<”),请写出一个能比较N和C非金属性强弱的化学事实:_______ 。
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:_______ 。
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体_______ L(标准状态)。
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是_______ (用电离方程式解释),常见氮肥种类有_______ (列举两个)。
(1)氮元素在周期表中的位置是
(2)氨气分子的结构式为
(3)CN-中N元素显-3价,说明非金属性N
(4)NO2是燃油汽车尾气中的主要污染物之一。
①在催化剂和加热条件下,NO2与NH3可反应生成无害物质,请写出反应的化学方程式:
②实验室可用烧碱溶液吸收NO2和NO,(已知2NO2+2NaOH=NaNO2+NaNO3+H2O,NO2+NO+2NaOH=2NaNO2+H2O),当消耗100mL0.5mol·L-1的烧碱溶液时,共吸收混合气体
(5)氨水是一种很好的氮肥,常温下测定0.1mol·L-1氨水溶液,其OH-浓度小于0.1mol·L-1,其原因是
更新时间:2022-07-13 11:05:21
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列物质:CO2、N2、CaCl2、NH4Cl、NaOH、H2O2、Na2O2。
(1)属于共价化合物的有_______________ ,含有非极性键的离子化合物的是__________ 。
(2)N2、CO2的结构式分别为________________ 、_________________ 。
(3)分别写出NaOH、H2O2、Na2O2的电子式:_______________ 、_____________ 、______________ 。
(1)属于共价化合物的有
(2)N2、CO2的结构式分别为
(3)分别写出NaOH、H2O2、Na2O2的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知H与O可以形成 H2O和H2O2两种化合物。请完成下列空白:
(1)H2O内的O−H、水分子间的范德华力和氢键,从强到弱依次为___________ 。
(2)H+可与 H2O 形成H3O+,H3O+中O采用___________ 杂化。H3O+中H−O−H键角比H2O中的___________ ,原因为___________ 。
(3)H2O2是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。H2O2的电子式是___________ ,结构式是___________ 。H2O2是含有___________ 键和___________ 键的___________ 分子(填"极性"或"非极性")。H2O2能与水混溶,却不溶于CCl4。请予以解释:___________ 。

(1)H2O内的O−H、水分子间的范德华力和氢键,从强到弱依次为
(2)H+可与 H2O 形成H3O+,H3O+中O采用
(3)H2O2是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。H2O2的电子式是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】NaClO溶液具有漂白能力,已知25℃时, ,向含有NaOH的NaClO溶液中逐滴滴入
,向含有NaOH的NaClO溶液中逐滴滴入 溶液,滴加过程中溶液的pH随
溶液,滴加过程中溶液的pH随 溶液的体积的变化曲线及实验现象见下表。
溶液的体积的变化曲线及实验现象见下表。
(1)NaClO的电子式是_______ ,次氯酸钠溶液中离子浓度大小顺序是:_______ 。
(2)25℃,pH=7.0的NaClO和HClO的混合溶液中,[HClO]_______ [ ] (填<,>或=)。
] (填<,>或=)。
 ,向含有NaOH的NaClO溶液中逐滴滴入
,向含有NaOH的NaClO溶液中逐滴滴入 溶液,滴加过程中溶液的pH随
溶液,滴加过程中溶液的pH随 溶液的体积的变化曲线及实验现象见下表。
溶液的体积的变化曲线及实验现象见下表。| 变化曲线 | 实验现象 |
 | ⅰ.A→B产生红褐色沉淀 ⅱ.B→C红褐色沉淀的量增多 ⅲ.C→D红褐色沉淀的量增多 ⅳ.D点附近产生有刺激性气味的气体 ⅴ.D→E红褐色沉淀的量略有增多 |
(2)25℃,pH=7.0的NaClO和HClO的混合溶液中,[HClO]
 ] (填<,>或=)。
] (填<,>或=)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。

(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是_____________________ 。
(2)B中加入的是______________ ,其作用是______________________ 。
(3)实验时在C中观察到的现象是_____________________ ,发生反应的化学方程式是:_______________ 。
(4)E中收集到的物质是________ 。

(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是
(2)B中加入的是
(3)实验时在C中观察到的现象是
(4)E中收集到的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮氧化物、二氧化硫能引发酸雨、雾霾等。回答下列问题:
(1) 产生硝酸型酸雨的化学方程式为
产生硝酸型酸雨的化学方程式为_______ 。
(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为_______ 。
(3)目前工业上烟气脱硫脱硝的工艺流程如下:

已知:烟气中含尘、 、NOx(
、NOx(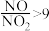 )。
)。
①“催化氧化”的目的是_______ 。
②图中产品中含硫成分为_______ (填化学式)。
(4)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

分离器的作用是_______ ,写出氧化炉中的化学反应方程式:_______ 。
(1)
 产生硝酸型酸雨的化学方程式为
产生硝酸型酸雨的化学方程式为(2)汽车尾气催化转化器可将尾气中的CO、NO均转化为无害气体,该反应的还原产物为
(3)目前工业上烟气脱硫脱硝的工艺流程如下:

已知:烟气中含尘、
 、NOx(
、NOx(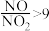 )。
)。①“催化氧化”的目的是
②图中产品中含硫成分为
(4)氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。

分离器的作用是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】根据所学知识,回答下列问题:
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是___ 。
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是___ 。
(3)检验氨气是否已经收集满的方法是__ ;为了得到干燥的NH3,用__ 干燥剂。
A.碱石灰 B.浓H2SO4 C.无水CaCl2 D.P2O5
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是___ (用化学方程式表示)。
(5)下列变化为化学变化的是___ (填标号)。
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
(1)“元时,南安有黄长者,为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之。”泥土能将红糖变白糖,其表现的性质是
(2)用鸡蛋壳膜和蒸馏水可除去淀粉胶体中的食盐,其原理是
(3)检验氨气是否已经收集满的方法是
A.碱石灰 B.浓H2SO4 C.无水CaCl2 D.P2O5
(4)工业上常用浓氨水检验输送氯气的管道是否泄漏(若泄漏,则有白烟生成),其原理是
(5)下列变化为化学变化的是
A.CaCl2的潮解 B.钠的焰色反应 C.常温下,Fe遇浓硫酸钝化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】有下列六种物质的溶液:①Na2CO3 ②Al2(SO4)3 ③CH3COOH ④NaHCO3 ⑤HCl ⑥Al(OH)3
(1)pH值相同的③和⑤,分别用蒸馏水稀释至原来的 倍和
倍和 倍,稀释后两溶液的
倍,稀释后两溶液的 值仍然相同,则
值仍然相同,则
______  (填“<”或“>”或“=”)
(填“<”或“>”或“=”)
(2)室温下, 值为11的①溶液中,由水电离出来的c(OH—)=
值为11的①溶液中,由水电离出来的c(OH—)=______
(3)写出①溶液的电荷守恒:____________ 。
(4)写出⑥的酸式电离方程式:________________
(5)用②和④的溶液可以制作泡沫灭火剂,其原理为:________________ (用离子方程式解释)
(6)已知反应NH4++HCO3-+H2O⇌NH3·H2O+H2CO3,该反应平衡常数K=_____ 。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka1=4×10-7,Ka2=4×10-11)
(1)pH值相同的③和⑤,分别用蒸馏水稀释至原来的
 倍和
倍和 倍,稀释后两溶液的
倍,稀释后两溶液的 值仍然相同,则
值仍然相同,则
 (填“<”或“>”或“=”)
(填“<”或“>”或“=”)(2)室温下,
 值为11的①溶液中,由水电离出来的c(OH—)=
值为11的①溶液中,由水电离出来的c(OH—)=(3)写出①溶液的电荷守恒:
(4)写出⑥的酸式电离方程式:
(5)用②和④的溶液可以制作泡沫灭火剂,其原理为:
(6)已知反应NH4++HCO3-+H2O⇌NH3·H2O+H2CO3,该反应平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在常温下,0.1 mol/L一元酸HB溶液的pH=3,试回答下列问题:
(1)HB在水溶液中的电离方程式为___________
(2)在常温下,0.1 mol/L一元酸HB溶液,Ka=___________
(3)若将温度改变到t℃(此时Kw=10-12),则t___________ 25℃(填“<”、“>”或“=”),该温度下0.1 mol/L一元酸HB溶液中由水电离出的H+物质的量浓度___________ 。
A.10-11 mol/L B.10-9 mol/L C.10-6 mol/L D.以上答案都不正确
(1)HB在水溶液中的电离方程式为
(2)在常温下,0.1 mol/L一元酸HB溶液,Ka=
(3)若将温度改变到t℃(此时Kw=10-12),则t
A.10-11 mol/L B.10-9 mol/L C.10-6 mol/L D.以上答案都不正确
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)①H3PO2是一元中强酸,写出其电离方程式______________________ 。
②NaH2PO2为___________ (填“正盐”或“酸式盐”),其溶液显___________ (填“弱酸性”“中性”或“弱碱性”)。
③H3PO2中,P元素的化合价为___________ ;
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为________ 。
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应,写出白磷与Ba(OH)2溶液反应的化学方程式______________________ 。
(1)①H3PO2是一元中强酸,写出其电离方程式
②NaH2PO2为
③H3PO2中,P元素的化合价为
(2)H3PO2可用于化学镀银,反应中Ag+还原为银,H3PO2氧化为H3PO4,该反应中氧化剂与还原剂的物质的量之比为
(3)H3PO2的工业制法是:将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H2PO2)2,后者再与H2SO4 反应,写出白磷与Ba(OH)2溶液反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】富硒酵母、二氧化硅、硫黄等食品添加剂用于食品生产中,丰富舌尖上的营养和美味。请回答下列问题:
(1)富硒酵母是一种新型添加剂,34Se在元素周期表中的位置为___________ 。
(2)下列说法正确的是___________(填字母)。
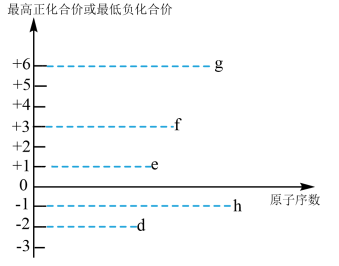
(3)短周期元素d、e、f、g、h都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:
①g的最简单氢化物中含有的化学键类型为___________ (填字母)。
A.离子键 B.非极性共价键 C.极性共价键
②d、e、f、g、h元素形成的简单离子中,半径最大的离子结构示意图为___________ 。
③e和d组成的淡黄色固体的电子式为___________ 。
④写出一种比较e、f两种元素金属性的方法___________ 。
(1)富硒酵母是一种新型添加剂,34Se在元素周期表中的位置为
(2)下列说法正确的是___________(填字母)。
| A.稳定性:H2Se>H2S>H2O | B.36S与74Se的中子数之和为60 |
| C.酸性:H2SeO4>H2SO4>HClO4 | D.还原性:S2>Se2﹣ |
(3)短周期元素d、e、f、g、h都可能存在于某些食品添加剂中,其最高正化合价或最低负化合价与原子序数的关系如图所示:

①g的最简单氢化物中含有的化学键类型为
A.离子键 B.非极性共价键 C.极性共价键
②d、e、f、g、h元素形成的简单离子中,半径最大的离子结构示意图为
③e和d组成的淡黄色固体的电子式为
④写出一种比较e、f两种元素金属性的方法
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列事实能说明X元素比Y元素的非金属性强的有_____
①与H2化合时X单质比Y单质容易;
②X单质可以把Y从其氢化物中置换出来;
③X的最高价氧化物对应水化物的酸性比Y的最高价氧化物对应水化物的酸性强;
④与金属反应时,X原子得电子数目比Y的多;
⑤X的单质熔、沸点比Y的低;
⑥X原子的最外层电子数比Y原子的最外层电子数多
①与H2化合时X单质比Y单质容易;
②X单质可以把Y从其氢化物中置换出来;
③X的最高价氧化物对应水化物的酸性比Y的最高价氧化物对应水化物的酸性强;
④与金属反应时,X原子得电子数目比Y的多;
⑤X的单质熔、沸点比Y的低;
⑥X原子的最外层电子数比Y原子的最外层电子数多
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】硫和硒(34Se)在元素周期表中位于同一主族,均是生产生活中重要的非金属元素。
(1)含+4价硫元素的化合物有SO2、H2SO3和X等。
①SO2使品红溶液褪色,说明SO2具有的化学性质是___________ 。
②已知X属于钠盐。写出X转化为SO2的化学方程式:___________ 。
③从下列试剂中任选一种试剂:浓硫酸、酸性高锰酸钾溶液、氯水、硫化钠溶液,设计实验证明SO2中硫元素的化合价在化学反应中可以发生变化(写出一种方案即可),填写下表。
(2)以工业硒为原料制备高纯硒时的主要物质转化如下图。___________ (填字母序号)。
a.硒原子的最外层有6个电子 b.硒元素的非金属性强于硫元素的非金属性
c.SeO2属于酸性氧化物 d.过程i中硒被氧化
②过程iii中使用的还原剂为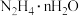 ,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的
,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的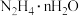 的物质的量之比为
的物质的量之比为___________ (工业硒中杂质与O2的反应可忽略)。
(1)含+4价硫元素的化合物有SO2、H2SO3和X等。
①SO2使品红溶液褪色,说明SO2具有的化学性质是
②已知X属于钠盐。写出X转化为SO2的化学方程式:
③从下列试剂中任选一种试剂:浓硫酸、酸性高锰酸钾溶液、氯水、硫化钠溶液,设计实验证明SO2中硫元素的化合价在化学反应中可以发生变化(写出一种方案即可),填写下表。
| 选择的试剂 | 转化后的含硫物质 | 预期现象 |
(2)以工业硒为原料制备高纯硒时的主要物质转化如下图。
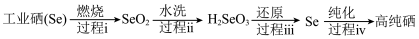
a.硒原子的最外层有6个电子 b.硒元素的非金属性强于硫元素的非金属性
c.SeO2属于酸性氧化物 d.过程i中硒被氧化
②过程iii中使用的还原剂为
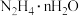 ,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的
,对应产物是N2.理论上,过程i消耗的O2与过程iii消耗的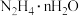 的物质的量之比为
的物质的量之比为
您最近一年使用:0次



