1 . 已知四种酸的电离平衡常数如下表,其中酸性最强的是
| 弱酸 | 次氯酸 | 醋酸 | 碳酸 | 硫化氢 |
| 电离平衡常数 | Ka=4.7×10-8 | Ka=1.7×10-5 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-12 |
| A.醋酸 | B.次氯酸 | C.碳酸 | D.硫化氢 |
您最近半年使用:0次
2 . 已知常温下水溶液中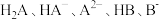 的分布分数
的分布分数 [如
[如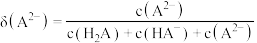 ]随
]随 变化曲线如图1所示;用
变化曲线如图1所示;用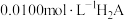 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和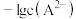 关系如图2所示。下列说法错误的是
关系如图2所示。下列说法错误的是
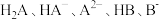 的分布分数
的分布分数 [如
[如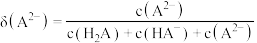 ]随
]随 变化曲线如图1所示;用
变化曲线如图1所示;用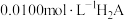 溶液滴定
溶液滴定 溶液,溶液中
溶液,溶液中 和
和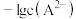 关系如图2所示。下列说法错误的是
关系如图2所示。下列说法错误的是
A.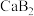 的水解平衡常数的数量级为 的水解平衡常数的数量级为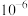 |
B.曲线e为 |
C. |
D.滴定过程中始终存在: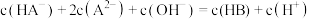 |
您最近半年使用:0次
3 . 下表是几种弱酸常温下的电离常数:
(1)写出 的电离方程式
的电离方程式___________ 。
(2) 四种酸的酸性由强到弱的顺序为
四种酸的酸性由强到弱的顺序为___________ 。
(3)写出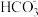 的水解方程式
的水解方程式___________ 。
(4)同浓度的 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为___________ 。
 |  |  |  |
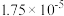 | 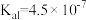 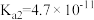 | 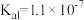 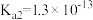 |  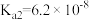 |
(1)写出
 的电离方程式
的电离方程式(2)
 四种酸的酸性由强到弱的顺序为
四种酸的酸性由强到弱的顺序为(3)写出
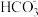 的水解方程式
的水解方程式(4)同浓度的
 结合
结合 的能力由强到弱的顺序为
的能力由强到弱的顺序为
您最近半年使用:0次
名校
解题方法
4 . 25℃时,用0.1
 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 、
、 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是

 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 与
与 值、微粒分布分数
值、微粒分布分数 ,X表示
,X表示 、
、 或
或 ]的关系如图所示,下列说法正确的是
]的关系如图所示,下列说法正确的是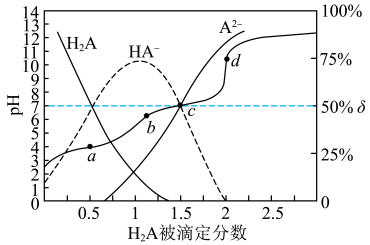
A.用 溶液滴定0.1 溶液滴定0.1 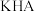 溶液可以用酚酞作指示剂 溶液可以用酚酞作指示剂 |
B.25℃时, 第二步电离平衡常数 第二步电离平衡常数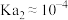 |
C.c点溶液中: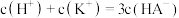 |
D.a、b、c、d四点溶液中水的电离程度: |
您最近半年使用:0次
昨日更新
|
276次组卷
|
3卷引用:云南省大理白族自治州2024届高三第二次复习统一检测理综-化学试卷
解题方法
5 . 亚砷酸 在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法
在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法不正确 的是
 在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法
在溶液中存在多种微粒形态,KOH溶液滴入亚砷酸溶液,各种微粒物质的量分数与溶液pH关系如图所示。下列说法
A. 的 的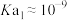 |
B.由图像信息可知 为三元弱酸 为三元弱酸 |
C.当pH调至8~11时,主要反应的离子方程式为 |
D. 时溶液中: 时溶液中: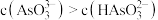 |
您最近半年使用:0次
6 . 常温下,用0.5mol·L-1NaHCO3溶液滴定25.00mL0.25mol·L-1CaCl2溶液,消耗NaHCO3溶液的体积与混合液pH关系如下图所示。滴定过程中有白色沉淀生成,但整个过程未见气泡产生。已知:碳酸Ka1=4.5×10-7,Ka2=4.7×10-11;Ksp(CaCO3)=3.4×10-9。下列说法正确的是
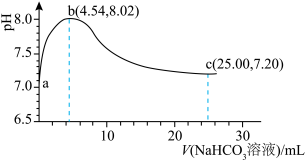
| A.ab段溶液有白色沉淀生成 |
B.ab段pH升高的主要原因: +Ca2+=CaCO3↓+H+ +Ca2+=CaCO3↓+H+ |
C.b点:c( )>c(H2CO3) )>c(H2CO3) |
D.c点2c( )+c( )+c( )<2c(Ca2+) )<2c(Ca2+) |
您最近半年使用:0次
7 . 向10mLHCOOH-NH4Cl混合溶液(浓度均为0.1mol·L−1)中滴加0.1mol·L−1NaOH溶液,并监测溶液pH变化,实验数据如图。由该实验可得到的结论是
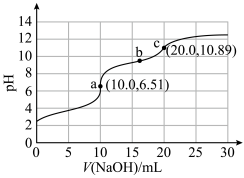
| A.HCOOH电离方程式为HCOOH=H++HCOO− |
| B.由a点数据可推出电离能力:HCOOH>NH3·H2O |
| C.b点溶液中的OH−主要来自HCOO−水解 |
| D.0.05mol·L−1氨水的pH<10.89 |
您最近半年使用:0次
8 . 室温下,向Mg(NO3)2溶液、HF溶液、CH3CH2COOH溶液中分别滴加NaOH溶液,测得溶液中pH与pX[pX=-lgX,X代表 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是
已知:
 、
、 、
、 ]的关系如图所示。
]的关系如图所示。
 ,HF的酸性比CH3CH2COOH强。下列叙述正确的是
,HF的酸性比CH3CH2COOH强。下列叙述正确的是已知:

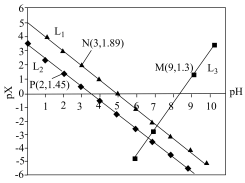
A. 代表的是pH与 代表的是pH与 的关系 的关系 |
B. 的 的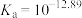 |
C.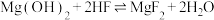 的 的 |
| D.含相同浓度NaF、HF的混合溶液的pH>7 |
您最近半年使用:0次
9 . 氧化钪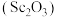 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪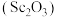 的一种流程如下图。
的一种流程如下图。

回答下列问题:
(1)基态钪原子的价层电子排布式为___________ 。
(2)“萃取”时,钛白工业废酸中加入 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的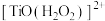 ,其中钛的化合价为
,其中钛的化合价为___________ ; 的作用是
的作用是___________ (填标号)。
A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将 试剂沿烧杯内壁缓慢注入
试剂沿烧杯内壁缓慢注入 试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入
试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入 试剂中,并不断搅拌,则A、C分别对应上述试剂中的
试剂中,并不断搅拌,则A、C分别对应上述试剂中的___________ 、___________ 。
(4)萃取剂萃取 的原理为
的原理为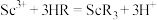 (
( 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成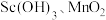 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为___________ 。 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为___________  (已知:
(已知: 时,
时,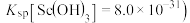 。
。
(5)“沉钪”时用到草酸。已知草酸的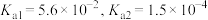 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中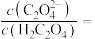
___________ 。
(6)在空气中焙烧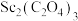 只生成一种碳氧化物的化学方程式为
只生成一种碳氧化物的化学方程式为___________ 。
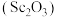 可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含
可用作半导体镀层的蒸镀材料,也可制成可变波长的固体激光器和高清晰度的电视电子枪、金属卤化物灯等。以钛白工业废酸(含 、
、 等离子)为原料制备氧化钪
等离子)为原料制备氧化钪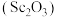 的一种流程如下图。
的一种流程如下图。
回答下列问题:
(1)基态钪原子的价层电子排布式为
(2)“萃取”时,钛白工业废酸中加入
 可降低钛的萃取率,可能是生成了难萃取的
可降低钛的萃取率,可能是生成了难萃取的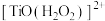 ,其中钛的化合价为
,其中钛的化合价为 的作用是
的作用是A.作氧化剂 B.作还原剂 C.提供配体
(3)“洗涤”时,洗涤剂是用
 和
和 三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将
三种试剂按一定比例混合而成。实验室中混合三种试剂的操作是:将 试剂沿烧杯内壁缓慢注入
试剂沿烧杯内壁缓慢注入 试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入
试剂中,并用玻璃棒不断搅拌,冷却后再将所得混合液缓慢注入 试剂中,并不断搅拌,则A、C分别对应上述试剂中的
试剂中,并不断搅拌,则A、C分别对应上述试剂中的(4)萃取剂萃取
 的原理为
的原理为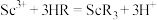 (
( 代表萃取剂)。在“反萃取”中,加入
代表萃取剂)。在“反萃取”中,加入 溶液后生成
溶液后生成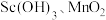 等物质,其中生成含
等物质,其中生成含 化合物的化学方程式为
化合物的化学方程式为 时,经“反萃取”后所得滤液的
时,经“反萃取”后所得滤液的 ,则残留的
,则残留的 浓度为
浓度为 (已知:
(已知: 时,
时,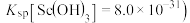 。
。(5)“沉钪”时用到草酸。已知草酸的
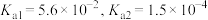 ,则在
,则在 时,
时, 的草酸溶液中
的草酸溶液中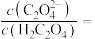
(6)在空气中焙烧
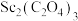 只生成一种碳氧化物的化学方程式为
只生成一种碳氧化物的化学方程式为
您最近半年使用:0次
10 . Al3+与F-具有很强的亲和性,AlF在NaF溶液中存在分步电离: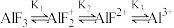 。常温下实验测定
。常温下实验测定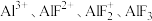 的百分含量随
的百分含量随 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
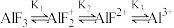 。常温下实验测定
。常温下实验测定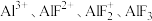 的百分含量随
的百分含量随 变化如图所示,下列说法错误的是
变化如图所示,下列说法错误的是
A.曲线b表示 |
B.N点时, |
C.M点溶液中 |
D.常温下, 化学平衡常数的数量级为1015 化学平衡常数的数量级为1015 |
您最近半年使用:0次



