解题方法
1 . 溶液法制取LiBF4的流程如下: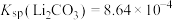 ,
,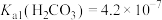 ,
,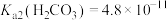 ;
;
ⅱ.反应①可以表示为: 。
。
(1)写出反应②的化学方程式:___________ 。室温条件下,反应②完成后若溶液中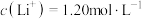 ,pH=8.0,则此时溶液中
,pH=8.0,则此时溶液中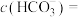
___________ 。
(2)对LiBF4粗品进一步提纯的方法称为______________ 。
(3)写出固相-气相接触法较溶液法制取LiBF4的一项优势:__________ 。

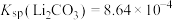 ,
,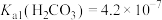 ,
,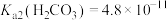 ;
;ⅱ.反应①可以表示为:
 。
。(1)写出反应②的化学方程式:
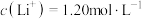 ,pH=8.0,则此时溶液中
,pH=8.0,则此时溶液中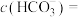
(2)对LiBF4粗品进一步提纯的方法称为
(3)写出固相-气相接触法较溶液法制取LiBF4的一项优势:
您最近半年使用:0次
2 .  为二元弱酸,常温下,现配制一组
为二元弱酸,常温下,现配制一组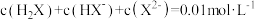 的溶液,在不同pH环境下,不同形态的含X粒子(
的溶液,在不同pH环境下,不同形态的含X粒子( 、
、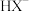 、
、 )的分布系数
)的分布系数 (平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
(平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
 为二元弱酸,常温下,现配制一组
为二元弱酸,常温下,现配制一组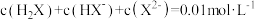 的溶液,在不同pH环境下,不同形态的含X粒子(
的溶液,在不同pH环境下,不同形态的含X粒子( 、
、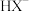 、
、 )的分布系数
)的分布系数 (平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
(平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是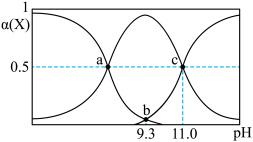
| A.a点对应的溶液的pH为7.6 |
B.在NaHX溶液中存在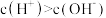 |
C.c点对应的溶液中存在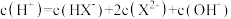 |
D.室温下,a、b、c三点对应的溶液中,由水电离出的 与 与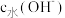 的乘积 的乘积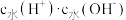 数值由大到小顺序:a>b>c 数值由大到小顺序:a>b>c |
您最近半年使用:0次
2024-04-18更新
|
146次组卷
|
2卷引用:2024届”3+3+3“高考备考诊断性联考卷(二)理综试题-高中化学
3 . 缓冲溶液在生产生活中有广泛应用,某缓冲溶液存在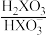 和
和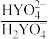 缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示
缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示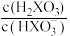 或
或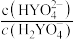 与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为
与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为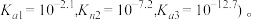
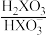 和
和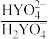 缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示
缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示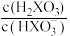 或
或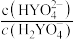 与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为
与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为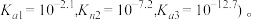
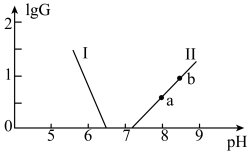
| A.H2XO3的Ka1的数量级为10-7 |
| B.a→b的过程中,水的电离程度逐渐增大 |
C.当溶液pH逐渐增大时,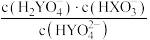 逐渐增大 逐渐增大 |
D.当 时, 时,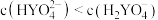 |
您最近半年使用:0次
4 . 常温下,往0.35 mol/LCa(ClO)2溶液中通入CO2。
已知:Ka(HClO)=4.0×10-8,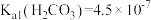 ,Ka2(H2CO3)=4.7×10-11,Ksp(CaCO3)=3.4×10-9
,Ka2(H2CO3)=4.7×10-11,Ksp(CaCO3)=3.4×10-9
下列说法不正确 的是
已知:Ka(HClO)=4.0×10-8,
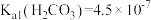 ,Ka2(H2CO3)=4.7×10-11,Ksp(CaCO3)=3.4×10-9
,Ka2(H2CO3)=4.7×10-11,Ksp(CaCO3)=3.4×10-9下列说法
| A.通入一定量CO2后溶液pH=7,未出现CaCO3沉淀 |
| B.往Ca(ClO)2溶液中加盐酸酸化,将有Cl2生成 |
| C.通入一定量CO2后溶液中c(HClO)=c(C1O-),滴入酚酞试剂,溶液一直呈无色 |
D.已知自然条件下,饱和碳酸溶液的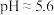 ,则自然条件下饱和碳酸溶液中存在c(H+)>c( ,则自然条件下饱和碳酸溶液中存在c(H+)>c( )>c(OH-)>c( )>c(OH-)>c( ) ) |
您最近半年使用:0次
解题方法
5 . 结合已有知识,根据下列实验操作,其对应的现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将乙醇和浓硫酸混合溶液加热到170℃,并将产生的气体经过氢氧化钠溶液洗气,再通入溴水 | 溴水褪色 | 有乙烯生成 |
| B | 常温下将铁片分别插入稀硝酸和浓硝酸中 | 前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
| C | 已知 : : 、 、 : :  ,向饱和溶液中滴加碳酸钠溶液 ,向饱和溶液中滴加碳酸钠溶液 | 无明显现象 |  与碳酸钠不反应 与碳酸钠不反应 |
| D | 向少量 悬浊液中加入足量饱和 悬浊液中加入足量饱和 溶液 溶液 | 沉淀颜色会由黑色变为浅红色( 为浅红色) 为浅红色) | Ksp(FeS)>Ksp(MnS) |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
6 . 生物质铁炭纳米材料可以活化过一硫酸盐,降解废水中有机污染物.
(1)生物质铁炭纳米材料活化过—硫酸钾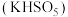 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中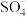 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基. (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: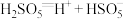 、
、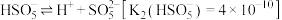 .写出
.写出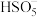 的结构式:
的结构式:_______ 。
②生物质铁炭纳米材料降解有机污染物的机理可描述为______ 。
③若有机污染物为苯酚,写出酸性条件下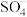 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:______ 。
(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:______ 。
(3)铁炭纳米材料在不同 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是:______ 。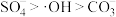 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是:______ 。
(1)生物质铁炭纳米材料活化过—硫酸钾
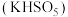 降解有机污染物的反应历程如图-1所示.图中
降解有机污染物的反应历程如图-1所示.图中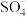 和
和 分别表示硫酸根自由基和羟基自由基.
分别表示硫酸根自由基和羟基自由基.
 (S的化合价为
(S的化合价为 )在水中的电离过程为:
)在水中的电离过程为: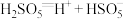 、
、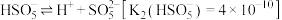 .写出
.写出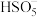 的结构式:
的结构式:②生物质铁炭纳米材料降解有机污染物的机理可描述为
③若有机污染物为苯酚,写出酸性条件下
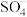 与苯酚反应的化学方程式:
与苯酚反应的化学方程式:(2)与直接使用纳米铁颗粒相比,使用生物质铁炭纳米材料降解的优点是:
(3)铁炭纳米材料在不同
 对有机污染物去除率(
对有机污染物去除率( 溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示,
溶液有机物浓度与初始有机物浓度的比值)的影响如图-2所示, 越小有机污染物去除率越高的原因是:
越小有机污染物去除率越高的原因是: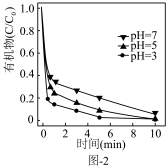
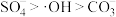 。水中存在一定量
。水中存在一定量 和无
和无 存在时对铁炭纳米材料降解有机污染物的影响如图-3所示.
存在时对铁炭纳米材料降解有机污染物的影响如图-3所示. 的存在对有机污染物的降解有影响,原因是:
的存在对有机污染物的降解有影响,原因是: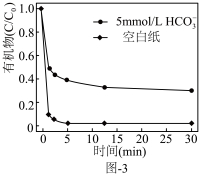
您最近半年使用:0次
解题方法
7 . 硫代硫酸钠的制备和应用相关流程如图所示,下列有关离子方程式书写正确的是 。
。
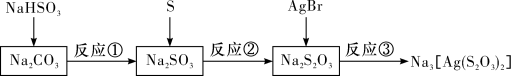
 。
。A.反应③: |
B.向 溶液中加入稀硫酸: 溶液中加入稀硫酸: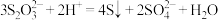 |
C.用 溶液测定碘单质的含量时生成 溶液测定碘单质的含量时生成 ,其离子反应方程式为 ,其离子反应方程式为 |
D.反应①: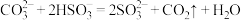 |
您最近半年使用:0次
8 . 25℃时,向20mL0.1 mol∙L-1HA溶液中逐滴加入0.1 mol∙L-1NaOH溶液,pH变化曲线如下图所示。下列说法不正确的

| A.HA电离平衡常数的数量级为10-5 |
| B.a点→c点的过程中水的电离度持续增大 |
| C.b点溶液中c(Na+)=c(A-) |
D.a点溶液中微粒浓度: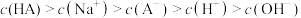 |
您最近半年使用:0次
9 . 下列说法或表示正确的是
A.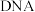 双螺旋结构中的两条多聚核苷酸链间通过共价键相互结合 双螺旋结构中的两条多聚核苷酸链间通过共价键相互结合 |
B. 要在光照和点燃条件下才反应,所以 要在光照和点燃条件下才反应,所以 , , |
C.已知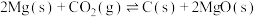 ,达平衡后,缩小容器体积, ,达平衡后,缩小容器体积, 浓度增大 浓度增大 |
D.将 的醋酸稀释为 的醋酸稀释为 的过程中, 的过程中, 减小 减小 |
您最近半年使用:0次
名校
10 . 常温下,用0.1mol/L硝酸溶液滴定25.00mL0.1mol/LMOH(一元弱碱)溶液,滴定过程中,溶液的pH、M+和MOH的物质的量分数与滴加硝酸溶液体积的关系如图所示。下列叙述错误的是

| A.可选择甲基橙为指示剂判断滴定终点 |
| B.溶液导电能力:a点小于b点 |
| C.MOH电离平衡常数的数量级为10-5 |
| D.图中V1>12.5mL |
您最近半年使用:0次



