解题方法
1 . 有一种有机三元弱酸广泛存在于水果中,用 表示,
表示, 时,用
时,用 调节
调节 溶液的
溶液的 ,溶液中含各种微粒的分布系数
,溶液中含各种微粒的分布系数 与
与 的关系如图所示[比如
的关系如图所示[比如 的分布系数:
的分布系数: ],下列叙述正确的是
],下列叙述正确的是
 表示,
表示, 时,用
时,用 调节
调节 溶液的
溶液的 ,溶液中含各种微粒的分布系数
,溶液中含各种微粒的分布系数 与
与 的关系如图所示[比如
的关系如图所示[比如 的分布系数:
的分布系数: ],下列叙述正确的是
],下列叙述正确的是
A.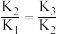 | B.曲线1代表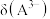 ,曲线4代表 ,曲线4代表 |
C.反应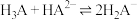 的 的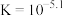 | D.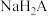 溶液、 溶液、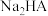 溶液都显酸性 溶液都显酸性 |
您最近一年使用:0次
解题方法
2 . 已知:①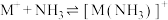

②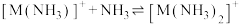

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是
{分布分数 }
}
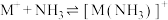

②
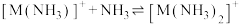

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是{分布分数
 }
}
A. |
B.曲线b代表 |
C.加水稀释,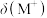 减小 减小 |
D.当 时, 时, 为含M粒子的主要存在形式 为含M粒子的主要存在形式 |
您最近一年使用:0次
名校
3 . 催化剂形貌的优化会影响生产效率。 可做烟气脱硝工艺的固相催化剂。
可做烟气脱硝工艺的固相催化剂。
已知:
ⅰ.常温下,AgOH极不稳定,易分解为难溶于水的 固体;
固体; ;
; 。
。
ⅱ.一般情况,析晶速率越快,晶粒尺寸越小。
(1)基态P原子的核外电子有____ 个空间运动状态,Ag、P、O元素的电负性由大到小的顺序为_______ 。
(2)某研究组调控反应条件控制 晶体形貌。
晶体形貌。
①常温下,向银氨溶液逐滴加入 溶液制得
溶液制得 晶体,完善该反应的离子方程式
晶体,完善该反应的离子方程式_______ 。

②在不同pH条件下,向 溶液中加入
溶液中加入 溶液制得磷酸银收率如图所示。样品A的晶粒较小,请从平衡移动与速率的角度解释原因
溶液制得磷酸银收率如图所示。样品A的晶粒较小,请从平衡移动与速率的角度解释原因_____________ 。___________
A.样品A中 杂质含量最高
杂质含量最高
B.可加入盐酸调控体系的pH制得不同样品
C.向 溶液中加入少量
溶液中加入少量 溶液时,溶液中
溶液时,溶液中 减小
减小
D.向 溶液中加入
溶液中加入 溶液得到晶粒尺寸与上述样品相同
溶液得到晶粒尺寸与上述样品相同
(3)研究组发现: 溶液与0.2
溶液与0.2
 溶液等体积混合也能制得
溶液等体积混合也能制得 。
。
①刚开始生成 沉淀时,溶液中的
沉淀时,溶液中的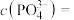
___________ 。
②常温下溶液中含磷物种的分布系数 ,
, 或
或 与pH的关系如图所示,则磷酸的一级电离平衡常数
与pH的关系如图所示,则磷酸的一级电离平衡常数
_________ 。 由
由 第一步电离决定,可表示为
第一步电离决定,可表示为 ,当生成
,当生成 沉淀时,溶液中
沉淀时,溶液中 至少为
至少为___________  (写出计算过程)。
(写出计算过程)。
 可做烟气脱硝工艺的固相催化剂。
可做烟气脱硝工艺的固相催化剂。已知:
ⅰ.常温下,AgOH极不稳定,易分解为难溶于水的
 固体;
固体; ;
; 。
。ⅱ.一般情况,析晶速率越快,晶粒尺寸越小。
(1)基态P原子的核外电子有
(2)某研究组调控反应条件控制
 晶体形貌。
晶体形貌。①常温下,向银氨溶液逐滴加入
 溶液制得
溶液制得 晶体,完善该反应的离子方程式
晶体,完善该反应的离子方程式
②在不同pH条件下,向
 溶液中加入
溶液中加入 溶液制得磷酸银收率如图所示。样品A的晶粒较小,请从平衡移动与速率的角度解释原因
溶液制得磷酸银收率如图所示。样品A的晶粒较小,请从平衡移动与速率的角度解释原因
A.样品A中
 杂质含量最高
杂质含量最高B.可加入盐酸调控体系的pH制得不同样品
C.向
 溶液中加入少量
溶液中加入少量 溶液时,溶液中
溶液时,溶液中 减小
减小D.向
 溶液中加入
溶液中加入 溶液得到晶粒尺寸与上述样品相同
溶液得到晶粒尺寸与上述样品相同(3)研究组发现:
 溶液与0.2
溶液与0.2
 溶液等体积混合也能制得
溶液等体积混合也能制得 。
。①刚开始生成
 沉淀时,溶液中的
沉淀时,溶液中的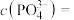
②常温下溶液中含磷物种的分布系数
 ,
, 或
或 与pH的关系如图所示,则磷酸的一级电离平衡常数
与pH的关系如图所示,则磷酸的一级电离平衡常数

 由
由 第一步电离决定,可表示为
第一步电离决定,可表示为 ,当生成
,当生成 沉淀时,溶液中
沉淀时,溶液中 至少为
至少为 (写出计算过程)。
(写出计算过程)。
您最近一年使用:0次
今日更新
|
353次组卷
|
2卷引用:广东省大湾区普通高中2024届高三下学期毕业年级联合模拟考试(二)化学试卷
4 . 常温下,在柠檬酸(记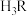 )和
)和 的混合液中滴加NaOH溶液,混合液中pX[
的混合液中滴加NaOH溶液,混合液中pX[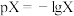 ,X代表
,X代表 、
、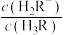 、
、 、
、 ]与pH的关系如图所示。下列叙述错误的是
]与pH的关系如图所示。下列叙述错误的是
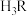 )和
)和 的混合液中滴加NaOH溶液,混合液中pX[
的混合液中滴加NaOH溶液,混合液中pX[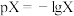 ,X代表
,X代表 、
、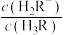 、
、 、
、 ]与pH的关系如图所示。下列叙述错误的是
]与pH的关系如图所示。下列叙述错误的是
A. 直线表 直线表 与pH关系 与pH关系 | B.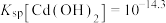 |
C.0.1 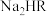 溶液呈碱性 溶液呈碱性 | D. 的K>1000 的K>1000 |
您最近一年使用:0次
5 . 实验室模拟某含有机酸 工业废水的处理过程。
工业废水的处理过程。
 .利用
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除
先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
,其机理如下:
(1) 和
和 发生络合反应生成有色物质:
发生络合反应生成有色物质:


①基态 的价电子排布式为
的价电子排布式为___________ 。
②下列有关上述络合反应的说法中,正确的有___________ (填标号)。
A.反应达平衡时,溶液的颜色不再变化
B.增大 浓度,逆反应速率减小
浓度,逆反应速率减小
C. 过低不利于
过低不利于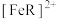 的生成
的生成
D.升高温度,该平衡正向移动
(2)紫外光催化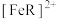 降解:
降解:
若有机酸为 ,则光催化降解反应的离子方程式为:
,则光催化降解反应的离子方程式为:___________ 。
 ___________
___________ ___________
___________ ___________
___________ ___________
___________
 .利用有机溶剂从废水中萃取
.利用有机溶剂从废水中萃取 的方法去除
的方法去除 。该过程涉及以下反应:
。该过程涉及以下反应:
(i)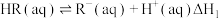
(ii)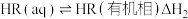
(iii)
(3)根据盖斯定律,反应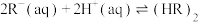 (有机相)的
(有机相)的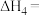
___________ 。
(4)水相的 以及体系温度
以及体系温度 对
对 的平衡分配比
的平衡分配比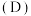 有影响。
有影响。
已知: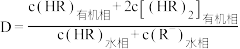 。
。
①常温下,配制体积相同、 不同、含
不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到
粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到 随
随 变化的曲线如图所示。分析
变化的曲线如图所示。分析 随
随 升高而降低的原因
升高而降低的原因___________ 。 溶液
溶液 时,
时,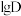 随
随 的变化曲线如图所示。
的变化曲线如图所示。 萃取宜在
萃取宜在___________ 温度下进行(填“较高”或“较低”)。
 经测定,在图中
经测定,在图中 点对应温度下,反应(ii)平衡常数
点对应温度下,反应(ii)平衡常数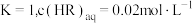 ,忽略水相中
,忽略水相中 的电离,则有机相中
的电离,则有机相中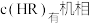
___________ 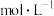 ;计算该温度下,反应(iii)的平衡常数
;计算该温度下,反应(iii)的平衡常数
___________ (写出计算过程)。
 工业废水的处理过程。
工业废水的处理过程。 .利用
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除
先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
,其机理如下:(1)
 和
和 发生络合反应生成有色物质:
发生络合反应生成有色物质:

①基态
 的价电子排布式为
的价电子排布式为②下列有关上述络合反应的说法中,正确的有
A.反应达平衡时,溶液的颜色不再变化
B.增大
 浓度,逆反应速率减小
浓度,逆反应速率减小C.
 过低不利于
过低不利于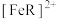 的生成
的生成 D.升高温度,该平衡正向移动
(2)紫外光催化
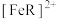 降解:
降解:若有机酸为
 ,则光催化降解反应的离子方程式为:
,则光催化降解反应的离子方程式为: ___________
___________ ___________
___________ ___________
___________ ___________
___________
 .利用有机溶剂从废水中萃取
.利用有机溶剂从废水中萃取 的方法去除
的方法去除 。该过程涉及以下反应:
。该过程涉及以下反应:(i)
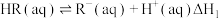
(ii)
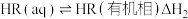
(iii)

(3)根据盖斯定律,反应
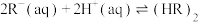 (有机相)的
(有机相)的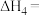
(4)水相的
 以及体系温度
以及体系温度 对
对 的平衡分配比
的平衡分配比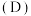 有影响。
有影响。已知:
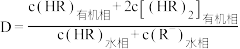 。
。①常温下,配制体积相同、
 不同、含
不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到
粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到 随
随 变化的曲线如图所示。分析
变化的曲线如图所示。分析 随
随 升高而降低的原因
升高而降低的原因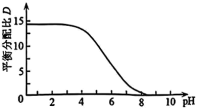
 溶液
溶液 时,
时,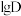 随
随 的变化曲线如图所示。
的变化曲线如图所示。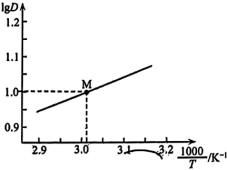
 萃取宜在
萃取宜在 经测定,在图中
经测定,在图中 点对应温度下,反应(ii)平衡常数
点对应温度下,反应(ii)平衡常数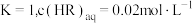 ,忽略水相中
,忽略水相中 的电离,则有机相中
的电离,则有机相中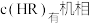
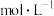 ;计算该温度下,反应(iii)的平衡常数
;计算该温度下,反应(iii)的平衡常数
您最近一年使用:0次
名校
6 .  盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
 盐酸与
盐酸与 碳酸钠溶液相互滴定,下图为反应过程中
碳酸钠溶液相互滴定,下图为反应过程中 、
、 、
、 微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是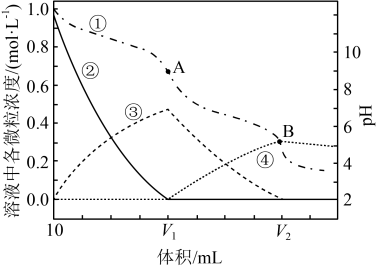
| A.上图是盐酸滴定碳酸钠溶液的曲线变化图 |
B.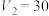 |
C.碳酸的电离平衡常数 数量级是 数量级是 |
D.已知草酸酸性大于碳酸,若用同浓度 溶液代替 溶液代替 溶液,其它实验条件不变,则A点下移 溶液,其它实验条件不变,则A点下移 |
您最近一年使用:0次
7 . 天然气(含 、
、 、
、 等)的脱硫和重整制氢综合利用,具有重要意义。
等)的脱硫和重整制氢综合利用,具有重要意义。
(1)用 干法脱硫涉及的反应如下:
干法脱硫涉及的反应如下:








反应 的
的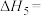
______ (写出一个代数式即可)。
(2)用NaOH溶液湿法脱硫时 和
和 同时被吸收。
同时被吸收。
①湿法脱硫后的吸收液中主要存在以下平衡:


下列说法正确的有______ 。
A.升高温度,溶液中 增大
增大
B.加少量水稀释,溶液中离子总数增加
C.通入少量HCl气体,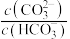 增大
增大
D.
②写出 和
和 溶液反应的化学方程式
溶液反应的化学方程式______ 。
( 的
的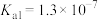 、
、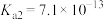 ,
, 的
的 、
、 )
)
(3) 和
和 的重整制氢涉及的反应如下:
的重整制氢涉及的反应如下:
a.
b.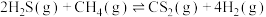
①设 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以 (
(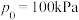 )。反应a的相对压力平衡常数表达式为
)。反应a的相对压力平衡常数表达式为
______ 。
②反应a、b的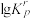 在400~1000℃范围内随T的变化如图1所示。反应a、b均为
在400~1000℃范围内随T的变化如图1所示。反应a、b均为______ 反应(填“吸热”或“放热”)。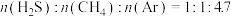 通入混合气体,测得平衡状态下H2、S2的收率和
通入混合气体,测得平衡状态下H2、S2的收率和 的转化率随温度的变化曲线如图2所示。
的转化率随温度的变化曲线如图2所示。 温度下
温度下 的收率,写出计算过程
的收率,写出计算过程______ 。
已知: 的收率=
的收率= ,
, 的收率=
的收率=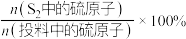
Ⅱ.从800℃升温到1000℃过程中,反应a平衡向______ 反应方向移动。
 、
、 、
、 等)的脱硫和重整制氢综合利用,具有重要意义。
等)的脱硫和重整制氢综合利用,具有重要意义。(1)用
 干法脱硫涉及的反应如下:
干法脱硫涉及的反应如下:







反应
 的
的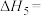
(2)用NaOH溶液湿法脱硫时
 和
和 同时被吸收。
同时被吸收。①湿法脱硫后的吸收液中主要存在以下平衡:


下列说法正确的有
A.升高温度,溶液中
 增大
增大B.加少量水稀释,溶液中离子总数增加
C.通入少量HCl气体,
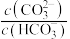 增大
增大D.

②写出
 和
和 溶液反应的化学方程式
溶液反应的化学方程式(
 的
的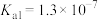 、
、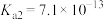 ,
, 的
的 、
、 )
)(3)
 和
和 的重整制氢涉及的反应如下:
的重整制氢涉及的反应如下:a.

b.
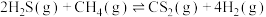
①设
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以 (
(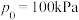 )。反应a的相对压力平衡常数表达式为
)。反应a的相对压力平衡常数表达式为
②反应a、b的
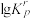 在400~1000℃范围内随T的变化如图1所示。反应a、b均为
在400~1000℃范围内随T的变化如图1所示。反应a、b均为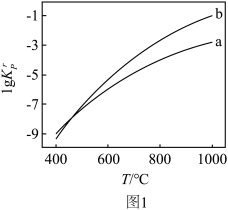
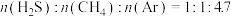 通入混合气体,测得平衡状态下H2、S2的收率和
通入混合气体,测得平衡状态下H2、S2的收率和 的转化率随温度的变化曲线如图2所示。
的转化率随温度的变化曲线如图2所示。
 温度下
温度下 的收率,写出计算过程
的收率,写出计算过程已知:
 的收率=
的收率= ,
, 的收率=
的收率=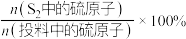
Ⅱ.从800℃升温到1000℃过程中,反应a平衡向
您最近一年使用:0次
名校
8 . 25℃时,用0.2mol·L-1的盐酸滴定20.00mL0.2mol·L-1一元弱碱MOH溶液,所得溶液的pH与滴加盐酸体积的关系如图1所示;不同pH时MOH溶液中不同形态的含M元素粒子的分布分数(δ)如图2所示(已知1g2=0.3,忽略溶液体积和温度变化)。下列叙述正确的是
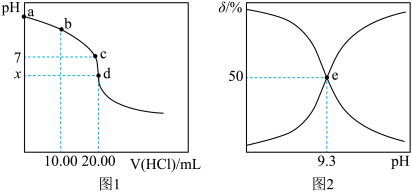
| A.b点溶液中由水电离出的c(H+)>10-7mol·L-1 |
B.d点溶液中存在离子浓度关系: |
C. |
| D.图2中的e点对应图1中的b点 |
您最近一年使用:0次
解题方法
9 .  用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。
 .配制溶液
.配制溶液
(1)配制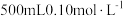 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为___________  。
。
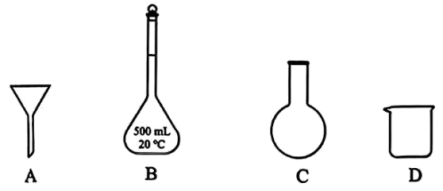
(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有___________ (填标号)。 .实验探究
.实验探究
探究温度对 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。
(3) 溶液显碱性的原因是
溶液显碱性的原因是___________ (用离子方程式表示)。
(4)实验1中测得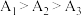 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中___________ 发挥主导作用。实验1中测得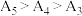 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。
(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料: 溶液中存在平衡:
溶液中存在平衡: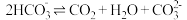 。
。
提出猜想:对于 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。
实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
实验结论:②根据实验1~3的结果,小组同学认为猜想成立,其判断依据是___________ 。
拓展总结:③ 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: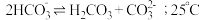 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为___________ [保留两位有效数字;已知: 时,
时,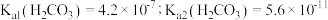 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。
(6)写出 在生产或生活中的一种应用
在生产或生活中的一种应用___________ 。
 用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。 .配制溶液
.配制溶液(1)配制
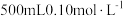 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为 。
。(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有
 .实验探究
.实验探究探究温度对
 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。| 实验序号 | 操作 | 测试温度 |  |
| 1 | 采用水浴加热,将 溶液从 溶液从 持续升温至 持续升温至 ,每隔 ,每隔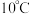 测量并记录溶液 测量并记录溶液 |  |  |
 |  | ||
 |  | ||
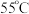 |  | ||
 | 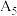 |
 溶液显碱性的原因是
溶液显碱性的原因是(4)实验1中测得
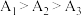 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中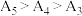 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料:
 溶液中存在平衡:
溶液中存在平衡: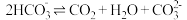 。
。提出猜想:对于
 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
| 实验序号 | 操作 | 测试温度 |  |
| 2 | 采用水浴加热,① ,并记录溶液 ,并记录溶液 |  |  |
| 3 | 采用水浴加热,将 溶液从 溶液从 升温至 升温至 ,然后冷却至 ,然后冷却至 ,并记录溶液 ,并记录溶液 |  |  |
拓展总结:③
 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: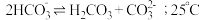 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为 时,
时,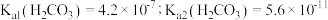 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。(6)写出
 在生产或生活中的一种应用
在生产或生活中的一种应用
您最近一年使用:0次
10 . 类比pH,对于稀溶液pc=-lgc,pKa=-lgKa.常温下,向某浓度H2A溶液中加入NaOH(s),保持溶液体积和温度不变,测得pH与pc(H2A)、pc(HA-)、pc(A2-)变化如图所示。下列说法正确的是
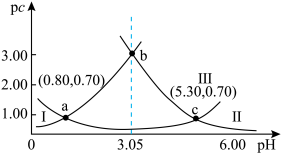
| A.pH=3.05时,c(HA-)>c(A2-)>c(H2A) |
| B.Ka1(H2A)的数量级为10-6 |
| C.c点时,c(Na+)=(10-8.70+3×10-0.7-10-5.30 ) mol·L-1 |
| D.若醋酸的pKa=4.76,则HA-与CH3COO-不能大量共存 |
您最近一年使用:0次



