安徽省滁州市2024届高三下学期第二次教学质量检测化学试卷
安徽
高三
二模
2024-05-10
260次
整体难度:
适中
考查范围:
有机化学基础、认识化学科学、物质结构与性质、化学实验基础、常见无机物及其应用、化学反应原理
安徽省滁州市2024届高三下学期第二次教学质量检测化学试卷
安徽
高三
二模
2024-05-10
260次
整体难度:
适中
考查范围:
有机化学基础、认识化学科学、物质结构与性质、化学实验基础、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
1. 中华瑰宝“笔”、“墨”、“纸”、“砚”,承载了几千年的文化传承,它们与化学密不可分。下列说法错误的是
| A.笔尖材料多为狼毫(毛),其主要成分为天然有机高分子材料 |
| B.墨的主要材料为煤烟或松烟,其主要成分为碳单质 |
| C.宣纸的材料主要成分是天然无机高分子材料 |
| D.砚台的主要材料砚石中多含有赤铁矿和褐铁矿,所以砚台多为深褐色或深紫色 |
【知识点】 淀粉和纤维素组成与结构 蛋白质
您最近一年使用:0次
单选题
|
适中(0.65)
2. 下列化学用语正确的是
A. 的球棍模型: 的球棍模型: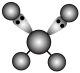 |
B.乙醛的结构简式: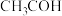 |
C. 的电子式: 的电子式: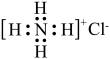 |
D.基态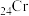 原子的价层电子轨道表示式: 原子的价层电子轨道表示式: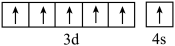 |
您最近一年使用:0次
3. 已知:
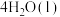
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是

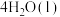
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是A.0.1  溶液中含有NA个K+ 溶液中含有NA个K+ |
B.1mol  参与反应断裂的π键数目为NA 参与反应断裂的π键数目为NA |
C.反应每放出m kJ的热量,生成NA个 分子 分子 |
| D.每转移10NA个电子,产生CO2的体积标况下约为44.8L |
您最近一年使用:0次
单选题
|
适中(0.65)
5. X、Y、Z、U、V、W是原子序数依次增大的短周期主族元素。X的一种核素原子核内没有中子,Y的最高价氧化物对应水化物为强酸,X与U、Z与W同主族,Z原子的最外层电子数是V原子最外层电子数的两倍。U与W形成的一种化合物其晶胞结构如下图所示,设晶胞边长为d pm。以下说法中不正确的是

| A.第一电离能∶Z>Y>U |
| B.简单氢化物热稳定性∶Z>Y |
| C.U、V、W的最高价氧化物对应水化物两两之间均能反应 |
D.该晶体的密度为 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 用下图装置进行实验,不能达到目的的是
|
|
| A.用盐酸滴定未知浓度的稀氨水 | B.制取NH4HCO3溶液 |
|
|
| C.实验室测定中和热 | D.用pH计测新制氯水的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 依托咪酯是常用的麻醉剂,其结构如下图所示。下列说法中不正确的是

| A.可水解但不能加成 | B.分子式为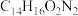 |
| C.分子中含一个手性碳原子 | D.碳原子杂化方式有两种 |
您最近一年使用:0次
单选题
|
适中(0.65)
8. 如图是石膏的部分层状结构,中间的虚线代表层与层的分界线。下列说法错误的是

A. 中心原子杂化方式为 中心原子杂化方式为 |
| B.该结构中既含有离子键又含有极性键 |
| C.加热石膏可以破坏层与层之间的氢键,只能发生物理变化 |
D.每个 连接在1个 连接在1个 和相邻两层各1个 和相邻两层各1个 的O上 的O上 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
9. 下列所述实验事实或所对应的离子方程式不正确的是
| 选项 | 实验事实 | 离子方程式 |
| A | 过量H2S通入FeCl3溶液中产生黑褐色沉淀 | 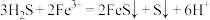 |
| B | 过量的NaOH与NH4AlFe(SO4)2反应未生成沉淀 | 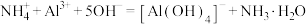 |
| C | 等物质的量NaHSO4与Ba(OH)2溶液反应产生白色沉淀 |  |
| D | 苯酚钠溶液中通入CO2,溶液变浑浊 |
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中(0.65)
10. 如图所示装置可由 制得异丙醇[
制得异丙醇[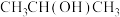 ]进而达成“双碳目标”。其中M、N均是惰性电极。下列说法错误的是
]进而达成“双碳目标”。其中M、N均是惰性电极。下列说法错误的是
 制得异丙醇[
制得异丙醇[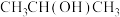 ]进而达成“双碳目标”。其中M、N均是惰性电极。下列说法错误的是
]进而达成“双碳目标”。其中M、N均是惰性电极。下列说法错误的是
| A.电子由N极流向M极 |
| B.该装置可将光能转化为电能 |
C.N极上 发生的电极反应为 发生的电极反应为 |
D.M极每产生60g异丙醇,N极生成标况下144g  |
【知识点】 原电池电极反应式书写解读 原电池有关计算解读
您最近一年使用:0次
单选题
|
适中(0.65)
11. 利用天然气制乙炔,反应原理如下:
①

②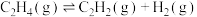

在1L恒容密闭反应器中充入适量的 ,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
①


②
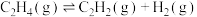

在1L恒容密闭反应器中充入适量的
 ,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
,发生上述反应,测得某温度时各含碳物质的物质的量随时间变化如图所示。下列叙述正确的是
| A.M点正反应速率小于逆反应速率 | B.反应前30min以乙烯生成为主 |
| C.若60min后升温,乙曲线上移,甲曲线下移 | D.0~40min内 平均速率为2. 平均速率为2.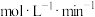 |
【知识点】 化学反应速率计算解读 化学平衡的移动及其影响因素
您最近一年使用:0次
单选题
|
适中(0.65)
12. 已知 催化反应
催化反应 历程如下图所示,催化历程中有
历程如下图所示,催化历程中有 参与。下列有关该反应的说法正确的是
参与。下列有关该反应的说法正确的是
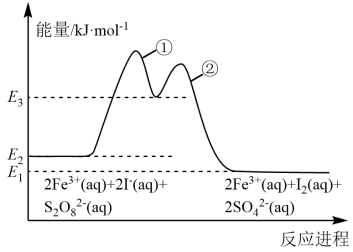
 催化反应
催化反应 历程如下图所示,催化历程中有
历程如下图所示,催化历程中有 参与。下列有关该反应的说法正确的是
参与。下列有关该反应的说法正确的是
| A.步骤①的速率常数大于步骤② |
| B.反应历程中存在非极性键的断裂和形成 |
| C.催化历程中,仅氧元素的化合价未发生变化 |
D.步骤②的热化学方程为:  |
您最近一年使用:0次
单选题
|
较难(0.4)
13. 某课题组为探究0.1 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:
实验一:
实验二: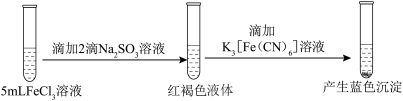
实验三: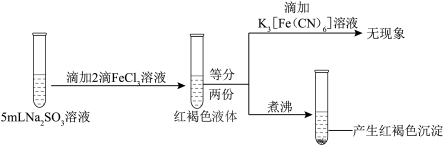
分析实验现象,下列说法中不合理的是
 的
的 与
与 溶液反应,进行了如下三个实验:
溶液反应,进行了如下三个实验:实验一:

实验二:

实验三:

分析实验现象,下列说法中不合理的是
| A.实验一的红褐色液体可产生丁达尔效应 |
B.实验二说明 既发生了水解反应也被 既发生了水解反应也被 还原 还原 |
C.实验三说明 发生了水解反应但未被还原 发生了水解反应但未被还原 |
D.以上三个实验说明 对 对 的水解无影响 的水解无影响 |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
14. 已知:①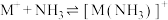

②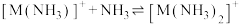

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是
{分布分数 }
}
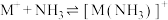

②
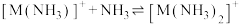

 、
、 、
、 的分布分数
的分布分数 与
与 关系如下图所示。下列说法正确的是
关系如下图所示。下列说法正确的是{分布分数
 }
}
A. |
B.曲线b代表 |
C.加水稀释,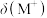 减小 减小 |
D.当 时, 时, 为含M粒子的主要存在形式 为含M粒子的主要存在形式 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
15. 焦亚硫酸钠( )可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题:
)可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题:___________ ,其作用为___________ 。
(2)圆底烧瓶中发生反应的化学方程式为___________ 。
(3)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
试剂:稀盐酸、稀 、稀
、稀 、
、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液
溶液
(4)某小组利用下列装置测定空气中 的含量。
的含量。___________ (填A或B)连接到导管末端。
②已知:该反应的化学方程式为: ,若空气流速为
,若空气流速为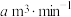 ,当观察到
,当观察到___________ 时,结束计时,测定耗时t min,假定样品中的 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是___________ 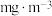 。
。
 )可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题:
)可用作食品添加剂,其实验室制备的装置如下图所示。回答下列问题: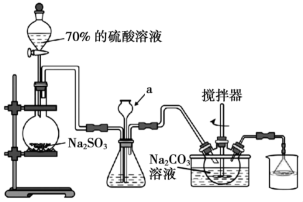
(2)圆底烧瓶中发生反应的化学方程式为
(3)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
试剂:稀盐酸、稀
 、稀
、稀 、
、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液
溶液| 实验编号 | 实验步骤 | 现象 | 结论 |
| Ⅰ | 取少量样品,加入除氧蒸馏水,溶解完后平均分装到两支相同的小试管中 | 固体完全溶解得到无色溶液 | / |
| Ⅱ | 取实验I的溶液, | 出现白色沉淀 | 样品已氧化变质 |
| Ⅲ | 另取实验Ⅰ的溶液,加入酸性 溶液,充分振荡 溶液,充分振荡 | 溶液褪色 | 样品未完全氧化变质 |
 的含量。
的含量。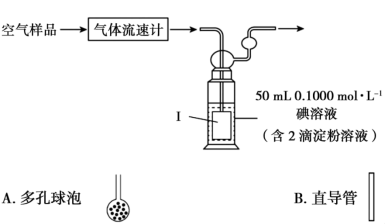
②已知:该反应的化学方程式为:
 ,若空气流速为
,若空气流速为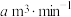 ,当观察到
,当观察到 可被溶液充分吸收,该空气样品中
可被溶液充分吸收,该空气样品中 的含量是
的含量是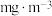 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
16. 我国是铜业大国,氨法浸取工艺是铜矿提炼中常用方法,可实现废弃物“铜包钢”的有效分离,同时生产的CuCl可用于催化、医药、冶金等多种领域。工艺流程如下:
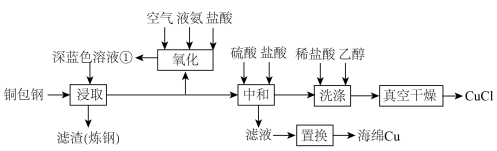
回答下列问题:
(1)首次浸取时所用深蓝色溶液①由细铜丝、足量液氨、空气和盐酸反应得到,其主要成分为___________ (填化学式),其配体的空间构型为___________ 。
(2)浸取工序的产物为 ,该工序发生反应的离子方程式为
,该工序发生反应的离子方程式为___________ 。
(3)浸取工序不宜超过40℃,其原因是___________ 。
(4)中和工序中主反应的离子方程式
___________ 。
(5)洗涤步骤中使用乙醇的优点有___________ 。
(6)选用真空干燥的原因___________ 。

回答下列问题:
(1)首次浸取时所用深蓝色溶液①由细铜丝、足量液氨、空气和盐酸反应得到,其主要成分为
(2)浸取工序的产物为
 ,该工序发生反应的离子方程式为
,该工序发生反应的离子方程式为(3)浸取工序不宜超过40℃,其原因是
(4)中和工序中主反应的离子方程式

(5)洗涤步骤中使用乙醇的优点有
(6)选用真空干燥的原因
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
17. 工业上以乙苯为原料制备苯乙烯。主要有以下两种制备方法,T K时相应的热化学方程式及其平衡常数如下:
反应Ⅰ:直接脱氢
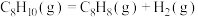
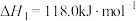 ,
,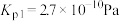
反应Ⅱ:氧化脱氢
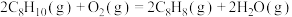
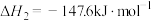 ,
,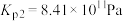
回答下列问题:
(1)①反应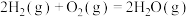 的平衡常数
的平衡常数
___________ (保留3位有效数字)。
②反应Ⅱ趋势远大于反应Ⅰ,从反应自发性角度分析其原因是___________ 。
(2)已知 ,忽略
,忽略 、
、 随温度的变化。当
随温度的变化。当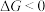 时,反应能自发进行。在100kPa下,直接脱氢反应的
时,反应能自发进行。在100kPa下,直接脱氢反应的 和
和 随温度变化的理论计算结果如图所示。
随温度变化的理论计算结果如图所示。 随温度的变化曲线为
随温度的变化曲线为___________ (选填“a”或“b”),判断的理由是___________ 。
②在某温度下,向恒容密闭容器中通入气态乙苯和氧气各1mol,初始压强为200kPa,只发生反应Ⅱ,达到平衡时,乙苯的转化率为99.8%,该反应的平衡常数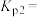
___________ kPa(保留小数点后一位;分压=总压×物质的量分数)。
(3)乙苯脱氢法制苯乙烯往往伴随副反应,一定条件下,为了提高反应速率和苯乙烯选择
性,应当___________ 。
反应Ⅰ:直接脱氢
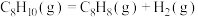
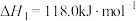 ,
,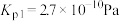
反应Ⅱ:氧化脱氢
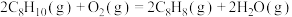
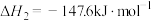 ,
,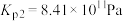
回答下列问题:
(1)①反应
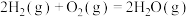 的平衡常数
的平衡常数
②反应Ⅱ趋势远大于反应Ⅰ,从反应自发性角度分析其原因是
(2)已知
 ,忽略
,忽略 、
、 随温度的变化。当
随温度的变化。当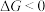 时,反应能自发进行。在100kPa下,直接脱氢反应的
时,反应能自发进行。在100kPa下,直接脱氢反应的 和
和 随温度变化的理论计算结果如图所示。
随温度变化的理论计算结果如图所示。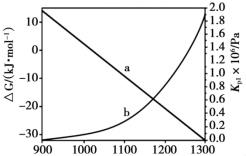
 随温度的变化曲线为
随温度的变化曲线为②在某温度下,向恒容密闭容器中通入气态乙苯和氧气各1mol,初始压强为200kPa,只发生反应Ⅱ,达到平衡时,乙苯的转化率为99.8%,该反应的平衡常数
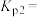
(3)乙苯脱氢法制苯乙烯往往伴随副反应,一定条件下,为了提高反应速率和苯乙烯选择
性,应当
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
18. 化合物K是一种化疗药物的活性成分,一种以甲苯为原料的合成路线如图所示:
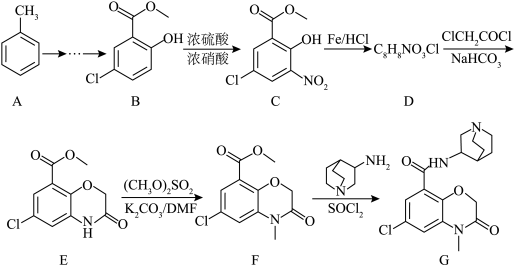
(1)A的化学名称是___________ ,B中非含氧官能团的名称为___________ 。
(2)E→F的反应类型是___________ 。
(3)B→C中酚羟基不被浓硝酸氧化,其主要原因是___________ 。
(4)E在加热条件下与足量NaOH溶液反应,生成的芳香族化合物结构简式为___________ 。
(5)X是芳香族化合物,比D分子少一个O原子,写出满足下列条件的X的结构简式___________ 。(写出任意一种即可)
a.苯环上有2个取代基
b.能与 溶液发生显色反应
溶液发生显色反应
c.与NaOH溶液共热有 生成
生成
(6)氨基具有较强的还原性。参照上述合成路线,以 和甲醇为原料,设计路线三步合成
和甲醇为原料,设计路线三步合成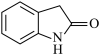
___________ 。(无机试剂任选)

(1)A的化学名称是
(2)E→F的反应类型是
(3)B→C中酚羟基不被浓硝酸氧化,其主要原因是
(4)E在加热条件下与足量NaOH溶液反应,生成的芳香族化合物结构简式为
(5)X是芳香族化合物,比D分子少一个O原子,写出满足下列条件的X的结构简式
a.苯环上有2个取代基
b.能与
 溶液发生显色反应
溶液发生显色反应c.与NaOH溶液共热有
 生成
生成(6)氨基具有较强的还原性。参照上述合成路线,以
 和甲醇为原料,设计路线三步合成
和甲醇为原料,设计路线三步合成
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:有机化学基础、认识化学科学、物质结构与性质、化学实验基础、常见无机物及其应用、化学反应原理
试卷题型(共 18题)
题型
数量
单选题
14
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 淀粉和纤维素组成与结构 蛋白质 | |
| 2 | 0.65 | 化学用语综合判断 轨道表示式 基态原子的电子排布的特殊性 利用杂化轨道理论判断分子的空间构型 | |
| 3 | 0.65 | 阿伏加德罗常数的应用 物质结构基础与NA相关推算 共价键的形成及主要类型 电子转移计算 | |
| 4 | 0.85 | 苯酚的弱酸性 物质的分离、提纯 化学实验基础操作 | |
| 5 | 0.65 | 元素非金属性强弱的比较方法 根据原子结构进行元素种类推断 晶胞的有关计算 | |
| 6 | 0.65 | 次氯酸及其性质 氨的碱性 中和热的测定与误差分析 酸碱中和滴定实验相关仪器 | |
| 7 | 0.65 | 分子的手性 多官能团有机物的结构与性质 利用杂化轨道理论判断化学键杂化类型 | |
| 8 | 0.65 | 化学键与物质类别关系的判断 共价键的形成及主要类型 利用杂化轨道理论判断化学键杂化类型 含有氢键的物质 | |
| 9 | 0.65 | 离子方程式的正误判断 铝盐与强碱溶液反应 Fe3+与其他物质氧化性强弱关系 苯酚的弱酸性 | |
| 10 | 0.65 | 原电池电极反应式书写 原电池有关计算 | |
| 11 | 0.65 | 化学反应速率计算 化学平衡的移动及其影响因素 | |
| 12 | 0.65 | 化学键与化学反应中的能量关系 活化能及其对反应速率的影响 催化剂对化学反应速率的影响 | |
| 13 | 0.4 | 胶体的性质和应用 铁盐 物质性质的探究 物质性质实验方案的设计 | |
| 14 | 0.4 | 弱电解质在水溶液中的电离平衡 浓度对电离平衡的影响 弱电解质的电离平衡常数 | |
| 二、解答题 | |||
| 15 | 0.65 | 硫酸根离子的检验 常用仪器及使用 探究物质组成或测量物质的含量 | 实验探究题 |
| 16 | 0.4 | 离子方程式的书写 简单配合物的成键 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 17 | 0.4 | 催化剂对化学反应速率的影响 化学平衡的移动及其影响因素 化学平衡常数的有关计算 转化率的相关计算及判断 | 原理综合题 |
| 18 | 0.4 | 根据要求书写同分异构体 有机物的推断 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |


 中的
中的







