天然气(含 、
、 、
、 等)的脱硫和重整制氢综合利用,具有重要意义。
等)的脱硫和重整制氢综合利用,具有重要意义。
(1)用 干法脱硫涉及的反应如下:
干法脱硫涉及的反应如下:








反应 的
的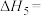
______ (写出一个代数式即可)。
(2)用NaOH溶液湿法脱硫时 和
和 同时被吸收。
同时被吸收。
①湿法脱硫后的吸收液中主要存在以下平衡:


下列说法正确的有______ 。
A.升高温度,溶液中 增大
增大
B.加少量水稀释,溶液中离子总数增加
C.通入少量HCl气体,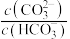 增大
增大
D.
②写出 和
和 溶液反应的化学方程式
溶液反应的化学方程式______ 。
( 的
的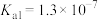 、
、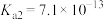 ,
, 的
的 、
、 )
)
(3) 和
和 的重整制氢涉及的反应如下:
的重整制氢涉及的反应如下:
a.
b.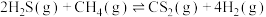
①设 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以 (
(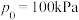 )。反应a的相对压力平衡常数表达式为
)。反应a的相对压力平衡常数表达式为
______ 。
②反应a、b的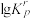 在400~1000℃范围内随T的变化如图1所示。反应a、b均为
在400~1000℃范围内随T的变化如图1所示。反应a、b均为______ 反应(填“吸热”或“放热”)。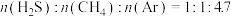 通入混合气体,测得平衡状态下H2、S2的收率和
通入混合气体,测得平衡状态下H2、S2的收率和 的转化率随温度的变化曲线如图2所示。
的转化率随温度的变化曲线如图2所示。 温度下
温度下 的收率,写出计算过程
的收率,写出计算过程______ 。
已知: 的收率=
的收率= ,
, 的收率=
的收率=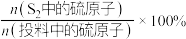
Ⅱ.从800℃升温到1000℃过程中,反应a平衡向______ 反应方向移动。
 、
、 、
、 等)的脱硫和重整制氢综合利用,具有重要意义。
等)的脱硫和重整制氢综合利用,具有重要意义。(1)用
 干法脱硫涉及的反应如下:
干法脱硫涉及的反应如下:







反应
 的
的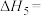
(2)用NaOH溶液湿法脱硫时
 和
和 同时被吸收。
同时被吸收。①湿法脱硫后的吸收液中主要存在以下平衡:


下列说法正确的有
A.升高温度,溶液中
 增大
增大B.加少量水稀释,溶液中离子总数增加
C.通入少量HCl气体,
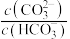 增大
增大D.

②写出
 和
和 溶液反应的化学方程式
溶液反应的化学方程式(
 的
的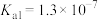 、
、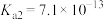 ,
, 的
的 、
、 )
)(3)
 和
和 的重整制氢涉及的反应如下:
的重整制氢涉及的反应如下:a.

b.
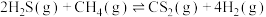
①设
 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以
为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压(单位为kPa)除以 (
(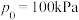 )。反应a的相对压力平衡常数表达式为
)。反应a的相对压力平衡常数表达式为
②反应a、b的
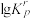 在400~1000℃范围内随T的变化如图1所示。反应a、b均为
在400~1000℃范围内随T的变化如图1所示。反应a、b均为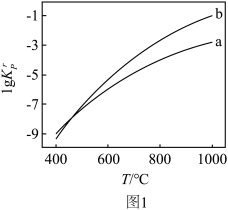
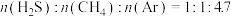 通入混合气体,测得平衡状态下H2、S2的收率和
通入混合气体,测得平衡状态下H2、S2的收率和 的转化率随温度的变化曲线如图2所示。
的转化率随温度的变化曲线如图2所示。
 温度下
温度下 的收率,写出计算过程
的收率,写出计算过程已知:
 的收率=
的收率= ,
, 的收率=
的收率=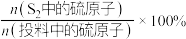
Ⅱ.从800℃升温到1000℃过程中,反应a平衡向
2024·广东广州·二模 查看更多[1]
更新时间:2024-05-18 19:33:42
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】氮氧化物污染指数是衡量空气质量的重要标准,氮氧化物的治理刻不容缓。回答下列问题:
(1)已知:①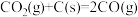 ΔH1
ΔH1
②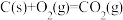 ΔH2
ΔH2
③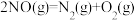 ΔH3
ΔH3
则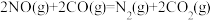 的ΔH=
的ΔH=___________ 。
(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
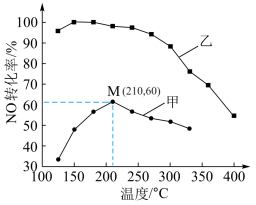
①工业上选择催化剂___________ (填“甲”或“乙”)。
②在催化剂甲作用下,图中M点NO的转化率___________ (填“是”或“不是”)该温度下的平衡转化率。高于210℃时,NO转化率降低的原因可能是___________ 。
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO ,其工作原理如下图所示。
,其工作原理如下图所示。
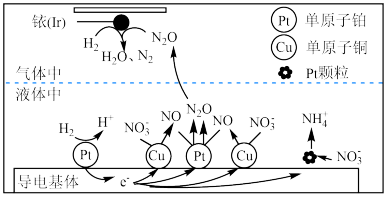
①导电基体Pt颗粒 上NO
上NO 发生的电极反应式为
发生的电极反应式为___________ 。
②在单原子铜、铂催化作用下,H2转化NO 为N2的过程可描述为
为N2的过程可描述为___________ 。
(1)已知:①
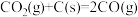 ΔH1
ΔH1②
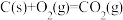 ΔH2
ΔH2③
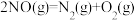 ΔH3
ΔH3则
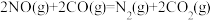 的ΔH=
的ΔH=(2)SCR(选择性催化还原)脱硝法是工业上消除氮氧化物的常用方法,反应原理为
 ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
ΔH<0。其他条件相同,在甲、乙两种催化剂作用下,经过相同时间,NO转化率与温度的关系如下图。
①工业上选择催化剂
②在催化剂甲作用下,图中M点NO的转化率
(3)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的NO
 ,其工作原理如下图所示。
,其工作原理如下图所示。
①导电基体Pt颗粒
 上NO
上NO 发生的电极反应式为
发生的电极反应式为②在单原子铜、铂催化作用下,H2转化NO
 为N2的过程可描述为
为N2的过程可描述为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与储存,过程如下:
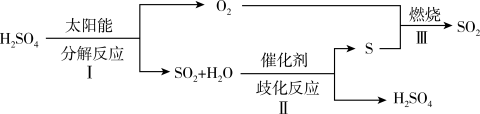
(1)反应I由两步反应完成:a. H2SO4(l) SO3(g)+H2O(g) △H1 = +177 kJ/mol
SO3(g)+H2O(g) △H1 = +177 kJ/mol
b. 2SO3(g) 2SO2(g) +O2(g) △H2 = +197 kJ/mol
2SO2(g) +O2(g) △H2 = +197 kJ/mol
①请写出反应I的热化学反应方程式:_________________________________ 。
②硫酸工业中可通过反应b的逆反应合成SO3,下表列出了不同温度、压强下SO2的平衡转化率:
在实际生产中,选定温度为400~500 ℃的原因是_________________ ;选定压强为常压的原因是_____________________ 。
(2) 可以作为水溶液中SO2歧化反应(反应II)的催化剂,催化历程如下:
可以作为水溶液中SO2歧化反应(反应II)的催化剂,催化历程如下:
i.SO2+4I-+4H+= S↓+2I2+2H2O ii.
某实验小组为探究i、ii反应速率与SO2歧化反应速率的关系,进行如下实验:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
①请补全反应ii:___________________________________ 。
②比较A、B、C,可得出的结论是:______________________ 。
③D是A的对比实验,则a=__________ 。
④实验表明,SO2的歧化反应速率D>A,则反应速率:i____ ii(填“>”、“=”或“<”)。

(1)反应I由两步反应完成:a. H2SO4(l)
 SO3(g)+H2O(g) △H1 = +177 kJ/mol
SO3(g)+H2O(g) △H1 = +177 kJ/molb. 2SO3(g)
 2SO2(g) +O2(g) △H2 = +197 kJ/mol
2SO2(g) +O2(g) △H2 = +197 kJ/mol①请写出反应I的热化学反应方程式:
②硫酸工业中可通过反应b的逆反应合成SO3,下表列出了不同温度、压强下SO2的平衡转化率:
温度/℃ | SO2的平衡转化率/% | ||||
0.1 MPa | 0.5 MPa | 1 MPa | 5 MPa | 10 MPa | |
450 | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
550 | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
在实际生产中,选定温度为400~500 ℃的原因是
(2)
 可以作为水溶液中SO2歧化反应(反应II)的催化剂,催化历程如下:
可以作为水溶液中SO2歧化反应(反应II)的催化剂,催化历程如下:i.SO2+4I-+4H+= S↓+2I2+2H2O ii.
某实验小组为探究i、ii反应速率与SO2歧化反应速率的关系,进行如下实验:分别将18 mL SO2饱和溶液加入到2 mL下列试剂中,密闭放置观察现象。(已知:I2易溶解在KI溶液中)
A | B | C | D | |
试剂组成 | 0.4 mol/L KI | 0.4 mol/L KI 0.2 mol/L H2SO4 | 0.2 mol/L H2SO4 | 0.2 mol/L KI a mol I2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 | 溶液由棕褐色很快褪色成黄色,出现浑浊较A快 |
①请补全反应ii:
②比较A、B、C,可得出的结论是:
③D是A的对比实验,则a=
④实验表明,SO2的歧化反应速率D>A,则反应速率:i
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】根据所学内容,回答下列问题:
(1)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
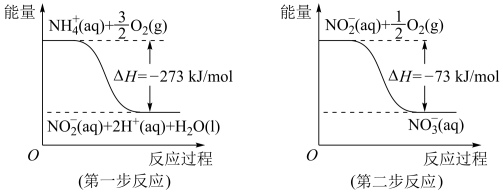
①第一步反应是___________ (填“放热”或“吸热”)反应,判断依据是___________ 。
②1mol (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是___________ 。
(2)白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
①已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1
P(s,红磷)+ O2(g)=
O2(g)= P4O10(s) ΔH2=-738.5kJ·mol-1
P4O10(s) ΔH2=-738.5kJ·mol-1
则该温度下白磷转化为红磷的热化学方程式为______ 。相同状况下,能量较低的是________ (填“红磷”或“白磷”),白磷的稳定性比红磷___________ (填“高”或“低”)。
②已知298K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)=P4O6(s) ΔH=-1638kJ·mol-1.在某密闭容器中加入12.4g白磷和8.96L氧气(标准状况下),控制条件使之恰好完全反应。则所得到的P4O10和P4O6的物质的量之比为___________ ,反应过程中放出的热量为___________ 。
(3)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=___________ 。
(1)在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
②1mol
 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是(2)白磷、红磷是磷的两种同素异形体,在空气中燃烧得到磷的氧化物,空气不足时生成P4O6,空气充足时生成P4O10。
①已知298K时白磷、红磷完全燃烧的热化学方程式分别为:
P4(s,白磷)+5O2(g)=P4O10(s) ΔH1=-2983.2kJ·mol-1
P(s,红磷)+
 O2(g)=
O2(g)= P4O10(s) ΔH2=-738.5kJ·mol-1
P4O10(s) ΔH2=-738.5kJ·mol-1则该温度下白磷转化为红磷的热化学方程式为
②已知298K时白磷不完全燃烧的热化学方程式为P4(s,白磷)+3O2(g)=P4O6(s) ΔH=-1638kJ·mol-1.在某密闭容器中加入12.4g白磷和8.96L氧气(标准状况下),控制条件使之恰好完全反应。则所得到的P4O10和P4O6的物质的量之比为
(3)已知H2(g)+Br2(l)=2HBr(g) ΔH=-72kJ·mol-1,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 200 | a |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】太阳能甲烷—水蒸气重整制氢技术因具有原料储量丰富、成本低、产量高等特点而被广泛采用。制氢的反应为 。
。
(1)已知:几种化学键的键能(键能为 气态分子离解成气态原子所吸收的能量或气态原子形成
气态分子离解成气态原子所吸收的能量或气态原子形成 气态分子所释放的能量)如下表。
气态分子所释放的能量)如下表。
反应: 的
的
______  。
。
(2)加压使 平衡转化率降低,但工业生产中仍采用较高的压强,原因可能是
平衡转化率降低,但工业生产中仍采用较高的压强,原因可能是____________ (填一条即可,下同),为弥补加压带来的不利因素,可采取的措施为______ 。
(3) 下,向
下,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和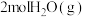 ,发生上述反应,
,发生上述反应, 达平衡,
达平衡, 的平衡转化率为
的平衡转化率为 。
。
① 内,
内,
______  。
。
②
______ 。
③平衡后保持温度和容积不变,若再向容器中充入 和
和 ,此时
,此时
______ (选填“>”、“<”或“=”)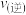 。
。
 。
。(1)已知:几种化学键的键能(键能为
 气态分子离解成气态原子所吸收的能量或气态原子形成
气态分子离解成气态原子所吸收的能量或气态原子形成 气态分子所释放的能量)如下表。
气态分子所释放的能量)如下表。化学键 |
|
|
|
|
键能 | 413 | 463 | 436 | 1071 |
 的
的
 。
。(2)加压使
 平衡转化率降低,但工业生产中仍采用较高的压强,原因可能是
平衡转化率降低,但工业生产中仍采用较高的压强,原因可能是(3)
 下,向
下,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和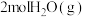 ,发生上述反应,
,发生上述反应, 达平衡,
达平衡, 的平衡转化率为
的平衡转化率为 。
。①
 内,
内,
 。
。②

③平衡后保持温度和容积不变,若再向容器中充入
 和
和 ,此时
,此时
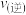 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】CO2-CH4干气重整反应制合成气(H2、CO)是CO2资源化利用的重要研究方向。其反应主要包括:
反应I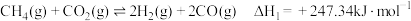
反应Ⅱ
(1)已知 H2(g)、CO(g)的燃烧热分别为285.8 kJ∙mol-1和283kJ∙mol-1,水的汽化热为44kJ∙mol-1,则△H2=_______ kJ∙mol-1;能同时提高CH4(g)的平衡转化率和反应速率的措施为_______ (写一条即可)。
(2)向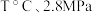 的恒压密闭容器中,充入1molCH4(g)和1mol CO2 (g)发生反应I和Ⅱ.达到平衡时,CO2的转化率为80%,
的恒压密闭容器中,充入1molCH4(g)和1mol CO2 (g)发生反应I和Ⅱ.达到平衡时,CO2的转化率为80%,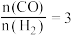 ,则平衡时气体的总物质的量
,则平衡时气体的总物质的量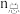 =
=_______ mol;反应Ⅰ的压强平衡常数Kp=_______ (MPa)2;若反应在刚性容器中达到平衡,则CO2(g)的转化率_______ (填“>”“=”或“<”)80%。
(3)实验研究发现,在(2)条件下,催化剂表面产生积碳与下列2个反应有关:
反应Ⅲ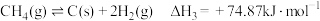
反应IV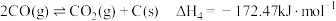
①已知ΔG=△H-TΔS,ΔG的值只取决于反应体系的始态和终态,忽略△H、ΔS随温度的变化,反应Ⅲ和反应IV的ΔG与T的关系如图1所示,其中表示反应Ⅲ的曲线为_______ (填“a”或“b”);在200~400℃时,催化剂表面产生的积碳主要来自于反应_______ (填“Ⅲ”或“IV”)。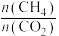 对催化剂表面积碳生成量的影响如图2、3所示。
对催化剂表面积碳生成量的影响如图2、3所示。_______ (填选项字母)。
A.压强一定时,增大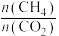 且升高温度
且升高温度
B.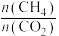 一定时,升高温度且减小压强
一定时,升高温度且减小压强
C.温度一定时,增大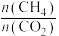 且增大压强
且增大压强
D.温度一定时,降低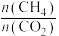 且减小压强
且减小压强
反应I
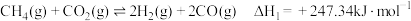
反应Ⅱ

(1)已知 H2(g)、CO(g)的燃烧热分别为285.8 kJ∙mol-1和283kJ∙mol-1,水的汽化热为44kJ∙mol-1,则△H2=
(2)向
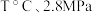 的恒压密闭容器中,充入1molCH4(g)和1mol CO2 (g)发生反应I和Ⅱ.达到平衡时,CO2的转化率为80%,
的恒压密闭容器中,充入1molCH4(g)和1mol CO2 (g)发生反应I和Ⅱ.达到平衡时,CO2的转化率为80%,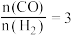 ,则平衡时气体的总物质的量
,则平衡时气体的总物质的量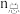 =
=(3)实验研究发现,在(2)条件下,催化剂表面产生积碳与下列2个反应有关:
反应Ⅲ
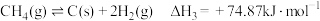
反应IV
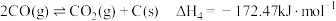
①已知ΔG=△H-TΔS,ΔG的值只取决于反应体系的始态和终态,忽略△H、ΔS随温度的变化,反应Ⅲ和反应IV的ΔG与T的关系如图1所示,其中表示反应Ⅲ的曲线为
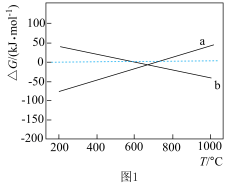
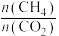 对催化剂表面积碳生成量的影响如图2、3所示。
对催化剂表面积碳生成量的影响如图2、3所示。
A.压强一定时,增大
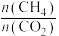 且升高温度
且升高温度B.
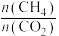 一定时,升高温度且减小压强
一定时,升高温度且减小压强C.温度一定时,增大
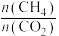 且增大压强
且增大压强D.温度一定时,降低
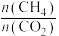 且减小压强
且减小压强
您最近一年使用:0次
【推荐3】合成氨在生产中具有重要意义。请按要求回答下列问题。
(1)已知反应N2(g)+3H2(g) 2NH3(g) △H<0。向恒温恒容密闭的反应容器中投料1 mol N2、3 mol H2,在不同温度下分别达平衡时,混合气中NH3的物质的量分数随压强变化的曲线如图所示:
2NH3(g) △H<0。向恒温恒容密闭的反应容器中投料1 mol N2、3 mol H2,在不同温度下分别达平衡时,混合气中NH3的物质的量分数随压强变化的曲线如图所示:

①曲线A、B、C对应的温度是由低到高依次是(填代表曲线的字母)_______ 。图中X、Y、Z点的平衡常数大小关系(填“>”“<”或“=”): K(X)__ K(Y)_____ K(Z).
②既能加快化学反应速率有能提高H2的转化率的措施有_______ 。
③Y点对应的H2的转化率是_______ ;若仅将起始投料均加倍,其他条件不变,达新平衡时,则H2的转化率将会(填“升高”、“降低”或“不变”) _______ 。
(2)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图甲和图乙所示:
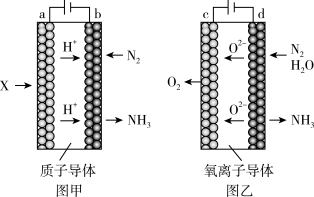
①图甲a电极上的电极反应式为_______ 图乙d电极上的电极反应式为_______ 。
②若图甲和图乙装置的通电时间相同、电流强度相等,电解效率分别为80%和60%,则两种装置中产生氨气的物质的量之比为_______ 。
(1)已知反应N2(g)+3H2(g)
 2NH3(g) △H<0。向恒温恒容密闭的反应容器中投料1 mol N2、3 mol H2,在不同温度下分别达平衡时,混合气中NH3的物质的量分数随压强变化的曲线如图所示:
2NH3(g) △H<0。向恒温恒容密闭的反应容器中投料1 mol N2、3 mol H2,在不同温度下分别达平衡时,混合气中NH3的物质的量分数随压强变化的曲线如图所示:
①曲线A、B、C对应的温度是由低到高依次是(填代表曲线的字母)
②既能加快化学反应速率有能提高H2的转化率的措施有
③Y点对应的H2的转化率是
(2)电解法合成氨因其原料转化率大幅度提高,有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图甲和图乙所示:

①图甲a电极上的电极反应式为
②若图甲和图乙装置的通电时间相同、电流强度相等,电解效率分别为80%和60%,则两种装置中产生氨气的物质的量之比为
您最近一年使用:0次
【推荐1】工业上利用正丁烷(CH3CH2CH2CH3)的裂解反应制备乙烯、丙烯等化工基础原料,相关反应有:
ⅰ. △H1=+80 kJ/mol
△H1=+80 kJ/mol
ⅱ. △H2=+92 kJ/mol
△H2=+92 kJ/mol
请回答下列问题:
(1)反应ⅰ在___________ 下能自发进行(填字母)。
a.高温 b.低温 c.任意温度
(2)已知 △H3=-9 kJ/mol,相对而言,
△H3=-9 kJ/mol,相对而言,___________ 较稳定(填“正丁烷”或“异丁烷”);若异丁烷发生反应ⅰ,则其反应热△H ___________ 80 kJ/mol(填“>”或“<”)。
(3)将一定量的正丁烷通入某恒容密闭容器中,发生上述反应ⅰ和反应ⅱ,测得正丁烷的平衡转化率(a)与压强(p)、温度(T)的关系如图所示。

①下列情况能说明上述反应达到平衡状态的是___________ (填字母)。
A.△H1、△H2保持不变
B.CH4与CH3CH3的物质的量之比保持不变
C.混合气体的平均摩尔质量保持不变
D.
②c点正丁烷的平衡转化率大于b点的原因为___________ 。
③对反应ⅰ而言,图中a、b、c三点的化学平衡常数K(a)、K(b)、K(c)从大到小的顺序为___________ 。
④若p1为18m kPa,a点丙烯的选择性为80%[丙烯的选择性= ],则该温度下反应ⅰ的平衡常数K=
],则该温度下反应ⅰ的平衡常数K=___________ kPa(用含m的代数式表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)从反应混合物中分离出的CH4可用于燃料电池。某CH4-空气燃料电池的工作原理如图所示:

电极R上的电极反应式为___________ ;理论上电极P上消耗的CH4与生成的CO2的物质的量之比为___________ 。
ⅰ.
 △H1=+80 kJ/mol
△H1=+80 kJ/molⅱ.
 △H2=+92 kJ/mol
△H2=+92 kJ/mol 请回答下列问题:
(1)反应ⅰ在
a.高温 b.低温 c.任意温度
(2)已知
 △H3=-9 kJ/mol,相对而言,
△H3=-9 kJ/mol,相对而言,(3)将一定量的正丁烷通入某恒容密闭容器中,发生上述反应ⅰ和反应ⅱ,测得正丁烷的平衡转化率(a)与压强(p)、温度(T)的关系如图所示。

①下列情况能说明上述反应达到平衡状态的是
A.△H1、△H2保持不变
B.CH4与CH3CH3的物质的量之比保持不变
C.混合气体的平均摩尔质量保持不变
D.

②c点正丁烷的平衡转化率大于b点的原因为
③对反应ⅰ而言,图中a、b、c三点的化学平衡常数K(a)、K(b)、K(c)从大到小的顺序为
④若p1为18m kPa,a点丙烯的选择性为80%[丙烯的选择性=
 ],则该温度下反应ⅰ的平衡常数K=
],则该温度下反应ⅰ的平衡常数K=(4)从反应混合物中分离出的CH4可用于燃料电池。某CH4-空气燃料电池的工作原理如图所示:

电极R上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.实验室用如图所示简易量热计进行中和热的测定实验,请回答。
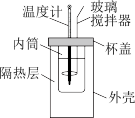
(1)简易量热计有利于减小误差的设计措施有_____ 、_____ 。
(2)分别取50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液进行反应,经测定并计算得出该反应放出的热量为QkJ。写出其热化学方程式_____ 。
Ⅱ.在I-存在下,H2O2分解的反应历程为:
①
②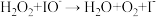
其反应过程的能量变化如图所示,回答下列问题:
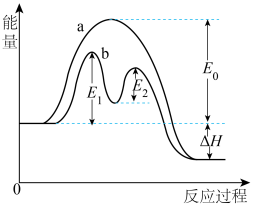
(3)在I-存在下,H2O2分解过程的最大能垒(活化能)为_____ ,决定总反应速率的是第_____ 步基元反应,
(4)反应过程中I-和IO-的浓度变化趋势为_____。
Ⅲ.向1L容器中加入1molSO2和足量焦炭,发生反应2C(s)+2SO2(g) S2(g)+2CO2(g)。测得反应速率v正(S2)和v逆(SO2)随温度变化如图所示,请回答:
S2(g)+2CO2(g)。测得反应速率v正(S2)和v逆(SO2)随温度变化如图所示,请回答:
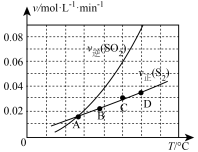
(5)A、B、C、D四点对应的状态中,达到平衡状态的有_____ (填字母)。
(6)该反应的△H_____ 0(填>、<或=)。
(7)下列措施能够增大SO2平衡转化率的是_____。

(1)简易量热计有利于减小误差的设计措施有
(2)分别取50mL0.50mol/L盐酸和50mL0.55mol/LNaOH溶液进行反应,经测定并计算得出该反应放出的热量为QkJ。写出其热化学方程式
Ⅱ.在I-存在下,H2O2分解的反应历程为:
①

②
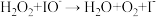
其反应过程的能量变化如图所示,回答下列问题:

(3)在I-存在下,H2O2分解过程的最大能垒(活化能)为
(4)反应过程中I-和IO-的浓度变化趋势为_____。
A.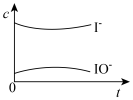 | B.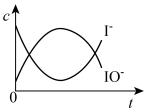 |
C.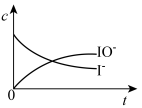 | D.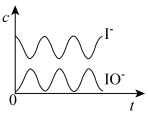 |
Ⅲ.向1L容器中加入1molSO2和足量焦炭,发生反应2C(s)+2SO2(g)
 S2(g)+2CO2(g)。测得反应速率v正(S2)和v逆(SO2)随温度变化如图所示,请回答:
S2(g)+2CO2(g)。测得反应速率v正(S2)和v逆(SO2)随温度变化如图所示,请回答:
(5)A、B、C、D四点对应的状态中,达到平衡状态的有
(6)该反应的△H
(7)下列措施能够增大SO2平衡转化率的是_____。
| A.降温 | B.增加C(s)的量 | C.减小容器体积 | D.恒压通入一定量SO2 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】甲醇的用途十分广泛,主要用于有机合成、作燃料、生成农药、作良好的有机溶剂等。催化CO和H2反应可以合成甲醇,反应化学方程式为CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。
已知:①CO2 (g)+H2(g) CO(g)+H2O(g) ΔH1=+41 kJ·mol−1
CO(g)+H2O(g) ΔH1=+41 kJ·mol−1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol−1
CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol−1
(1)催化CO和H2合成甲醇反应:CO(g)+2H2(g) CH3OH(g)的ΔH=
CH3OH(g)的ΔH=___________ 。
(2)对于催化CO和H2合成甲醇的反应,增大压强,平衡___________ (填“向左”“向右”或“不”)移动;温度升高平衡常数___________ (填“变大”“变小”或“不变”)。
(3)在相同条件下研究催化剂I、催化剂Ⅱ对反应CO(g)+2H2(g) CH3OH(g)的影响,在密闭容器内充入一定量CO和H2,部分物质的浓度c随反应时间t 的变化曲线如图所示。
CH3OH(g)的影响,在密闭容器内充入一定量CO和H2,部分物质的浓度c随反应时间t 的变化曲线如图所示。

①a曲线表示___________ 。
②催化剂I比催化剂Ⅱ催化效率___________ (填“高”“低”或“相同”),原因是___________ 。
(4)523K时,在1 L恒容密闭容器中充入2 mol CO和4 mol H2,在催化剂作用下反应合成甲醇,容器内的压强变化如下。
反应从开始到20 min时,以H2浓度表示平均反应速率v(H2)=___________ ;此温度下,压强平衡常数Kp =___________ (MPa)-2。
(5)一定条件下,在3个相同的密闭容器中分别充入CO2 (g)和H2(g),c(CO2):c(H2)分别为1:1、1:2、 1:3,CO2 (g)的转化率随压强的变化关系如图所示,
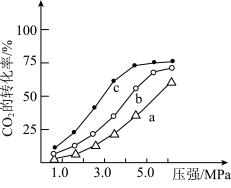
曲线a的c(CO2):c(H2)=___________ ,原因是___________ 。
 CH3OH(g)。
CH3OH(g)。已知:①CO2 (g)+H2(g)
 CO(g)+H2O(g) ΔH1=+41 kJ·mol−1
CO(g)+H2O(g) ΔH1=+41 kJ·mol−1②CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol−1
CH3OH(g)+H2O(g) ΔH2=-58 kJ·mol−1(1)催化CO和H2合成甲醇反应:CO(g)+2H2(g)
 CH3OH(g)的ΔH=
CH3OH(g)的ΔH=(2)对于催化CO和H2合成甲醇的反应,增大压强,平衡
(3)在相同条件下研究催化剂I、催化剂Ⅱ对反应CO(g)+2H2(g)
 CH3OH(g)的影响,在密闭容器内充入一定量CO和H2,部分物质的浓度c随反应时间t 的变化曲线如图所示。
CH3OH(g)的影响,在密闭容器内充入一定量CO和H2,部分物质的浓度c随反应时间t 的变化曲线如图所示。
①a曲线表示
②催化剂I比催化剂Ⅱ催化效率
(4)523K时,在1 L恒容密闭容器中充入2 mol CO和4 mol H2,在催化剂作用下反应合成甲醇,容器内的压强变化如下。
| 反应时间 / min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强 / MPa | 12.4 | 10.2 | 8.4 | 7.0 | 6.2 | 6.2 |
(5)一定条件下,在3个相同的密闭容器中分别充入CO2 (g)和H2(g),c(CO2):c(H2)分别为1:1、1:2、 1:3,CO2 (g)的转化率随压强的变化关系如图所示,

曲线a的c(CO2):c(H2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学反应原理与生产、生活密切相关。请回答以下问题。
(1)山西老陈醋是中国四大名醋之首,食醋的主要成分为醋酸。已知:25℃时 的电离常数
的电离常数 ,
, 的
的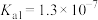 、
、 。请回答:25℃时,浓度均为
。请回答:25℃时,浓度均为 的
的 和
和 的缓冲溶液,
的缓冲溶液, ,该缓冲溶液中离子浓度由大到小的顺序是
,该缓冲溶液中离子浓度由大到小的顺序是___________ ,等浓度的 、
、 两种溶液的碱性较强的是
两种溶液的碱性较强的是___________ 。
(2)亚磷酸(H3PO3)是二元弱酸。已知25℃时, ,
,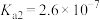 ,
, 属于
属于______ (填“酸式盐”或“正盐”); 溶液显
溶液显______ (填“酸性”“碱性”或“中性”)。
(3)在25℃下,将 的硫酸氢钠和等浓度的氢氧化钡溶液等体积混合,充分反应后溶液的pH=
的硫酸氢钠和等浓度的氢氧化钡溶液等体积混合,充分反应后溶液的pH=________ 。
(4)现有浓度均为 的几种溶液:①
的几种溶液:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ,以上溶液中
,以上溶液中 由大到小的顺序
由大到小的顺序______ (填序号)。
(1)山西老陈醋是中国四大名醋之首,食醋的主要成分为醋酸。已知:25℃时
 的电离常数
的电离常数 ,
, 的
的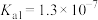 、
、 。请回答:25℃时,浓度均为
。请回答:25℃时,浓度均为 的
的 和
和 的缓冲溶液,
的缓冲溶液, ,该缓冲溶液中离子浓度由大到小的顺序是
,该缓冲溶液中离子浓度由大到小的顺序是 、
、 两种溶液的碱性较强的是
两种溶液的碱性较强的是(2)亚磷酸(H3PO3)是二元弱酸。已知25℃时,
 ,
,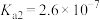 ,
, 属于
属于 溶液显
溶液显(3)在25℃下,将
 的硫酸氢钠和等浓度的氢氧化钡溶液等体积混合,充分反应后溶液的pH=
的硫酸氢钠和等浓度的氢氧化钡溶液等体积混合,充分反应后溶液的pH=(4)现有浓度均为
 的几种溶液:①
的几种溶液:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ,以上溶液中
,以上溶液中 由大到小的顺序
由大到小的顺序
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.已知25℃时,醋酸、碳酸、氢氰酸的电离平衡常数如表。
(1)C、N、O的第一电离能由大到小的顺序为________ ,未成对电子数最多的是______ (填元素符号),其最高能级的原子轨道形状为________ 。
(2)25℃时,浓度相等的三种溶液:① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液,pH由大到小的顺序为
溶液,pH由大到小的顺序为________ (填序号)。
(3)25℃时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为________ 。
(4)25℃时,将一定量 溶液与
溶液与 溶液混合,测得混合后溶液的pH为9,则混合溶液中,
溶液混合,测得混合后溶液的pH为9,则混合溶液中,
______  。
。
Ⅱ.常温下,某实验小组用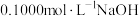 溶液滴定
溶液滴定 溶液。溶液pH、所有含A微粒的分布分数
溶液。溶液pH、所有含A微粒的分布分数 [如
[如 的分布分数:
的分布分数: ]随滴加
]随滴加 溶液体积
溶液体积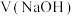 的变化关系如图所示。
的变化关系如图所示。

(5) 是
是_____ 元酸,写出 的电离方程式
的电离方程式________ 。
 |  |  |
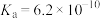 |  , , | 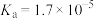 |
(1)C、N、O的第一电离能由大到小的顺序为
(2)25℃时,浓度相等的三种溶液:①
 溶液、②
溶液、② 溶液、③
溶液、③ 溶液,pH由大到小的顺序为
溶液,pH由大到小的顺序为(3)25℃时,向
 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为(4)25℃时,将一定量
 溶液与
溶液与 溶液混合,测得混合后溶液的pH为9,则混合溶液中,
溶液混合,测得混合后溶液的pH为9,则混合溶液中,
 。
。Ⅱ.常温下,某实验小组用
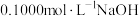 溶液滴定
溶液滴定 溶液。溶液pH、所有含A微粒的分布分数
溶液。溶液pH、所有含A微粒的分布分数 [如
[如 的分布分数:
的分布分数: ]随滴加
]随滴加 溶液体积
溶液体积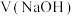 的变化关系如图所示。
的变化关系如图所示。
(5)
 是
是 的电离方程式
的电离方程式
您最近一年使用:0次
【推荐3】碲是VIA族元素,其单质和化合物在化工生产等方面具有广泛地应用。
(1)TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。TeO2和NaOH溶液发生反应的离子方程式为_________________________________ 。
(2)碲酸(H6TeO6)是一种很弱的酸,Ka1=1×10-7,该温度下,0.1mol/L H6TeO6的电离度a为_____________ (结果保留1位有效数字)。
(3)从粗铜精练的阳极泥(主要含有Cu2Te)中提取粗碲的一种工艺流程如图:

①已知加压酸浸时控制溶液的pH为5.0,生成TeO2沉淀。如果H2SO4溶液浓度过大,产生的后果是____________________________ 。
②“加压酸浸”中为什么要加压?_______________________________ 。
③对滤渣“酸浸”后,将Na2SO3加入Te(SO4)2溶液中进行“还原”得到固态碲,该反应的离子方程式是_________________________________ 。
④“还原”得到固态碲后分离出粗碲的方法是_______ ,对粗碲进行洗涤,判断洗涤干净的实验操作和现象是______________________________________ 。
已知阳极泥中Cu2Te的含量为a%,则m吨阳极泥理论上可制得纯度为n%的粗碲___ 吨。
(1)TeO2是两性氧化物,微溶于水,可溶于强酸或强碱。TeO2和NaOH溶液发生反应的离子方程式为
(2)碲酸(H6TeO6)是一种很弱的酸,Ka1=1×10-7,该温度下,0.1mol/L H6TeO6的电离度a为
(3)从粗铜精练的阳极泥(主要含有Cu2Te)中提取粗碲的一种工艺流程如图:

①已知加压酸浸时控制溶液的pH为5.0,生成TeO2沉淀。如果H2SO4溶液浓度过大,产生的后果是
②“加压酸浸”中为什么要加压?
③对滤渣“酸浸”后,将Na2SO3加入Te(SO4)2溶液中进行“还原”得到固态碲,该反应的离子方程式是
④“还原”得到固态碲后分离出粗碲的方法是
已知阳极泥中Cu2Te的含量为a%,则m吨阳极泥理论上可制得纯度为n%的粗碲
您最近一年使用:0次








