3-乙基吡啶(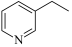 )是一种重要的有机合成中间体,具有芳香性。回答下列问题:
)是一种重要的有机合成中间体,具有芳香性。回答下列问题:
(1)3-乙基吡啶中所含元素电负性由大到小的顺序为____ ;其中碳原子的杂化方式为____ 。
(2)3-乙基吡的沸点高于2,6-二甲基吡啶(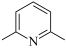 ),分析可能的原因为
),分析可能的原因为____ 。
(3)吡啶(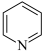 )的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与
)的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与____ molH2发生加成反应;3-乙基吡啶与浓硫酸、浓硝酸混合,在一定条件下发生硝化反应的方程式为___ 。
(4)3-乙基吡啶有多种同分异构体,其中含苯环的同分异构体有____ 种(不考虑立体异构),其中核磁共振氢谱有4组峰的结构简式为____ 。
 )是一种重要的有机合成中间体,具有芳香性。回答下列问题:
)是一种重要的有机合成中间体,具有芳香性。回答下列问题:(1)3-乙基吡啶中所含元素电负性由大到小的顺序为
(2)3-乙基吡的沸点高于2,6-二甲基吡啶(
 ),分析可能的原因为
),分析可能的原因为(3)吡啶(
 )的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与
)的键合情况和苯类似,所以与苯有类似的性质,既能发生加成反应,又能发生取代反应;其中发生取代反应时,N间位碳原子上的氢原子要比邻位和对位活泼。1mol3-乙基吡啶最多能与(4)3-乙基吡啶有多种同分异构体,其中含苯环的同分异构体有
更新时间:2022-07-15 20:23:08
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)符合下列3个条件的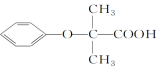 的同分异构体有
的同分异构体有_______ 种。①与FeCl3溶液显色;②苯环上只有两个取代基;③1 mol该物质最多消耗3 mol NaOH,其中氢原子共有五种不同环境的是_______ (写结构简式)。
(2)同时满足下列条件:①与FeCl3溶液发生显色反应;②苯环上有两个取代基、含C=O的 的同分异构体有
的同分异构体有_______ 种(不包括立体异构);其中核磁共振氢谱为4组峰、能水解的物质的结构简式为_______ 。
 的同分异构体有
的同分异构体有(2)同时满足下列条件:①与FeCl3溶液发生显色反应;②苯环上有两个取代基、含C=O的
 的同分异构体有
的同分异构体有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】肉桂醛是一种食用香精,它广泛用于牙膏、洗涤剂、糖果以及调味品中。工业上通过下列反应制备:

(1)肉桂醛所含官能团的名称是___________ 。
(2)请写出两分子的乙醛在上述条件下反应的化学方程式:___________ 。
(3)B有多种同分异构体,同时满足下列条件的同分异构体有___________ 种。
①分子中不含羰基和羟基;②是苯的对二取代物;③除苯环外,不含其他环状结构。
(4)肉桂醛与新制Cu(OH)2反应的化学方程式是___________ 。

(1)肉桂醛所含官能团的名称是
(2)请写出两分子的乙醛在上述条件下反应的化学方程式:
(3)B有多种同分异构体,同时满足下列条件的同分异构体有
①分子中不含羰基和羟基;②是苯的对二取代物;③除苯环外,不含其他环状结构。
(4)肉桂醛与新制Cu(OH)2反应的化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知O的电负性为3.5,Cl为3.1,但Cl2 远比O2 活泼,请加以解释。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置_______ ,钛原子核外有_______ 种空间运动状态不同的电子,Ti2+电子占据的最高能层的电子排布式为_______ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是_______ ,第一电离能介于Al、P之间的第三周期元素为_______ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为_______ ,B原子的杂化方式是_______ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有_______ (填序号)
①σ键②π键③氢键④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为_______ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
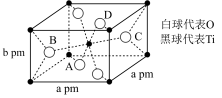
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
【推荐3】按要求完成下列填空。
(1)在元素周期表中电负性最大的元素是_______ (填元素符号);短周期中第一电离能最小的元素基态原子的价层电子排布图为_______ 。
(2)基态原子的2p轨道上有两个未成对电子的元素有_______ (填元素符号)。前四周期元素中,未成对电子数最多的元素基态原子的价层电子排布式为_______ 。
(3) 中
中 原子的杂化方式为
原子的杂化方式为_______ ,属于_______ (“极性”或“非极性”)分子。
(4)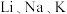 熔沸点依次降低的原因是
熔沸点依次降低的原因是_______ 。
(1)在元素周期表中电负性最大的元素是
(2)基态原子的2p轨道上有两个未成对电子的元素有
(3)
 中
中 原子的杂化方式为
原子的杂化方式为(4)
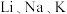 熔沸点依次降低的原因是
熔沸点依次降低的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】[化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求填空。
I.元素周期表中第四周期过渡元素在工业及生活方面有重要应用。请回答下列问题:
(1)“钛”被称为 21 世纪金属,画出基态钛的价电子的轨道表示式_______ 。
(2)能区别[Co(NH3)4Cl2]Cl 和[Co(NH3)4Cl2]NO3两种溶液的试剂是_______ (填选项)。
(3)K3[Fe(CN)6]是鉴别 Fe2+的重要试剂,这四种元素的电负性从大到小的顺序是_______ (填元素符号),K3[Fe(CN)6]中碳的杂化方式与下列物质中碳杂化方式相同的是_______ (填选项)。
A.CH2Cl2 B.C2H2 C.溴苯 D.乙烯
II.根据题意写出化学方程式:
(4)写出肉桂醛 ( )与银氨溶液反应的化学方程式
)与银氨溶液反应的化学方程式_______ 。
(5)写出有机物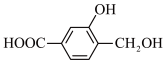 与足量 NaOH 反应的化学方程式
与足量 NaOH 反应的化学方程式_______ 。
(6)两分子苹果酸(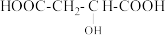 )在浓硫酸作用下可生成六元环状化合物,写出该化学方程式
)在浓硫酸作用下可生成六元环状化合物,写出该化学方程式_______ 。
(7)写出苯甲酸甲酯(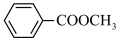 )在 NaOH 溶液中发生水解反应的化学方程式
)在 NaOH 溶液中发生水解反应的化学方程式_____ 。
I.元素周期表中第四周期过渡元素在工业及生活方面有重要应用。请回答下列问题:
(1)“钛”被称为 21 世纪金属,画出基态钛的价电子的轨道表示式
(2)能区别[Co(NH3)4Cl2]Cl 和[Co(NH3)4Cl2]NO3两种溶液的试剂是_______ (填选项)。
| A.浓氨水 | B.NaOH 溶液 | C.稀 H2SO4 | D.AgNO3溶液 |
A.CH2Cl2 B.C2H2 C.溴苯 D.乙烯
II.根据题意写出化学方程式:
(4)写出肉桂醛 (
 )与银氨溶液反应的化学方程式
)与银氨溶液反应的化学方程式(5)写出有机物
 与足量 NaOH 反应的化学方程式
与足量 NaOH 反应的化学方程式(6)两分子苹果酸(
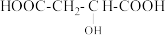 )在浓硫酸作用下可生成六元环状化合物,写出该化学方程式
)在浓硫酸作用下可生成六元环状化合物,写出该化学方程式(7)写出苯甲酸甲酯(
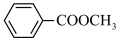 )在 NaOH 溶液中发生水解反应的化学方程式
)在 NaOH 溶液中发生水解反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请按要求回答下列问题:
(1)基态Cr原子的价电子排布图为:___________ 。
(2)基态氯原子核外电子占据的最高能层的符号为:___________ ,其最外层有___________ 种运动状态不同的电子。
(3)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为___________ 。
(4)CO与N2互为等电子体,1molCO分子内含有π键___________ mol。
(5)NCl3分子的中心原子的杂化方式为___________ 。
(1)基态Cr原子的价电子排布图为:
(2)基态氯原子核外电子占据的最高能层的符号为:
(3)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(4)CO与N2互为等电子体,1molCO分子内含有π键
(5)NCl3分子的中心原子的杂化方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:______ 、_______ 、________ 。
(2)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)____ 。
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):HClO3___ HClO4;
(2)在下列物质①CO2、②NH3、③CCl4、④BF3、⑤H2O、⑥SO2、⑦SO3、⑧PCl3中,属于非极性分子的是(填序号)
(3)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):HClO3
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】键的极性与分子的极性关系
(1)只含有非极性键的双原子分子或多原子分子大多是___________ ,如O2、H2、P4、C60。
(2)含有极性键的双原子分子都是___________ ,如HCl、HF、HBr。
(3)含有极性键的多原子分子,立体构型对称的是___________ ;立体构型不对称的是___________ 。
(1)只含有非极性键的双原子分子或多原子分子大多是
(2)含有极性键的双原子分子都是
(3)含有极性键的多原子分子,立体构型对称的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】碳族元素的物质是化学世界中最庞大的家族,“天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是___________。
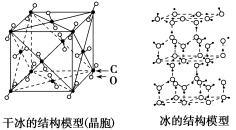
(3)干冰和冰的晶体模型如下图存在差别的本质原因___________ 。___________ 。
(5)金刚石晶体中,每个C被___________ 个六元环共用。
(6)晶体硅和碳化硅熔点较高的是___________ (填化学式)。
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为___________ 。
(1)已知 25℃时,H2CO3的Ka1=4.2×10-7、Ka2=4.8×10- 11,HCN的Ka=4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是___________。
A.电子式为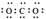 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
(5)金刚石晶体中,每个C被
(6)晶体硅和碳化硅熔点较高的是
(7)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为
您最近一年使用:0次

 )互为同系物。分子组成比A多1个CH2,M分子可能的结构有
)互为同系物。分子组成比A多1个CH2,M分子可能的结构有

