有机物种类繁多,应用广泛。
(1)邻氨基吡啶(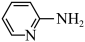 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为______ (填元素符号)。1mol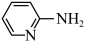 中含有σ键的数目为
中含有σ键的数目为______ mol。
(2)一种鸟嘌呤和吡咯的结构如图。
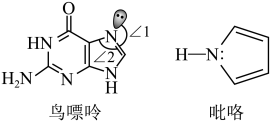
①鸟嘌呤中轨道之间的夹角∠1______ ∠2(填“>”或“<”)。
②分子中的大π键可以用符号π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为______ 。
(3)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。
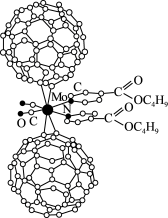
①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布式是______ ,该超分子中存在的化学键类型有______ (填选项字母)。
A.离子键 B.氢键 C.σ键 D.π键
②该超分子中,配体CO提供孤电子对的原子是______ (填元素符号),p-甲酸丁酯吡啶配体中C原子的杂化方式有_______ 。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为 中含有σ键的数目为
中含有σ键的数目为(2)一种鸟嘌呤和吡咯的结构如图。

①鸟嘌呤中轨道之间的夹角∠1
②分子中的大π键可以用符号π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数。则该吡咯中的大π键可表示为(3)超分子化学已逐渐扩展到化学的各个领域。由Mo将2个C60分子、2个p-甲酸丁酯吡啶及2个CO分子利用配位键自组装的超分子结构如图所示。

①Mo处于第五周期第VIB族,价电子排布与Cr相似,它的基态价电子排布式是
A.离子键 B.氢键 C.σ键 D.π键
②该超分子中,配体CO提供孤电子对的原子是
更新时间:2023-05-26 17:09:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)基态 原子中,电子占据的最高能层符号为
原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_______ 、电子数为_______ 。
(2) 的价电子排布图为
的价电子排布图为_______ 。
(3)Br原子序数为_______ ,其核外 层电子的排布式为
层电子的排布式为_______ 。
(1)基态
 原子中,电子占据的最高能层符号为
原子中,电子占据的最高能层符号为(2)
 的价电子排布图为
的价电子排布图为(3)Br原子序数为
 层电子的排布式为
层电子的排布式为
您最近一年使用:0次
【推荐2】请回答下列问题:
(1)某元素X基态原子的最外层有3个未成对电子,次外层有2个电子,其价电子排布图为___ ,其原子核外有___ 种不同运动状态的电子;其最低价氢化物电子式为___ ,中心原子采用___ 杂化,分子立体构型为___ 。
(2)某元素Y基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其元素名称为___ ,Y+的外围电子排布式为___ ,该元素固体单质常常采用___ 堆积方式,配位数为___ ,空间利用率为___ 。
(1)某元素X基态原子的最外层有3个未成对电子,次外层有2个电子,其价电子排布图为
(2)某元素Y基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其元素名称为
您最近一年使用:0次
【推荐3】现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
(2) 元素的原子核外共有
元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3) 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是___________ 。
(5) 位于元素周期表中
位于元素周期表中___________ 区(按电子排布分区),其基态原子的价层电子排布式为___________ 。
(6)G单质投入水中所得溶液阳离子检验方法___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
 元素是形成化合物种类最多的元素 元素是形成化合物种类最多的元素 |
 元素基态原子的核外 元素基态原子的核外 能级电子数比 能级电子数比 能级电子总数少1个 能级电子总数少1个 |
 元素基态原子的核外 元素基态原子的核外 轨道中有两个未成对电子 轨道中有两个未成对电子 |
 元素的气态基态原子的第一至第四电离能分别是 元素的气态基态原子的第一至第四电离能分别是 , , , , , ,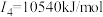 |
 元素的主族序数与周期数的差为4 元素的主族序数与周期数的差为4 |
 元素是前四周期中电负性最小的元素 元素是前四周期中电负性最小的元素 |
 元素位于元素周期表中的第8列 元素位于元素周期表中的第8列 |
 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)(2)
 元素的原子核外共有
元素的原子核外共有(3)
 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是(5)
 位于元素周期表中
位于元素周期表中(6)G单质投入水中所得溶液阳离子检验方法
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)下图是s能级和p能级的原子轨道图,试回答下列问题:

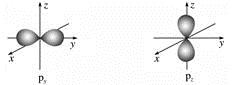
s电子的原子轨道呈________ 形,每个s能级有________ 个原子轨道;p电子的原子轨道呈________ 形,每个p能级有________ 个原子轨道。
(2)有X、Y、Z、Q、E、M、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,E与Q同周期,M元素的第一电离能在同周期主族元素中从大到小排第三位,G原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。回答下列问题:
①基态G原子的价电子排布式为____________ ,写出第三周期基态原子未成对电子数与G相同且电负性最大的元素是________ (填元素名称)。GQ受热分解生成G2Q和Q2,请从G的原子结构来说明GQ受热易分解的原因:________ 。
②Z、Q、M三种元素的第一电离能从大到小的顺序为____________ (用元素符号表示)。
③X与Q形成原子个数比为1:1的化合物的化学式为________ 。
④Z、M、E所形成的简单离子的半径由大到小顺序为____________ (用离子符号表示)。
⑤X、Y、Z、Q的电负性由大到小的顺序为__________ (用元素符号表示)。

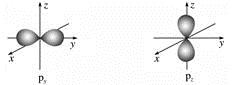
s电子的原子轨道呈
(2)有X、Y、Z、Q、E、M、G原子序数依次递增的七种元素,除G元素外其余均为短周期主族元素。X的原子中没有成对电子,Y元素基态原子中电子占据三种能量不同的原子轨道且每种轨道中的电子数相同,Z元素原子的外围电子层排布式为nsnnpn+1,Q的基态原子核外成对电子数是成单电子数的3倍,E与Q同周期,M元素的第一电离能在同周期主族元素中从大到小排第三位,G原子最外电子层只有未成对电子,其内层所有轨道全部充满,但并不是第ⅠA族元素。回答下列问题:
①基态G原子的价电子排布式为
②Z、Q、M三种元素的第一电离能从大到小的顺序为
③X与Q形成原子个数比为1:1的化合物的化学式为
④Z、M、E所形成的简单离子的半径由大到小顺序为
⑤X、Y、Z、Q的电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
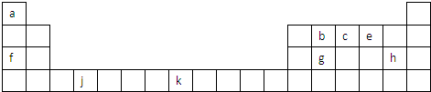
【推荐2】如图是元素周期表的一部分,表中所列字母分别代表一种元素.
试回答下列问题:
(1)以上元素中,属于d区元素的是________ (填元素符号),h在周期表的位置是_________ 。
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为______________ 。
(3)元素k的基态原子电子排布式为__________ ;画出c的核外电子排布图:_____________ 。
(4)元素c的电负性______ 元素g的电负性(填“>”、“=”、“<”),元素b、c、e的第一电离能由大到小的顺序是___________________ (用元素符号表示)。
(5)工业上冶炼g元素的单质的化学方程式_______________________________ ,f、 h两种元素最高价氧化物对应的水化物反应的化学方程式是___________________ 。
试回答下列问题:
(1)以上元素中,属于d区元素的是
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为
(3)元素k的基态原子电子排布式为
(4)元素c的电负性
(5)工业上冶炼g元素的单质的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】对氨基苯甲酸和邻氨基苯甲酸分别用于防晒剂和制造药物,某小组以甲苯为主要原料进行合成,设计流程如下图。
ii .苯胺中的氨基易被氧化
iii.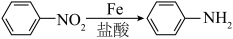
(1)基态N原子的电子有___________ 种运动状态。
(2)氨基苯甲酸中C=O中O原子的杂化方式是___________ 。
(3)组成氨基苯甲酸的4种元素的电负性由大到小的顺序是___________ 。
(4)对氨基苯甲酸和邻氨基苯甲酸的沸点分别是339.9℃和311.9℃,沸点不同的原因是___________ 。
(5)甲同学认为邻氨基苯甲酸可以形成“内盐”,请从化学键的角度解释“内盐”中离子键的形成过程___________ 。
(6)步骤A的反应条件___________ ;步骤C中生成1 mol对氨基苯甲酸电子转移___________ mol。
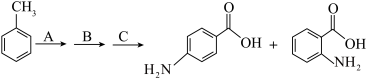
ii .苯胺中的氨基易被氧化
iii.
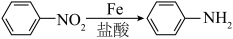
(1)基态N原子的电子有
(2)氨基苯甲酸中C=O中O原子的杂化方式是
(3)组成氨基苯甲酸的4种元素的电负性由大到小的顺序是
(4)对氨基苯甲酸和邻氨基苯甲酸的沸点分别是339.9℃和311.9℃,沸点不同的原因是
(5)甲同学认为邻氨基苯甲酸可以形成“内盐”,请从化学键的角度解释“内盐”中离子键的形成过程
(6)步骤A的反应条件
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)COCl2分子中所有原子均满足8电子稳定结构,COCl2分子中σ键和π键的个数比为____ ,中心原子的杂化方式为____ 。
(2)AlH 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为____ ;列举与AlH 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:____ 、____ (填化学式)。
(3)用价层电子对互斥模型推断SnBr2分子中,Sn原子的轨道杂化方式为____ ,SnBr2分子中Br—Sn—Br的键角____ 120°(填“>”“<”或“=”)。
(1)COCl2分子中所有原子均满足8电子稳定结构,COCl2分子中σ键和π键的个数比为
(2)AlH
 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为 空间结构相同的一种离子和一种分子:
空间结构相同的一种离子和一种分子:(3)用价层电子对互斥模型推断SnBr2分子中,Sn原子的轨道杂化方式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】完成下列问题
(1)配体氨基乙酸根 受热分解可产生
受热分解可产生 和
和 ,
, 中
中 键和
键和 键数目之比是
键数目之比是_______ 。
(2)已知: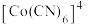 是强还原剂,与水反应能生成
是强还原剂,与水反应能生成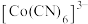 。
。 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为_______ ,该离子中C的杂化方式为_______ 。
(3) 的结构如图所示。
的结构如图所示。 原子的杂化类型为
原子的杂化类型为_______ , 配体bpy分子中含有
配体bpy分子中含有 键的数目为
键的数目为_______  。
。

(1)配体氨基乙酸根
 受热分解可产生
受热分解可产生 和
和 ,
, 中
中 键和
键和 键数目之比是
键数目之比是(2)已知:
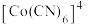 是强还原剂,与水反应能生成
是强还原剂,与水反应能生成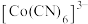 。
。 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为(3)
 的结构如图所示。
的结构如图所示。 原子的杂化类型为
原子的杂化类型为 配体bpy分子中含有
配体bpy分子中含有 键的数目为
键的数目为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】钛、铬、铁、镍、铜等金属及其化合物在工业上有重要用途。
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为________________ 。
②Fe的基态原子共有________ 种不同能级的电子。
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是____________ (用元素符号表示)。
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为________ ,中心原子的杂化方式为________ 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2 nm和7.8×10-2 nm。则熔点:NiO________ (填“>”、“<”或“=”)FeO。
(4)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式_____________________________ 。

若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为________________ cm。(阿伏伽德罗常数用NA表示)
(1)钛铁合金是钛系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为
②Fe的基态原子共有
(2)制备CrO2Cl2的反应为K2Cr2O7+3CCl4===2KCl+2CrO2Cl2+3COCl2↑。
①上述化学方程式中非金属元素电负性由大到小的顺序是
②COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中Ni2+和Fe2+的离子半径分别为6.9×10-2 nm和7.8×10-2 nm。则熔点:NiO
(4)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式

若该晶体的密度是ρg·cm-3,则两个最近的Fe原子间的距离为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】锰及其化合物用途非常广泛。回答下列问题:
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是___________ 。
(2)基态Mn原子的价电子排布式为_________ ,未成对电子数为_____ 个。
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是____________ 。
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为________ 。
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是_____ ,该分子中碳原子的杂化方式为_______ ;C、H、N的电负性从大到小的顺序为________ 。
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是_________ 。
(6)某种含锰特殊材料的晶胞结构如下图所示:
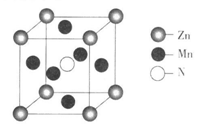
若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为____ ( 列出代数式即可)。
(1)Al70Pd21Mn9是一种准晶体(介于晶体和非晶体之间的固体),能准确证明其不是晶体的方法是
(2)基态Mn原子的价电子排布式为
(3)MnS熔点(1610℃)比MnO熔点(1650℃)低,其原因是
(4)锰的一种配合物的化学式为[Mn(CO)5(CH3CN)]Br。
①配合物中锰元素的价态为
②配体CH3CN与中心原子形成配位键时,提供孤对电子的原子是
(5)锰的含氧酸有HMnO4(高锰酸)、H2MnO3(亚锰酸),高锰酸的酸性比亚锰酸强,理由是
(6)某种含锰特殊材料的晶胞结构如下图所示:

若晶胞参数为a nm,用NA表示阿伏伽德罗常数的值,则该晶胞的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】中国古代四大发明之一——黑火药,它在爆炸时发生的化学反应为2KNO3+3C+S=A+N2↑+3CO2↑(已配平)
(1)①除S外,上列元素的电负性从大到小依次为__________ 。
②在生成物中,A的晶体类型为_______ ,含极性共价键的分子的中心原子轨道杂化类型为_____ 。
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为_____ 。
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为______ ,Q2+的未成对电子数是_______ 。
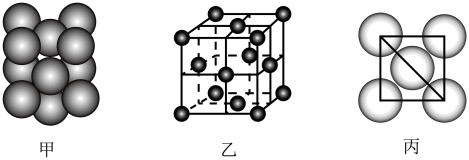
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为________ ,该单质晶体中原子的堆积方式为四种基本堆积方式中的________ 。
(1)①除S外,上列元素的电负性从大到小依次为
②在生成物中,A的晶体类型为
③已知CN-与N2互为等电子体,推算HCN分子中σ键与π键数目之比为
(2)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2。T的基态原子外围电子(价电子)排布为
(3)若某金属单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。则晶胞中该原子的配位数为

您最近一年使用:0次



