现有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1) 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
(2) 元素的原子核外共有
元素的原子核外共有___________ 种不同运动状态的电子,基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3) 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是___________ 。
(4) 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是___________ 。
(5) 位于元素周期表中
位于元素周期表中___________ 区(按电子排布分区),其基态原子的价层电子排布式为___________ 。
(6)G单质投入水中所得溶液阳离子检验方法___________ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
8种元素,均为前四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答有关问题。 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
 元素是形成化合物种类最多的元素 元素是形成化合物种类最多的元素 |
 元素基态原子的核外 元素基态原子的核外 能级电子数比 能级电子数比 能级电子总数少1个 能级电子总数少1个 |
 元素基态原子的核外 元素基态原子的核外 轨道中有两个未成对电子 轨道中有两个未成对电子 |
 元素的气态基态原子的第一至第四电离能分别是 元素的气态基态原子的第一至第四电离能分别是 , , , , , ,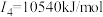 |
 元素的主族序数与周期数的差为4 元素的主族序数与周期数的差为4 |
 元素是前四周期中电负性最小的元素 元素是前四周期中电负性最小的元素 |
 元素位于元素周期表中的第8列 元素位于元素周期表中的第8列 |
 的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)
的电子式为___________。(A、C为字母代号,请将字母代号用元素符号表示,下同)(2)
 元素的原子核外共有
元素的原子核外共有(3)
 元素原子的
元素原子的 远远大于
远远大于 ,其原因是
,其原因是(4)
 、
、 、
、 三种元素的简单离子半径由大到小的顺序是
三种元素的简单离子半径由大到小的顺序是(5)
 位于元素周期表中
位于元素周期表中(6)G单质投入水中所得溶液阳离子检验方法
更新时间:2024-03-13 09:52:32
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】中医认为:“肺主秋,肺收敛,急食酸以收之,用酸补之,辛泄之”。就是说秋天是“收”的季节,吃酸味的食物可以起到收敛肺气的作用。醋酸、酒石酸、维生素C均是食物中常见的酸性物质。请回答下列问题:
(1)醋酸可以与食物中以不溶性状态存在的钙元素生成可溶性的(CH3COO)2Ca,Ca2+的核外电子排布式为___________ ,钙元素焰色反应的焰色为___________ (填标号)。
A.黄色 B.红色 C.紫色 D.绿色。
(2)酒石酸是二元弱酸,结构简式为 ,请从结构与性质的关系解释其第一步电离程度大于第二步电离程度的原因:
,请从结构与性质的关系解释其第一步电离程度大于第二步电离程度的原因:___________ 。
(3)维生素的结构简式为 ,其中氧原子的杂化方式为
,其中氧原子的杂化方式为___________ 。维生素C易溶于水的主要原因为___________ 。
(4)醋酸铵可用作分析试剂、肉类防腐剂、医药工业,常用来测定醋酸铵官能团类别的仪器名称为___________ ,与NH 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为___________ (写一种)。
(1)醋酸可以与食物中以不溶性状态存在的钙元素生成可溶性的(CH3COO)2Ca,Ca2+的核外电子排布式为
A.黄色 B.红色 C.紫色 D.绿色。
(2)酒石酸是二元弱酸,结构简式为
 ,请从结构与性质的关系解释其第一步电离程度大于第二步电离程度的原因:
,请从结构与性质的关系解释其第一步电离程度大于第二步电离程度的原因:(3)维生素的结构简式为
 ,其中氧原子的杂化方式为
,其中氧原子的杂化方式为(4)醋酸铵可用作分析试剂、肉类防腐剂、医药工业,常用来测定醋酸铵官能团类别的仪器名称为
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)下列几种物质,其中属于电解质的是___________ 。(填序号)
① ②CaO ③盐酸 ④KOH ⑤Fe
②CaO ③盐酸 ④KOH ⑤Fe
(2)人们通过焰色试验制造了绚丽多彩的烟花,下列焰色为紫色的是___________ 。(填序号)
a. b.NaCl c.
b.NaCl c.
(3)漂白粉的有效成分为___________ ;在空气中失效的方程式为___________ 。
(4)标准状况下11.2L 气体的质量为
气体的质量为___________ ;与0.1mol  含有相同电子数的
含有相同电子数的 在标状况下的体积为
在标状况下的体积为___________ ;同温同压下,同体积的 和
和 气体的质量比为
气体的质量比为___________ ;同质量的 和
和 中氢原子的个数比为
中氢原子的个数比为___________ ;8.4g  与9.6g某单质
与9.6g某单质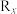 ,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是
,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是___________ ,x值为___________ 。
(5)把标准状况下134.4L HCl气体溶于861mL水中,所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为___________  。
。
(6)硫酸、氨水的密度与所加水量的关系如图所示(水的密度为 ),请根据图中信息,回答下列问题:
),请根据图中信息,回答下列问题: ,则质量分数为a%的氨水物质的量浓度
,则质量分数为a%的氨水物质的量浓度___________ (填“大于”、“小于”或硫酸“等于”)5 ;已知8
;已知8 的硫酸溶液密度为
的硫酸溶液密度为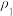 ,4
,4 的硫酸溶液密度为
的硫酸溶液密度为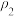 。200g浓度为8
。200g浓度为8 的硫酸溶加水的量
的硫酸溶加水的量___________ mL水混合,使硫酸的物质的量浓度减小到4 。(用含
。(用含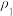 、
、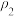 的式子表示)
的式子表示)
(1)下列几种物质,其中属于电解质的是
①
 ②CaO ③盐酸 ④KOH ⑤Fe
②CaO ③盐酸 ④KOH ⑤Fe(2)人们通过焰色试验制造了绚丽多彩的烟花,下列焰色为紫色的是
a.
 b.NaCl c.
b.NaCl c.
(3)漂白粉的有效成分为
(4)标准状况下11.2L
 气体的质量为
气体的质量为 含有相同电子数的
含有相同电子数的 在标状况下的体积为
在标状况下的体积为 和
和 气体的质量比为
气体的质量比为 和
和 中氢原子的个数比为
中氢原子的个数比为 与9.6g某单质
与9.6g某单质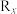 ,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是
,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是(5)把标准状况下134.4L HCl气体溶于861mL水中,所得溶液的密度为
 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为 。
。(6)硫酸、氨水的密度与所加水量的关系如图所示(水的密度为
 ),请根据图中信息,回答下列问题:
),请根据图中信息,回答下列问题:
 ,则质量分数为a%的氨水物质的量浓度
,则质量分数为a%的氨水物质的量浓度 ;已知8
;已知8 的硫酸溶液密度为
的硫酸溶液密度为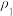 ,4
,4 的硫酸溶液密度为
的硫酸溶液密度为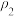 。200g浓度为8
。200g浓度为8 的硫酸溶加水的量
的硫酸溶加水的量 。(用含
。(用含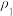 、
、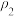 的式子表示)
的式子表示)
您最近一年使用:0次
【推荐3】单质硅是制造太阳能电池板的主要原料,制备电池板时还需添加硼、氮、钛、钴、钙等多种化学物质。
请回答下列问题:
(1)基态硼原子的电子排布式为______ ,下列钴原子的价层电子轨道表示式中,不符合洪特规则的是______ (填选项字母)。
A.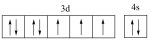 B.
B.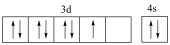
C.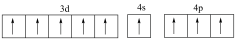 D.
D.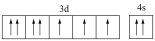
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为______ (用元素符号表示),原因为______ 。
(3)钛元素位于元素周期表______ 区;基态钛原子中,最外层电子的电子云轮廓图为______ 。
(4) 在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:
在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:______ 。
请回答下列问题:
(1)基态硼原子的电子排布式为
A.
 B.
B.
C.
 D.
D.
(2)氮与其同周期相邻两元素的第一电离能由大到小的顺序为
(3)钛元素位于元素周期表
(4)
 在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:
在火焰上灼烧时火焰的颜色为砖红色,从微观角度解释部分金属元素在火焰上灼烧呈现不同颜色的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】1869年,俄国化学家门捷列夫编制了一份元素周期表,随着不断地研究和修正,现代的元素周期表逐渐发展大家所熟知的这种常见形式。
(1)一种药物的分子结构如图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M的原子序数为W的两倍。下列说法中错误的是_____ (单选)。

(2)下列关于元素周期表的说法正确的是_____ (单选)。
I.海水中含有大量的氯化钠,是生活中和人体内不可或缺的,也被用来生产各种含氯和含钠的制品,为人们的日常生活和化学工业提供重要的原料。氯元素的“价类二维图”的部分信息如图。

(3)写出Cl2和水反应生成Z的离子方程式______ 。
(4)用化学方程式表示84消毒液在空气中的漂白原理______ 。
Ⅱ.为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。

(5)甲装置中,a电极的反应式为______ 。
(6)乙装置对应的氯碱工业中,使用阳离子交换膜的好处是______ 。
(7)用如图示的方法可以保护钢质闸门。下列说法正确的是______ (不定项)

(1)一种药物的分子结构如图所示,其中X、Y、Z、W、M是原子序数依次增大的短周期主族元素,M的原子序数为W的两倍。下列说法中错误的是

| A.YM2的键角为180° |
| B.X、Z、W只能形成共价化合物 |
| C.第一电离能:Z>W>Y |
| D.Z、W分别与X形成的最简单化合物中,W所形成的化合物热稳定性最高 |
| A.IA族元素全部是金属元素,称为碱金属元素 |
| B.元素周期表第15列全为非金属元素 |
| C.元素周期表中电负性最强的元素是Cl |
| D.在过渡元素区域可以寻找优良的催化剂 |
I.海水中含有大量的氯化钠,是生活中和人体内不可或缺的,也被用来生产各种含氯和含钠的制品,为人们的日常生活和化学工业提供重要的原料。氯元素的“价类二维图”的部分信息如图。

(3)写出Cl2和水反应生成Z的离子方程式
(4)用化学方程式表示84消毒液在空气中的漂白原理
Ⅱ.为探究原电池和电解池的工作原理,某研究性小组分别用如图所示装置进行实验。

(5)甲装置中,a电极的反应式为
(6)乙装置对应的氯碱工业中,使用阳离子交换膜的好处是
(7)用如图示的方法可以保护钢质闸门。下列说法正确的是

| A.当a、b间用导线连接时,X可以是锌棒,X上发生氧化反应 |
| B.当a、b间用导线连接时,X可以是锌棒,电子经导线流入X |
| C.当a、b与外接电源相连时,a应连接电源的正极 |
| D.当a、b与外接电源相连时,阴极的电极反应式:2Cl--2e-=Cl2↑ |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响。如氧气、水、臭氧、二氧化硫等。
(1)在氧、硫、硒、碲元素原子形成的简单阴离子中,其离子半径由大到小的顺序为_________ (用离子符号表示)。与硫元素同周期且在本周期中非金属性最强的元素在周期表中的位置_______ 。
(2)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是________
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(3)火山喷发时会释放出许多H2S气体,请写出H2S分子的电子式____________ 。在H2S分子中, 两个H—S键之间的夹角_____________ (填“大于”、“小于”或“等于”)180°,H2S分子属_____ (填“极性”或“非极性”)分子。
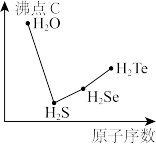
(4)从图可知氧族元素氢化物的沸点变化规律是____________________ 。
(1)在氧、硫、硒、碲元素原子形成的简单阴离子中,其离子半径由大到小的顺序为
(2)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(3)火山喷发时会释放出许多H2S气体,请写出H2S分子的电子式

(4)从图可知氧族元素氢化物的沸点变化规律是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量橄榄石矿物(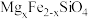 )。回答下列问题:
)。回答下列问题:
(1)基态Fe原子的价电子排布式为__________ 。橄榄石中,各元素电负性大小顺序为__________ ,铁的化合价为__________ 。
(2) 分子的空间结构(以
分子的空间结构(以 为中心)名称为
为中心)名称为__________ ,分子中氮原子的杂化轨道类型是__________ 。 原子核外有种不同运动状态的电子
原子核外有种不同运动状态的电子__________ 。
(3)由硅原子核形成的三种微粒,电子排布式分别为:① 、②
、② 、③
、③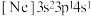 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。
(4)根据价层电子对互斥理论,NH3、 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是___________ (填化学式); 与
与 中O-N-O的键角:
中O-N-O的键角: 
________  (填“<”、“>”、“=”),解释原因
(填“<”、“>”、“=”),解释原因__________ 。
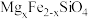 )。回答下列问题:
)。回答下列问题:(1)基态Fe原子的价电子排布式为
(2)
 分子的空间结构(以
分子的空间结构(以 为中心)名称为
为中心)名称为 原子核外有种不同运动状态的电子
原子核外有种不同运动状态的电子(3)由硅原子核形成的三种微粒,电子排布式分别为:①
 、②
、② 、③
、③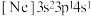 ,有关这些微粒的叙述,正确的是___________。
,有关这些微粒的叙述,正确的是___________。| A.微粒半径:③>①>② |
| B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ |
| D.得电子能力:①>② |
 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是 与
与 中O-N-O的键角:
中O-N-O的键角: 
 (填“<”、“>”、“=”),解释原因
(填“<”、“>”、“=”),解释原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知元素周期表中共有18纵行,如图实线表示元素周期表的边界。按电子排布,可把周期表里的元素划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入的电子的能级符号。
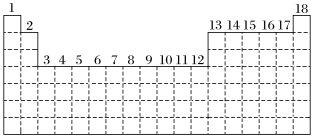
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影 和
和 表示d区和ds区。
表示d区和ds区。___________
(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在___________ 区。
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布___________ 种元素。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
 和
和 表示d区和ds区。
表示d区和ds区。(2)有的同学受这种划分的启发,认为d区内6、7纵行的部分元素可以排在另一区,你认为应排在
(3)随着科学技术的发展,不断有新的元素被发现。若把第七周期排满,则元素周期表共可以排布
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(1)氨硼烷的结构
①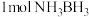 中
中 键的数目为
键的数目为_______ 。
② 熔点104℃,
熔点104℃,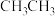 熔点-183.3℃。两者熔点差异较大的原因是
熔点-183.3℃。两者熔点差异较大的原因是_______ 。
(2)氨硼烷水解释氢
①氨硼烷水解释氢需要在金属型催化剂(如 、Pt等)催化下进行。写出基态Fe原子的核外电子排布式:
、Pt等)催化下进行。写出基态Fe原子的核外电子排布式:_______ 。
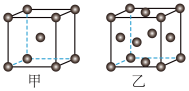
②铁的甲、乙两种晶胞(所示图形为正方体)结构示意如图所示。甲、乙晶胞所含铁原子个数比为_______ 。
③氨硼烷水解释氢时转化为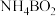 ,写出水解释氢的化学方程式
,写出水解释氢的化学方程式_______ 。
(3)氨硼烷热分解释氢
①氨硼烷受热时固体残留率随温度的变化如图所示。110℃时残留固体的化学式可能为_______ 。
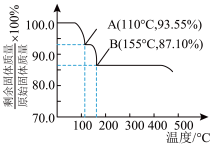
②若B点一种产物的最简式就是分子式,该产物分子中 键∶
键∶ 键=
键=_______ 。
 (氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。| 元素 | H | B | N |
| 电负性 | 2.1 | 2.0 | 3.0 |
①
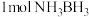 中
中 键的数目为
键的数目为②
 熔点104℃,
熔点104℃,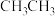 熔点-183.3℃。两者熔点差异较大的原因是
熔点-183.3℃。两者熔点差异较大的原因是(2)氨硼烷水解释氢
①氨硼烷水解释氢需要在金属型催化剂(如
 、Pt等)催化下进行。写出基态Fe原子的核外电子排布式:
、Pt等)催化下进行。写出基态Fe原子的核外电子排布式:②铁的甲、乙两种晶胞(所示图形为正方体)结构示意如图所示。甲、乙晶胞所含铁原子个数比为
③氨硼烷水解释氢时转化为
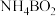 ,写出水解释氢的化学方程式
,写出水解释氢的化学方程式
(3)氨硼烷热分解释氢
①氨硼烷受热时固体残留率随温度的变化如图所示。110℃时残留固体的化学式可能为

②若B点一种产物的最简式就是分子式,该产物分子中
 键∶
键∶ 键=
键=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”“中国紫”颜料。人们对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐( )。回答下列问题:
)。回答下列问题:
(1)基态铜原子的价电子排布式为_______ 。“中国蓝”的发色中心是以 为中心的配位化合物,形成该配位键,
为中心的配位化合物,形成该配位键, 提供
提供_______ ,若“中国蓝”的化学组成中 ,则其化学式为
,则其化学式为_______ 。
(2)Si和C同主族,但 与
与 的熔沸点差异很大,这是因为
的熔沸点差异很大,这是因为 是
是_______ 晶体,而 是
是_______ 晶体。
(3)立方CuO晶胞结构如图所示。其中 的配位数为
的配位数为_______ 。

 )。回答下列问题:
)。回答下列问题:(1)基态铜原子的价电子排布式为
 为中心的配位化合物,形成该配位键,
为中心的配位化合物,形成该配位键, 提供
提供 ,则其化学式为
,则其化学式为(2)Si和C同主族,但
 与
与 的熔沸点差异很大,这是因为
的熔沸点差异很大,这是因为 是
是 是
是(3)立方CuO晶胞结构如图所示。其中
 的配位数为
的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下表为元素周期表的一部分,其中字母代表相应的元素。

试回答下列问题:
(1)元素h的基态原子的核外电子排布式为_______ 。
(2)c、d、e、f元素原子的第一电离能( )由小到大的顺序为
)由小到大的顺序为_______ (用相应元素符号表示)。
(3)表中所列的元素之间可以形成多种化合物,其中邻甲基苯甲醛( )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为_____ 。1mol苯甲醛( )分子中含有σ键的物质的量为
)分子中含有σ键的物质的量为______ mol。
(4)一种由表中元素形成的离子与单质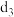 互为等电子体,其离子符号为
互为等电子体,其离子符号为_______ 。

试回答下列问题:
(1)元素h的基态原子的核外电子排布式为
(2)c、d、e、f元素原子的第一电离能(
 )由小到大的顺序为
)由小到大的顺序为(3)表中所列的元素之间可以形成多种化合物,其中邻甲基苯甲醛(
 )分子中碳原子轨道的杂化类型为
)分子中碳原子轨道的杂化类型为 )分子中含有σ键的物质的量为
)分子中含有σ键的物质的量为(4)一种由表中元素形成的离子与单质
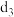 互为等电子体,其离子符号为
互为等电子体,其离子符号为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硼、砷、铁等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是___________ (填标号,下同),用光谱仪可捕捉到发射光谱的是___________ 。___________ 种。CH3As(OH)2与(CH3)2AsOH两种含砷有机酸中沸点较高的是___________ (填化学式),原因为___________ 。
(3)LiZnAs晶体的立方晶胞结构如图1所示,N点原子分数坐标为( ,
, ,
, );LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs,其立方晶胞结构如图2所示。
);LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs,其立方晶胞结构如图2所示。___________ 。
②m=_________
③已知NA为阿伏加德罗常数的值,LiZnmMnnAs的摩尔质量为Mg/mol,晶体密度为dg/cm3。晶胞中As原子与Mn原子之间的最短距离为___________ nm(列出计算式)。
(4)FeSO4·7H2O的结构如图所示。___________ (填序号)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.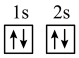 B.
B.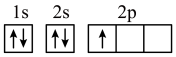
C. D.
D.
(3)LiZnAs晶体的立方晶胞结构如图1所示,N点原子分数坐标为(
 ,
, ,
, );LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs,其立方晶胞结构如图2所示。
);LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体LiZnmMnnAs,其立方晶胞结构如图2所示。
②m=
③已知NA为阿伏加德罗常数的值,LiZnmMnnAs的摩尔质量为Mg/mol,晶体密度为dg/cm3。晶胞中As原子与Mn原子之间的最短距离为
(4)FeSO4·7H2O的结构如图所示。

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
I、2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水,并将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。___________ 。
A.卡通形象中标“+”号的小球表示质子
B.氚的核素符号为
C.氚和及其同位素性质不完全相同
(2)有关 和
和 的说法正确的是___________。
的说法正确的是___________。
(3)已知天然氢元素中:氕的丰度为 ,氘的丰度为
,氘的丰度为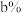 ,氚的丰度为
,氚的丰度为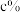 ;氕、氘、氚原子的实际质量分别用
;氕、氘、氚原子的实际质量分别用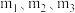 表示,
表示,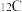 原子的质量用
原子的质量用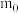 表示。则氢元素的相对原子质量计算表达式为
表示。则氢元素的相对原子质量计算表达式为___________ 。
(4)在离子 中,电子数、质子数和中子数之比为
中,电子数、质子数和中子数之比为___________ 。
II、硼氢化钠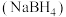 是有机合成中常用的还原剂
是有机合成中常用的还原剂
(5)硼氢化钠中存在的化学键为___________ (填标号)。
a.离子键 b.氢键 c.共价键 d.配位键
(6)已知 的第一电离能大于B的第一电离能,原因为
的第一电离能大于B的第一电离能,原因为___________ 。
(7)___________  的还原能力与标准状况下
的还原能力与标准状况下 的还原能力相当(已知电负性:
的还原能力相当(已知电负性: ;还原能力可用还原剂发生反应时失去电子的物质的量来衡量)。
;还原能力可用还原剂发生反应时失去电子的物质的量来衡量)。
I、2021年4月13日,日本政府召开相关阁僚会议,正式决定向海洋排放福岛第一核电站含有对海洋环境有害的核废水,并将核废水主要辐射物质“氚(T)”做成卡通形象,以合理化将放射性核废水排入太平洋的行为,进而引发国内外民众的严重不满。

A.卡通形象中标“+”号的小球表示质子
B.氚的核素符号为

C.氚和及其同位素性质不完全相同
(2)有关
 和
和 的说法正确的是___________。
的说法正确的是___________。| A.互为同位素 | B.互为同素异形体 |
| C.电子数不同 | D.同温同压下密度之比为 |
 ,氘的丰度为
,氘的丰度为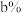 ,氚的丰度为
,氚的丰度为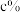 ;氕、氘、氚原子的实际质量分别用
;氕、氘、氚原子的实际质量分别用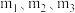 表示,
表示,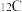 原子的质量用
原子的质量用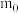 表示。则氢元素的相对原子质量计算表达式为
表示。则氢元素的相对原子质量计算表达式为(4)在离子
 中,电子数、质子数和中子数之比为
中,电子数、质子数和中子数之比为II、硼氢化钠
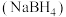 是有机合成中常用的还原剂
是有机合成中常用的还原剂(5)硼氢化钠中存在的化学键为
a.离子键 b.氢键 c.共价键 d.配位键
(6)已知
 的第一电离能大于B的第一电离能,原因为
的第一电离能大于B的第一电离能,原因为(7)
 的还原能力与标准状况下
的还原能力与标准状况下 的还原能力相当(已知电负性:
的还原能力相当(已知电负性: ;还原能力可用还原剂发生反应时失去电子的物质的量来衡量)。
;还原能力可用还原剂发生反应时失去电子的物质的量来衡量)。
您最近一年使用:0次



