根据所学知识,回答下列问题:
(1)下列几种物质,其中属于电解质的是___________ 。(填序号)
① ②CaO ③盐酸 ④KOH ⑤Fe
②CaO ③盐酸 ④KOH ⑤Fe
(2)人们通过焰色试验制造了绚丽多彩的烟花,下列焰色为紫色的是___________ 。(填序号)
a. b.NaCl c.
b.NaCl c.
(3)漂白粉的有效成分为___________ ;在空气中失效的方程式为___________ 。
(4)标准状况下11.2L 气体的质量为
气体的质量为___________ ;与0.1mol  含有相同电子数的
含有相同电子数的 在标状况下的体积为
在标状况下的体积为___________ ;同温同压下,同体积的 和
和 气体的质量比为
气体的质量比为___________ ;同质量的 和
和 中氢原子的个数比为
中氢原子的个数比为___________ ;8.4g  与9.6g某单质
与9.6g某单质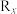 ,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是
,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是___________ ,x值为___________ 。
(5)把标准状况下134.4L HCl气体溶于861mL水中,所得溶液的密度为 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为___________  。
。
(6)硫酸、氨水的密度与所加水量的关系如图所示(水的密度为 ),请根据图中信息,回答下列问题:
),请根据图中信息,回答下列问题: ,则质量分数为a%的氨水物质的量浓度
,则质量分数为a%的氨水物质的量浓度___________ (填“大于”、“小于”或硫酸“等于”)5 ;已知8
;已知8 的硫酸溶液密度为
的硫酸溶液密度为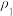 ,4
,4 的硫酸溶液密度为
的硫酸溶液密度为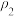 。200g浓度为8
。200g浓度为8 的硫酸溶加水的量
的硫酸溶加水的量___________ mL水混合,使硫酸的物质的量浓度减小到4 。(用含
。(用含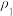 、
、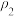 的式子表示)
的式子表示)
(1)下列几种物质,其中属于电解质的是
①
 ②CaO ③盐酸 ④KOH ⑤Fe
②CaO ③盐酸 ④KOH ⑤Fe(2)人们通过焰色试验制造了绚丽多彩的烟花,下列焰色为紫色的是
a.
 b.NaCl c.
b.NaCl c.
(3)漂白粉的有效成分为
(4)标准状况下11.2L
 气体的质量为
气体的质量为 含有相同电子数的
含有相同电子数的 在标状况下的体积为
在标状况下的体积为 和
和 气体的质量比为
气体的质量比为 和
和 中氢原子的个数比为
中氢原子的个数比为 与9.6g某单质
与9.6g某单质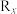 ,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是
,所含原子个数相同,且分子数之比为3∶2,则R的相对原子质量是(5)把标准状况下134.4L HCl气体溶于861mL水中,所得溶液的密度为
 ,则此溶液的物质的量浓度为
,则此溶液的物质的量浓度为 。
。(6)硫酸、氨水的密度与所加水量的关系如图所示(水的密度为
 ),请根据图中信息,回答下列问题:
),请根据图中信息,回答下列问题:
 ,则质量分数为a%的氨水物质的量浓度
,则质量分数为a%的氨水物质的量浓度 ;已知8
;已知8 的硫酸溶液密度为
的硫酸溶液密度为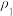 ,4
,4 的硫酸溶液密度为
的硫酸溶液密度为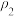 。200g浓度为8
。200g浓度为8 的硫酸溶加水的量
的硫酸溶加水的量 。(用含
。(用含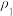 、
、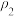 的式子表示)
的式子表示)
更新时间:2024-05-08 08:48:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)向沸水中逐滴滴加适量饱和FeCl3溶液,继续加热至液体呈透明的红褐色,形成该分散系的分散质粒子的直径范围是_______ 。利用_______ 效应,证明该分散系。
(2)①56g氮气在标准状况下的体积为_______ ;密度为_______ 。
②3.9gNa2O2中阴、阳离子的个数比为_______ 。
③现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g, 则此混合气体中,CO2和CO的物质的量之比是_______ 。
(3)阅读下列《高铁酸钾使用说明书》,回答问题:
①K2FeO4中铁元素的化合价为_______ 。
②制备K2FeO4需要在_______ (填“酸性”、“碱性”或“中性”)环境中进行。
③下列关于K2FeO4的说法中,不正确的是_______ 。
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快,安全性好、无异味
④将K2FeO4与水反应的化学方程式补充完整:_______ 。
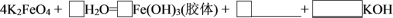
(1)向沸水中逐滴滴加适量饱和FeCl3溶液,继续加热至液体呈透明的红褐色,形成该分散系的分散质粒子的直径范围是
(2)①56g氮气在标准状况下的体积为
②3.9gNa2O2中阴、阳离子的个数比为
③现有标准状况下CO和CO2混合气体6.72L,其质量为11.6g, 则此混合气体中,CO2和CO的物质的量之比是
(3)阅读下列《高铁酸钾使用说明书》,回答问题:
| 高铁酸钾使用说明书 [化学式] K2FeO4 [性状]暗紫色具有金属光泽的粉末,无臭无味 [产品特点]干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气。K2FeO4通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 [用途]主要用于饮用水消毒净化、城市生活污水和工业污水处理 [用量]消毒净化1 L水投放5 mg K2FeO4即可达到卫生标准 |
②制备K2FeO4需要在
③下列关于K2FeO4的说法中,不正确的是
a.是强氧化性的盐
b.固体保存需要防潮
c.其消毒和净化水的原理相同
d.其净水优点有:作用快,安全性好、无异味
④将K2FeO4与水反应的化学方程式补充完整:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)由O2和CH4组成的混合气体,标准状况下的密度为1g/L,则该混合气体中O2和CH4的体积比为___________ 。
(2)已知某硫酸的物质的量浓度为cmol/L,溶质的质量分数为w,溶液的密度为ρg/cm3。如果蒸发溶剂使硫酸的质量分数变为2w,则所得硫酸的物质的量浓度___________ (填“>”、“<”或“=”)2c。
(3)某结晶水合物的化学式为AnH2O,其相对分子质量为M。25℃时,将a克该晶体溶于b克水中恰好可形成Vml饱和溶液。则该饱和溶液中溶质的质量分数为___________ 。该饱和溶液的物质的量浓度为___________ (用含a、M、V的式子表示)。
(4)铁粉能与水蒸气反应,化学方程式为___________ ;若铁粉与一定量水蒸气反应后得到的干燥固体质量比反应前铁粉的质量增加了16g,则参加反应的铁粉质量为___________ 。
(2)已知某硫酸的物质的量浓度为cmol/L,溶质的质量分数为w,溶液的密度为ρg/cm3。如果蒸发溶剂使硫酸的质量分数变为2w,则所得硫酸的物质的量浓度
(3)某结晶水合物的化学式为AnH2O,其相对分子质量为M。25℃时,将a克该晶体溶于b克水中恰好可形成Vml饱和溶液。则该饱和溶液中溶质的质量分数为
(4)铁粉能与水蒸气反应,化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)1个NH4+离子含有________ 个质子,________ 个电子。
(2)2molH3PO4含有___________ 个分子,_________ mol O,_________ 个原子。
(3)含有6.02×1023个H的CH4的物质的量为________ mol。
(4)含有相同氧原子数的CO、CO2、O3的物质的量之比为______________ 。
(5)相同物质的量的SO2和SO3,分子数之比为_________ ;原子数之比为_________ ;电子数之比为_________ 。
(2)2molH3PO4含有
(3)含有6.02×1023个H的CH4的物质的量为
(4)含有相同氧原子数的CO、CO2、O3的物质的量之比为
(5)相同物质的量的SO2和SO3,分子数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】今有九种物质:①铜丝、②CO2、③盐酸、④石灰水、⑤液氨、⑥NaCl固体、⑦乙醇、⑧氯气、⑨液态K2SO4,其中属于化合物的是____________ (填序号,下同),属于混合物的是_______ ,能导电的是__________ ,属于电解质的是___________ ,属于非电解质的是_____________ ,属于电解质但是不能导电的是__________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
I .今有 10 种物质:①Na ②盐酸 ③纯醋酸 ④NH3 ⑤空气 ⑥CO2⑦Fe(OH)3胶体 ⑧NaCl晶体 ⑨BaCO3 ⑩碘酒
(1)能导电的物质___________ 。(用序号填空 ,下同)
(2)电解质,但熔融状态下并不导电___________ 。
(3)强电解质___________ 。
(4)非电解质___________ 。
Ⅱ.请回答:
(5)区分Fe(OH)3胶体和FeCl3溶液实验方法是___________ 。
(6)配平该离子方程式并用双线桥表示电子转移:___________
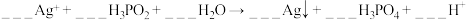
(7)H3PO2是一元弱酸,写出其与足量NaOH 溶液反应的离子方程式:___________ 。
I .今有 10 种物质:①Na ②盐酸 ③纯醋酸 ④NH3 ⑤空气 ⑥CO2⑦Fe(OH)3胶体 ⑧NaCl晶体 ⑨BaCO3 ⑩碘酒
(1)能导电的物质
(2)电解质,但熔融状态下并不导电
(3)强电解质
(4)非电解质
Ⅱ.请回答:
(5)区分Fe(OH)3胶体和FeCl3溶液实验方法是
(6)配平该离子方程式并用双线桥表示电子转移:
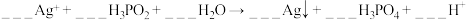
(7)H3PO2是一元弱酸,写出其与足量NaOH 溶液反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请用学过的知识分析其中的化学原理并写出化学方程式,属于离子反应的请写出离子方程式。
(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】_________________________________ 。
(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质__________________________ 。
(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸____________________ 、__________________ 。
(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用_______________ 。
(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:_____________
(1)将氯气通入熟石灰即可制的漂白粉【漂白粉的有效成分是次氯酸钙Ca(ClO)2,商品漂白粉往往含有Ca(OH)2等杂质】
(2)漂白粉之所以具有漂白作用是由于Ca(ClO)2在水溶液中发生水解反应生成具有强氧化性的物质
(3)Ca(OH)2杂质的存在使溶液的碱性增强,因此漂白作用进行缓慢。要在短时间受到漂白效果,必须除去Ca(OH)2,所以工业上使用漂白粉是常加入少量弱酸如醋酸等,或加入少量的稀盐酸
(4)家庭使用漂白粉不必加酸,因为水中的CO2也起到了弱酸的作用
(5)不要将漂白粉与洁厕剂等强酸性物质混合使用,因为在强酸性条件下二者可以发生氧化还原反应生成一种有毒气体:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某学生对SO2与漂粉精的反应进行实验探究:
(1)Cl2和 Ca(OH)2制取漂粉精的化学方程式为_______ 。
(2)pH 试纸颜色的变化说明漂粉精溶液具有的性质是_______ (选填编号)。
A.酸性 B.碱性 C.漂白性
(3)请用化学用语表示SO2通入水中为何溶液呈酸性(用方程式和电离方程式表示)_______ ;_______ 。
(4)现象ii中,黄绿色气体是_______ (写化学式)。资料显示,漂粉精在酸性条件下可发生反应并生成黄绿色气体,写出反应的离子方程式:_______ 。
(5)将A 瓶中混合物过滤、洗涤,得到沉淀X。向沉淀X 中加入稀HCl,无明显变化。取上层清液,加入 BaCl2溶液,产生白色沉淀。则沉淀X 中含有的物质是_______ (写化学式)。
| 操作 | 现象 |
| 取 4g 漂粉精固体,加入 100mL 水 | 部分固体溶解,溶液略有颜色。 |
| 过滤,测漂粉精溶液的pH | pH 试纸:先变蓝(pH约为12),后褪色。 |
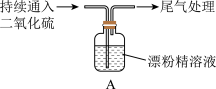 | i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去。 |
(1)Cl2和 Ca(OH)2制取漂粉精的化学方程式为
(2)pH 试纸颜色的变化说明漂粉精溶液具有的性质是
A.酸性 B.碱性 C.漂白性
(3)请用化学用语表示SO2通入水中为何溶液呈酸性(用方程式和电离方程式表示)
(4)现象ii中,黄绿色气体是
(5)将A 瓶中混合物过滤、洗涤,得到沉淀X。向沉淀X 中加入稀HCl,无明显变化。取上层清液,加入 BaCl2溶液,产生白色沉淀。则沉淀X 中含有的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化钠是一种重要的化工原料,用它可以制取日常生活中常使的消毒剂、清洁剂等多种物质,如下图所示。
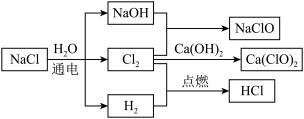
(1)氯元素在周期表中的位置是_______ , 的电子式为
的电子式为_______
(2)下列有关氯气的说法正确的是_______(填字母)。
(3)漂白粉的有效成分是_______ (填化学式);工业上制取漂白粉的化学方程式为_______ 。
(4)曾有报道,因“洁厕灵”(主要成分是盐酸)与“84”消毒液(主要成分是 )混合使用而发生中毒事件,请结合离子方程式分析其原因:
)混合使用而发生中毒事件,请结合离子方程式分析其原因:_______
(5)写出 水溶液通电后发生反应的离子方程式
水溶液通电后发生反应的离子方程式_______

(1)氯元素在周期表中的位置是
 的电子式为
的电子式为(2)下列有关氯气的说法正确的是_______(填字母)。
| A.氯气溶于水只发生化学变化 | B.氯气是黄绿色有毒气体 |
| C.钠在氯气中燃烧产生白烟 | D.将氯气通入鼠洞灭鼠,利用的是氯气易液化和有毒性的性质 |
(4)曾有报道,因“洁厕灵”(主要成分是盐酸)与“84”消毒液(主要成分是
 )混合使用而发生中毒事件,请结合离子方程式分析其原因:
)混合使用而发生中毒事件,请结合离子方程式分析其原因:(5)写出
 水溶液通电后发生反应的离子方程式
水溶液通电后发生反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求回答下列问题。
(1)下列各组微粒:① 与
与 ;②
;② 和
和 ;③H、D、T;④金刚石和石墨;⑤
;③H、D、T;④金刚石和石墨;⑤ 和
和 ;⑥
;⑥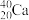 和
和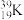 。互为同位素的是
。互为同位素的是___________ (填序号),透过蓝色钴玻璃观察K元素燃烧时的焰色为___________ 色。
(2)苯与浓硫酸、浓硝酸在55℃~60℃时反应的化学方程式为___________ 。
(3)现有如下三个反应:
A.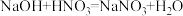
B.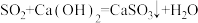
C.
根据三个反应本质,能设计成原电池的是___________ (填“A”、“B”或“C”)。该原电池的负极材料为___________ ,若导线上转移电子0.6mol,则电极减少的质量是___________ g。
(1)下列各组微粒:①
 与
与 ;②
;② 和
和 ;③H、D、T;④金刚石和石墨;⑤
;③H、D、T;④金刚石和石墨;⑤ 和
和 ;⑥
;⑥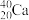 和
和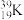 。互为同位素的是
。互为同位素的是(2)苯与浓硫酸、浓硝酸在55℃~60℃时反应的化学方程式为
(3)现有如下三个反应:
A.
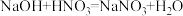
B.
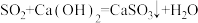
C.

根据三个反应本质,能设计成原电池的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】汽车的方向盘和前排乘客座位前的仪表板内都有折叠安全气囊,该安全气囊中含有叠氮化钠( )、硝酸钾(
)、硝酸钾( )、二氧化硅(
)、二氧化硅( )粉等。完成下列填空:
)粉等。完成下列填空:
(1)关于 ,下列分析正确的是_______。
,下列分析正确的是_______。
(2)行驶的汽车发生有足够强度的意外碰撞时,碰撞传感器将激活特定的电路,放电使 迅速分解,生成Na并放出
迅速分解,生成Na并放出 ,写出
,写出 分解的化学方程式
分解的化学方程式_______ 。
(3)生成的Na与 发生二次反应:
发生二次反应: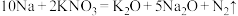 ,标出上式的单线桥:
,标出上式的单线桥:_______ ,其中生成2个氮气分子时,转移_______ 个电子,该反应的还原剂与氧化剂的个数比为_______ 。
 )、硝酸钾(
)、硝酸钾( )、二氧化硅(
)、二氧化硅( )粉等。完成下列填空:
)粉等。完成下列填空:(1)关于
 ,下列分析正确的是_______。
,下列分析正确的是_______。A. 电离需要通电 电离需要通电 |
B. 的焰色反应为蓝色 的焰色反应为蓝色 |
C.熔融状态的 中含自由移动的 中含自由移动的 和 和 |
D.固态 不导电,因其中不含 不导电,因其中不含 和 和 |
 迅速分解,生成Na并放出
迅速分解,生成Na并放出 ,写出
,写出 分解的化学方程式
分解的化学方程式(3)生成的Na与
 发生二次反应:
发生二次反应: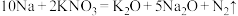 ,标出上式的单线桥:
,标出上式的单线桥:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)生石灰可作食品干燥剂,它属于___________ (填“碱”、“盐”或“氧化物”)。
(2)将食品袋中的抗氧化剂还原铁粉投入食醋中,发现产生大量气泡,溶液变为浅绿色。请写出发生反应的离子方程式___________ 。
(3)洪涝灾害后,加入KAl(SO4)2·12H2O可使浑浊的水变澄清,该物质俗名为___________ ,因其溶于水生成___________ (化学式)而具有净水作用。
(4)铝粉和氢氧化钠混合物可用作下水道疏通剂,其主要原因为___________ (用化学方程式表示)。
(5)炒菜时,食盐不慎撒落在天然气火焰上,可能看到的现象为:___________ 。
(1)生石灰可作食品干燥剂,它属于
(2)将食品袋中的抗氧化剂还原铁粉投入食醋中,发现产生大量气泡,溶液变为浅绿色。请写出发生反应的离子方程式
(3)洪涝灾害后,加入KAl(SO4)2·12H2O可使浑浊的水变澄清,该物质俗名为
(4)铝粉和氢氧化钠混合物可用作下水道疏通剂,其主要原因为
(5)炒菜时,食盐不慎撒落在天然气火焰上,可能看到的现象为:
您最近一年使用:0次

 );④
);④ ;⑤
;⑤ 固体;⑥
固体;⑥ 固体;⑦蔗糖;⑧氨水;⑨稀硝酸;⑩
固体;⑦蔗糖;⑧氨水;⑨稀硝酸;⑩ 固体。
固体。 ,写出该离子反应对应的化学方程式
,写出该离子反应对应的化学方程式

