某学生对SO2与漂粉精的反应进行实验探究:
(1)Cl2和 Ca(OH)2制取漂粉精的化学方程式为_______ 。
(2)pH 试纸颜色的变化说明漂粉精溶液具有的性质是_______ (选填编号)。
A.酸性 B.碱性 C.漂白性
(3)请用化学用语表示SO2通入水中为何溶液呈酸性(用方程式和电离方程式表示)_______ ;_______ 。
(4)现象ii中,黄绿色气体是_______ (写化学式)。资料显示,漂粉精在酸性条件下可发生反应并生成黄绿色气体,写出反应的离子方程式:_______ 。
(5)将A 瓶中混合物过滤、洗涤,得到沉淀X。向沉淀X 中加入稀HCl,无明显变化。取上层清液,加入 BaCl2溶液,产生白色沉淀。则沉淀X 中含有的物质是_______ (写化学式)。
| 操作 | 现象 |
| 取 4g 漂粉精固体,加入 100mL 水 | 部分固体溶解,溶液略有颜色。 |
| 过滤,测漂粉精溶液的pH | pH 试纸:先变蓝(pH约为12),后褪色。 |
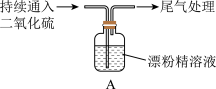 | i.液面上方出现白雾; ii.稍后,出现浑浊,溶液变为黄绿色; iii.稍后,产生大量白色沉淀,黄绿色褪去。 |
(1)Cl2和 Ca(OH)2制取漂粉精的化学方程式为
(2)pH 试纸颜色的变化说明漂粉精溶液具有的性质是
A.酸性 B.碱性 C.漂白性
(3)请用化学用语表示SO2通入水中为何溶液呈酸性(用方程式和电离方程式表示)
(4)现象ii中,黄绿色气体是
(5)将A 瓶中混合物过滤、洗涤,得到沉淀X。向沉淀X 中加入稀HCl,无明显变化。取上层清液,加入 BaCl2溶液,产生白色沉淀。则沉淀X 中含有的物质是
更新时间:2023-01-04 23:53:01
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)很多含氯物质都能做消毒剂。液氯可以用于饮用水消毒,但是消毒后的水中可能产生危害人体健康的有机氯化物。世界各国陆续开发新型自来水消毒剂,下列物质可以用于自来水消毒的有___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是___ (写出化学式)。高铁酸钠(Na2FeO4)也可以用于作自来水处理剂,高铁酸钠处理过的水中含有氢氧化铁胶体,则高铁酸钠作自来水处理剂的优点是___ 。
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:___ 。
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯= ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯=
 ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】漂白液、漂白粉和漂粉精既可作漂白棉、麻、纸张的漂白剂,又可用作游泳池及环境的消毒剂。
(1)在常温下,将氯气通入NaOH溶液中制取漂白液的化学方程式为:______ 。
(2)漂白粉或漂粉精的有效成分是______ ,使用漂白粉或漂粉精时通常要加入少量的水并通入CO2,此操作方法的目的是:______ 。
(1)在常温下,将氯气通入NaOH溶液中制取漂白液的化学方程式为:
(2)漂白粉或漂粉精的有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaCl是一种化工原料,可以制备多种物质,如下图所示。
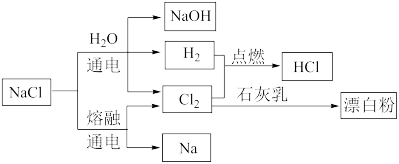
回答问题:
(1)氯化钠溶液通电后,发生反应的离子方程式为_____ ,氢气在氯气中燃烧的现象是_____ 。
(2)氯气通入石灰乳中制取漂白粉的离子方程式为_____ ,从氧化剂、还原剂的角度分析,该反应中氯气的作用是____ 。
(3)漂白粉的有效成分是_____ (填化学式),漂白粉久置于空气中会变质,用化学方程式描述其变质的原因____ 。

回答问题:
(1)氯化钠溶液通电后,发生反应的离子方程式为
(2)氯气通入石灰乳中制取漂白粉的离子方程式为
(3)漂白粉的有效成分是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】化学基本概念是学习化学的基石,请正确回答下列问题。
(1)①写出NaHCO3的俗名:_______ ;
②Fe2O3俗称:_______
③写出工业制漂白粉化学方程式:_______ ,并指出漂白粉的有效成分:_______ 。
④写出氯化铁溶液腐蚀铜箔的离子方程式,并用单线桥标出电子转移方向和数目:_______ 。
(2)今有6种物质:①NaCl溶液;②Cu;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;⑥干冰。属于电解质的是_______ ;属于非电解质的是_______ ;能导电的是_______ 。
(3)标准状况下11.2LNH3中含_______ 个氨分子;12.4gNa2R含Na+0.4mol,则Na2R的摩尔质量为_______ 。
(1)①写出NaHCO3的俗名:
②Fe2O3俗称:
③写出工业制漂白粉化学方程式:
④写出氯化铁溶液腐蚀铜箔的离子方程式,并用单线桥标出电子转移方向和数目:
(2)今有6种物质:①NaCl溶液;②Cu;③乙醇(C2H5OH);④熔融的KNO3;⑤BaSO4固体;⑥干冰。属于电解质的是
(3)标准状况下11.2LNH3中含
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知铜和浓硫酸可以在加热条件下发生反应(已配平): 。试通过计算和推理完成下面的问题
。试通过计算和推理完成下面的问题
(1)此反应中,硫酸体现了___________ 性和___________ 性。
(2)A物质可以导致酸雨的形成。A应该属于___________ 。(用字母代号填写)
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)___________ 失去电子,氧化剂是___________ 。
 。试通过计算和推理完成下面的问题
。试通过计算和推理完成下面的问题(1)此反应中,硫酸体现了
(2)A物质可以导致酸雨的形成。A应该属于
a.酸 b.碱 c.盐 d.酸性氧化物 e.碱性氧化物
(3)A可使紫红色的酸性KMnO4溶液褪色,此褪色反应中(填写化学式,下同)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为___________ 。
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是___________ (填化学式)。排放的尾气中含量较高的氮氧化物是___________ (填化学式)。
(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:

①尿素[CO(NH2)2]中氮元素的化合价为___________ 。
②写出“催化反应”过程中NH3还原NO2的化学方程式___________ 。
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程___________ 。
④“催化反应”过程中需控制温度在250℃~380℃之间。温度过高,NH3发生催化氧化反应,写出该化学方程式___________ 。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含NO、NO2),获得副产品NaNO2。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到NaNO2晶体中最有可能混有的杂质是
(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:

①尿素[CO(NH2)2]中氮元素的化合价为
②写出“催化反应”过程中NH3还原NO2的化学方程式
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程
④“催化反应”过程中需控制温度在250℃~380℃之间。温度过高,NH3发生催化氧化反应,写出该化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如下图所示,将甲、乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(气体体积在同温同压下测定)。试回答问题:
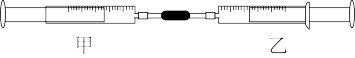
(1)实验1中发生反应的离子方程式为:___________ 。
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入___________ 溶液中。
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式___________ ,写出检验所得白色固体中阳离子的操作方法:___________ ,充分反应后甲针筒内剩余气体成分为___________ (填化学式)。

| 实验序号 | 甲针筒内物质 | 乙针筒内物质 |
| 1 | 溴水 | SO2 |
| 2 | H2S | SO2 |
| 3 | 15mLCl2 | 35mLNH3 |
(2)实验2反应后甲针筒内有少量的残留气体,正确的处理方法是将其通入
(3)实验3中能看见有白烟产生并生成一种气体(空气主要成分之一),该化学反应方程式
您最近一年使用:0次



