(1)很多含氯物质都能做消毒剂。液氯可以用于饮用水消毒,但是消毒后的水中可能产生危害人体健康的有机氯化物。世界各国陆续开发新型自来水消毒剂,下列物质可以用于自来水消毒的有___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是___ (写出化学式)。高铁酸钠(Na2FeO4)也可以用于作自来水处理剂,高铁酸钠处理过的水中含有氢氧化铁胶体,则高铁酸钠作自来水处理剂的优点是___ 。
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:___ 。
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯= ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯=
 ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
更新时间:2021-02-05 20:33:51
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)请完成并配平如下化学方程式,再用双线桥法表示该氧化还原反应电子转移的方向和数目:________
_____ ________
________ ________
________ ________
________ ________
________
(2)NaH可在野外作生氢剂。反应原理为 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为________ 。
(3)工业废水中的 有毒,常在酸性条件下用
有毒,常在酸性条件下用 做处理剂,将
做处理剂,将 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为________ 。
(4)某一反应体系中有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 中发生的过程为
中发生的过程为 。
。
①该反应中,发生还原反应的过程是________ →________ 。
②写出该反应的化学方程或(配平)________ 。
(1)请完成并配平如下化学方程式,再用双线桥法表示该氧化还原反应电子转移的方向和数目:
_____
 ________
________ ________
________ ________
________ ________
________
(2)NaH可在野外作生氢剂。反应原理为
 ,该反应中氧化产物和还原产物的质量比为
,该反应中氧化产物和还原产物的质量比为(3)工业废水中的
 有毒,常在酸性条件下用
有毒,常在酸性条件下用 做处理剂,将
做处理剂,将 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为(4)某一反应体系中有反应物和生成物共五种物质:
 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 中发生的过程为
中发生的过程为 。
。①该反应中,发生还原反应的过程是
②写出该反应的化学方程或(配平)
您最近一年使用:0次
填空题
|
适中
(0.65)
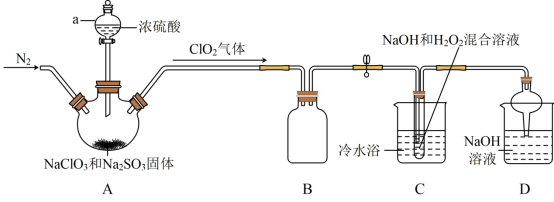
【推荐2】二氧化氯(ClO2)与亚氯酸钠(NaClO2)都具有强氧化性。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组利用如图装置由二氧化氯制备NaClO2·3H2O,并探究其性质。
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2 =
=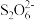 +2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
+2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现_______ (填实验现象),达到滴定终点,共消耗该标准溶液25.00mL,经计算该试样中NaClO2·3H2O的百分含量为_______ (结果保留3位有效数字)。
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2
 =
=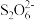 +2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
+2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在盛有淀粉KI溶液的试管中,滴加少量的NaClO溶液和稀H2SO4,会立即看到溶液变为蓝色,这是因为_______________ ,相应的离子方程式为__________ 在盛有淀粉和碘水的混合液中,滴加Na2SO3溶液,发现____________ 现象,这是因为_________ ,其离子方程式为______________________ ,对于上述两组实验的结果,可得出:ClO-、I2、SO42-的氧化性强弱顺序为_____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学与人类生活密切相关。请按要求,回答下列问题:
(1)漂白粉有效成分的化学式为______ ;其能消毒杀菌是因有强_________ 性。
(2)KAl(SO4)2·12H2O的俗名为_______ ,因其溶于水生成_______ 具有净水作用。
(3)新制氯水在阳光照射下产生的无色气体该反应的化学方程式是_____________ 。
(4)小苏打的化学式为__________ ,可用于治疗胃酸过多,其反应的离子方程式为_______ 。
(1)漂白粉有效成分的化学式为
(2)KAl(SO4)2·12H2O的俗名为
(3)新制氯水在阳光照射下产生的无色气体该反应的化学方程式是
(4)小苏打的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)酸雨的pH小于______________ 。
(2)漂白粉有效成分的化学式为______________ ,其能消毒杀菌是因有强_________ 性。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_____________ 。
⑷KA1(SO4)2 • 12H2O的俗名为_________ ,因其溶于水生成______________ (化学式)而具有净水作用。
(5)向一铝制易拉罐中充满CO2后,再往罐中注入足量的质量分数为20%的NaOH溶液,立即严封罐口,不—会儿就发现易拉罐变瘪,再过一会易拉罐又鼓胀起来,解释上述实验现象,易拉罐又鼓胀起来的原因是________________ (用化学方程式表示)。
(1)酸雨的pH小于
(2)漂白粉有效成分的化学式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
⑷KA1(SO4)2 • 12H2O的俗名为
(5)向一铝制易拉罐中充满CO2后,再往罐中注入足量的质量分数为20%的NaOH溶液,立即严封罐口,不—会儿就发现易拉罐变瘪,再过一会易拉罐又鼓胀起来,解释上述实验现象,易拉罐又鼓胀起来的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)实验室制取氯气反应的离子方程式为_________________________
(2)工业上制取漂白粉反应的化学方程式为_________________________
(3)配平:____ KClO3+____ H2C2O4+____ H2SO4→_____ K2SO4+____ ClO2↑+_____ CO2↑+_____ H2O
(4)二氧化碳气体通过一定量的过氧化钠固体,固体增重2.8g时,放出热量为Q KJ
则此反应的热化学方程式为_________________________
(5)标况下3.136 L Cl2通入0.1 L FeBr2溶液中,测得溶液Br-中消耗了三分之二,则此时总反应的离子方程式为_________________________
(2)工业上制取漂白粉反应的化学方程式为
(3)配平:
(4)二氧化碳气体通过一定量的过氧化钠固体,固体增重2.8g时,放出热量为Q KJ
则此反应的热化学方程式为
(5)标况下3.136 L Cl2通入0.1 L FeBr2溶液中,测得溶液Br-中消耗了三分之二,则此时总反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】合成与开发大量自然界并不存在的新物质、新材料,并为人类服务是现代化学的重要任务。请结合所学知识回答下列问题:
(1)沙滩上沙粒的主要成分是____ 。工业上可用沙粒的主要成分与纯碱在高温下反应制备Na2SiO3,该反应的化学方程式为____ 。
(2)氯气溶于水能杀菌消毒,在新制氯水中滴入紫色石蕊试液的现象是___ ,该现象说明氯水中含有_______ (填化学式或离子符号)。
(3)直接用氯气作漂白剂,难以保存,效果不理想。经过多年的实验、改进,目前常用的是漂白粉。工业制取漂白粉的化学方程式为__ 。
(1)沙滩上沙粒的主要成分是
(2)氯气溶于水能杀菌消毒,在新制氯水中滴入紫色石蕊试液的现象是
(3)直接用氯气作漂白剂,难以保存,效果不理想。经过多年的实验、改进,目前常用的是漂白粉。工业制取漂白粉的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】写出下列反应化学方程式
1、重氢形成的盐酸和碳酸钙反应__________________________________
2、漂白粉露置在空气中变质______________________________________
3、电解饱和食盐水______________________________________________
4、次氯酸的不稳定性____________________________________________
5、适量的氯气与碘化钠溶液反应__________________________________
1、重氢形成的盐酸和碳酸钙反应
2、漂白粉露置在空气中变质
3、电解饱和食盐水
4、次氯酸的不稳定性
5、适量的氯气与碘化钠溶液反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 + 3Cl2 +10KOH 2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是
2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是____________ ,当反应中有1mol K2FeO4生成时,消耗的Cl2在标况下的体积为____________ L,转移电子的数目为____________ 。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:_____________________________________________ 。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:_____ 。
(4)工业上制漂白粉的化学方程式为________________________________ ,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是_________________________ 。
(5)KAl(SO4)2·12H2O因其溶于水生成_____ (化学式)可以吸附杂质,从而达到净水作用。
(6)硅酸钠水溶液的俗名为__________ ,可作为木材_______________ 的原料。
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3 + 3Cl2 +10KOH
 2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是
2 K2FeO4 + 6KCl +8H2O在该反应中,还原剂是(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(4)工业上制漂白粉的化学方程式为
(5)KAl(SO4)2·12H2O因其溶于水生成
(6)硅酸钠水溶液的俗名为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁是应用最广泛的金属,铁的卤化物、氧化物、氢氧化物以及高价铁的含氧酸盐均为重要化合物。如图是铁及其化合物的“价一类”二维图。回答下列问题:

(1)在高温下,甲与水蒸气反应的化学方程式为___________ 。
(2)若戊为硫酸盐,缺铁性贫血往往口服戊,当用戊制成药片时,外表包有一层特殊的糖衣,其作用是防止___________ 。
(3)铁元素的高价铁盐 可以做杀毒剂和净水剂,原因是
可以做杀毒剂和净水剂,原因是___________ 。
(4)若己为氯化物,工业上还可以用己溶液来腐蚀印刷电路板上的铜,向反应所得的溶液中加入一定量的锌粉充分反应后,从理论上分析,下列说法合理的是___________ (填字母)。
a.若无固体剩余,则溶液中可能含有 、
、 、
、 、
、 四种离子
四种离子
b.若溶液中有 ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余
c.若有固体剩余,则溶液中一定有反应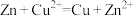 发生
发生
d.当溶液中有 存在时,则一定没有Cu析出
存在时,则一定没有Cu析出

(1)在高温下,甲与水蒸气反应的化学方程式为
(2)若戊为硫酸盐,缺铁性贫血往往口服戊,当用戊制成药片时,外表包有一层特殊的糖衣,其作用是防止
(3)铁元素的高价铁盐
 可以做杀毒剂和净水剂,原因是
可以做杀毒剂和净水剂,原因是(4)若己为氯化物,工业上还可以用己溶液来腐蚀印刷电路板上的铜,向反应所得的溶液中加入一定量的锌粉充分反应后,从理论上分析,下列说法合理的是
a.若无固体剩余,则溶液中可能含有
 、
、 、
、 、
、 四种离子
四种离子b.若溶液中有
 ,则体系中一定没有固体剩余
,则体系中一定没有固体剩余c.若有固体剩余,则溶液中一定有反应
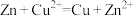 发生
发生d.当溶液中有
 存在时,则一定没有Cu析出
存在时,则一定没有Cu析出
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中O2是(填氧化产物或还原产物)_ 。
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O
、Cl-、H2O
①碱性条件下,氧化剂和还原剂按照物质的量的比为_____ 发生反应。
②上述反应方程式配平后H2O的系数为_____ 。
(3)低温下向高铁酸钠溶液中加入KOH至饱和析出高铁酸钾的化学方程式为_______ 。
II.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-,离子的还原性顺序为:I->Fe2+>Br->Cl-。
(4)含有1molFeI2和2molFeBr2的溶液中通入2molCl2,此时被氧化的离子是______ 。
(5)向含amolFeI2和bmolFeBr2的溶液中通入cmolCl2,当I-、Fe2+、Br-恰好完全被氧化时,c=____ (用含a、b的代数式表示)
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中O2是(填氧化产物或还原产物)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O
、Cl-、H2O①碱性条件下,氧化剂和还原剂按照物质的量的比为
②上述反应方程式配平后H2O的系数为
(3)低温下向高铁酸钠溶液中加入KOH至饱和析出高铁酸钾的化学方程式为
II.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-,离子的还原性顺序为:I->Fe2+>Br->Cl-。
(4)含有1molFeI2和2molFeBr2的溶液中通入2molCl2,此时被氧化的离子是
(5)向含amolFeI2和bmolFeBr2的溶液中通入cmolCl2,当I-、Fe2+、Br-恰好完全被氧化时,c=
您最近一年使用:0次

 溶液;⑥铜;⑦蔗糖;⑧熔融
溶液;⑥铜;⑦蔗糖;⑧熔融 ,其中能导电的是
,其中能导电的是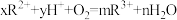 的离子方程式中,下列判断正确的是___________;
的离子方程式中,下列判断正确的是___________; ,
, 是还原剂
是还原剂 ,
, 被氧化
被氧化 ,
, ,
, 的
的 溶液30mL恰好将
溶液30mL恰好将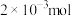 的
的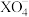 还原,则元素X在还原产物中的化合价是
还原,则元素X在还原产物中的化合价是

