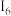如图是元素周期表的一部分,表中所列字母分别代表一种元素.
试回答下列问题:
(1)以上元素中,属于d区元素的是________ (填元素符号),h在周期表的位置是_________ 。
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为______________ 。
(3)元素k的基态原子电子排布式为__________ ;画出c的核外电子排布图:_____________ 。
(4)元素c的电负性______ 元素g的电负性(填“>”、“=”、“<”),元素b、c、e的第一电离能由大到小的顺序是___________________ (用元素符号表示)。
(5)工业上冶炼g元素的单质的化学方程式_______________________________ ,f、 h两种元素最高价氧化物对应的水化物反应的化学方程式是___________________ 。
试回答下列问题:
(1)以上元素中,属于d区元素的是
(2)由e、f以原子个数1∶1形成的晶体中,化学键类型为
(3)元素k的基态原子电子排布式为
(4)元素c的电负性
(5)工业上冶炼g元素的单质的化学方程式
更新时间:2018-10-26 12:25:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下图为元素周期表的一部分,请参照元素①~⑦在表中的位置,回答下列问题:

(1)元素⑥在周期表中的位置是___________ 。
(2)③④⑤的简单离子半径由大到小的顺序为___________ (用离子符号和“>”表示)。
(3)④和⑦形成的化合物中含有化学键类型为___________ 。
(4)④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物发生反应的离子方程式为___________ 。

(1)元素⑥在周期表中的位置是
(2)③④⑤的简单离子半径由大到小的顺序为
(3)④和⑦形成的化合物中含有化学键类型为
(4)④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:第________ 周期________ 族。
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为_______________ 。
(3)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:________________ 。
(4)写出3p轨道上有2个未成对电子的元素的符号:____________ 。
(5)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为________ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:第
(2)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为
(3)写出原子序数最小的第Ⅷ族元素原子的核外电子排布式:
(4)写出3p轨道上有2个未成对电子的元素的符号:
(5)日常生活中广泛使用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素②的原子结构示意图是___________ ,形成化合物种类最多的元素是___________ 。(填元素符号)
(2)元素⑨在周期表中所处位置___________ ,从元素原子得失电子的角度看,元素⑨具有___________ (填“氧化性”或“还原性”)。
(3)元素③与元素⑤形成原子个数比为1:1的化合物的电子式为___________ ,该化合物中存在的化学键类型有___________ 、___________ 。
(4)第三周期元素除⑩外原子半径最大的是___________ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),具有两性的是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是___________ 。(填离子符号)
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)元素⑨在周期表中所处位置
(3)元素③与元素⑤形成原子个数比为1:1的化合物的电子式为
(4)第三周期元素除⑩外原子半径最大的是
(5)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下表数据是Na、Mg、Al三种元素的原子逐级失去电子的电离能( ):
):
根据表中数据判断,元素②是__________ 。
(2)Na、Mg、Al的化学活动性依次减弱,试从化学键角度解释其原因__________ 。
(3)基态Al原子转化为下列激发态时,吸收能量最少的是__________(填标号)。
(4)AlCl,为l共价化合物,蒸汽状态下以双聚分子 形式存在,所有原子均满足8电子稳定结构,其结构式为
形式存在,所有原子均满足8电子稳定结构,其结构式为__________ (用“→”表示出分子中的配位键),其中Al的配位数为__________ 。
(5)元素硼(B)和镓(Ga)和铝同族,分别与铝处于相邻周期。已知硼酸(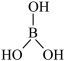 )为一元弱酸,与强碱反应的离子方程式为
)为一元弱酸,与强碱反应的离子方程式为 。在
。在 和
和 中B原子的杂化轨道类型分别为
中B原子的杂化轨道类型分别为__________ 、__________ 。
(6)基态Ga原子的核外电子排布式为[Ar]__________ 。
(7)根据元素周期律分析,
__________ (填序号)。
①只能与强酸反应 ②只能与强碱反应 ③既能与强酸反应,又能与强碱反应
(1)下表数据是Na、Mg、Al三种元素的原子逐级失去电子的电离能(
 ):
):
|
|
|
|
|
| …… | |
元素① | 496 | 4562 | 6912 | 9543 | 13353 | 16610 | …… |
元素② | 577 | 1817 | 2745 | 11575 | 14830 | 18376 | …… |
元素③ | 738 | 1451 | 7733 | 10540 | 13630 | 17995 | …… |
(2)Na、Mg、Al的化学活动性依次减弱,试从化学键角度解释其原因
(3)基态Al原子转化为下列激发态时,吸收能量最少的是__________(填标号)。
A.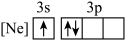 | B.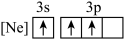 |
C.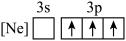 | D.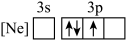 |
(4)AlCl,为l共价化合物,蒸汽状态下以双聚分子
 形式存在,所有原子均满足8电子稳定结构,其结构式为
形式存在,所有原子均满足8电子稳定结构,其结构式为(5)元素硼(B)和镓(Ga)和铝同族,分别与铝处于相邻周期。已知硼酸(
 )为一元弱酸,与强碱反应的离子方程式为
)为一元弱酸,与强碱反应的离子方程式为 。在
。在 和
和 中B原子的杂化轨道类型分别为
中B原子的杂化轨道类型分别为(6)基态Ga原子的核外电子排布式为[Ar]
(7)根据元素周期律分析,

①只能与强酸反应 ②只能与强碱反应 ③既能与强酸反应,又能与强碱反应
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铜、镁、钙、锡及其化合物有许多用途。CuSO4和Cu(NO3)2中阳离子基态核外电子排布式为___________ ,S、O、 N三种元素的第一电离能由大到小的顺序为___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
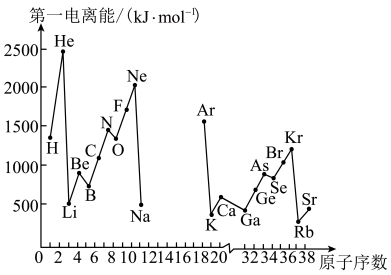
(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为____ <Al<__ ;(填元素符号)
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是_____ 。
(3)上图中第一电离能最小的元素在周期表中的位置是第________ 周期________ 族;

(1)认真分析上图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
(2)从上图分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)上图中第一电离能最小的元素在周期表中的位置是第
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】以下元素均为第4周期元素,请回答相关问题。
(1)钾、锰分别位于___________ 族、___________ 族。
(2)基态铁原子的电子排布式为___________ 。
(3)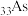 、
、 、
、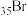 三种非金属元素的电负性由大到小的顺序为
三种非金属元素的电负性由大到小的顺序为___________ ;Br可与第三周期Cl元素形成化合物BrCl,其中显正价的元素为___________ ,原因是___________ 。
(1)钾、锰分别位于
(2)基态铁原子的电子排布式为
(3)
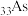 、
、 、
、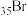 三种非金属元素的电负性由大到小的顺序为
三种非金属元素的电负性由大到小的顺序为
您最近一年使用:0次
【推荐2】富马酸亚铁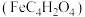 是一种补铁剂。富马酸分子的结构模型如图所示:
是一种补铁剂。富马酸分子的结构模型如图所示:
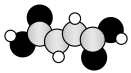
(1)富马酸分子中 键与
键与 键的数目比为
键的数目比为_______ ;
(2)富马酸亚铁中各元素的电负性由大到小的顺序为_______ 。
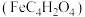 是一种补铁剂。富马酸分子的结构模型如图所示:
是一种补铁剂。富马酸分子的结构模型如图所示:
(1)富马酸分子中
 键与
键与 键的数目比为
键的数目比为(2)富马酸亚铁中各元素的电负性由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】李灿院士团队研发的“液态阳光”计划是通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)H、C、N的电负性由大到小的顺序为___________
(2)基态C原子中电子占据最高能级的符号是___________ ,核外电子的空间运动状态有___________ 种,成对电子数与未成对电子数之比为___________ 。
(3)甲醇(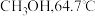 )的沸点比甲硫醇(
)的沸点比甲硫醇(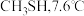 )的高,原因是
)的高,原因是___________ 。
(4)太阳能电池板主要材料为 的晶体。
的晶体。 是生产高纯
是生产高纯 的前驱体,
的前驱体, 可发生水解反应,机理如下:
可发生水解反应,机理如下:
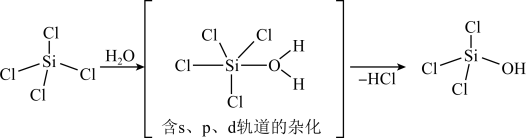
含s、p、d轨道的杂化类型有:① 、②
、② 、③
、③ ,中间体
,中间体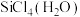 中
中 采取的杂化类型为
采取的杂化类型为___________ (填标号)。
(1)H、C、N的电负性由大到小的顺序为
(2)基态C原子中电子占据最高能级的符号是
(3)甲醇(
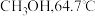 )的沸点比甲硫醇(
)的沸点比甲硫醇(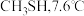 )的高,原因是
)的高,原因是(4)太阳能电池板主要材料为
 的晶体。
的晶体。 是生产高纯
是生产高纯 的前驱体,
的前驱体, 可发生水解反应,机理如下:
可发生水解反应,机理如下:
含s、p、d轨道的杂化类型有:①
 、②
、② 、③
、③ ,中间体
,中间体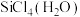 中
中 采取的杂化类型为
采取的杂化类型为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.S4N4的结构如图:
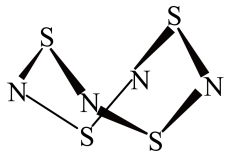
(1)S4N4的晶体类型是__________ 。
(2)用干燥的氨作用于S2Cl2的CCl4,溶液中可制S4N4。化学反应方程为:6S2Cl2+16NH3= S4N4 +S8+12NH4Cl
①上述反应过程中,没有破坏或形成的微粒间作用力是_____ 。
a.离子键 b.极性键 c.非极性键 d.金属键 e.配位键 f.范德华力
②S2Cl2中,S原子轨道的杂化类型是_________ 。
II.二甘氨酸合铜(II)是最早被发现的电中性内配盐,它的结构如图:

(3)基态Cu2+的最外层电子排布式为_______________ 。
(4)二甘氨酸合铜(II)中,第一电离能最大的元素与电负性最小的非金属元素可形成多种微粒,其中一种是5核10电子的微粒,该微粒的空间构型是__________________ 。
(5)lmol二甘氨酸合铜(II)含有的二键数目是______ 。
(6)二甘氨酸合铜(II)结构中,与铜形成的化学键中一定属于配位键的是________ (填写编号)。

(1)S4N4的晶体类型是
(2)用干燥的氨作用于S2Cl2的CCl4,溶液中可制S4N4。化学反应方程为:6S2Cl2+16NH3= S4N4 +S8+12NH4Cl
①上述反应过程中,没有破坏或形成的微粒间作用力是
a.离子键 b.极性键 c.非极性键 d.金属键 e.配位键 f.范德华力
②S2Cl2中,S原子轨道的杂化类型是
II.二甘氨酸合铜(II)是最早被发现的电中性内配盐,它的结构如图:

(3)基态Cu2+的最外层电子排布式为
(4)二甘氨酸合铜(II)中,第一电离能最大的元素与电负性最小的非金属元素可形成多种微粒,其中一种是5核10电子的微粒,该微粒的空间构型是
(5)lmol二甘氨酸合铜(II)含有的二键数目是
(6)二甘氨酸合铜(II)结构中,与铜形成的化学键中一定属于配位键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题。
(1)基态N原子的电子排布式为___________ 。基态P原子中,电子占据的最高能级原子轨道形状为___________ 。
(2)H2O中心原子杂化轨道类型为___________ ,说明H2O沸点大于H2S的原因___________ 。
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为___________ (填“发射”或“吸收”)光谱。
(4)下列氧原子电子排布图表示的状态中,能量最高的是___________ (填标号,下同),能量最低的是___________ 。
A.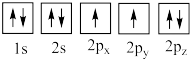 B.
B.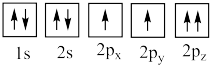
C. D.
D.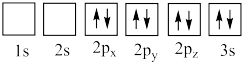
(1)基态N原子的电子排布式为
(2)H2O中心原子杂化轨道类型为
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为
(4)下列氧原子电子排布图表示的状态中,能量最高的是
A.
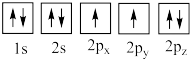 B.
B.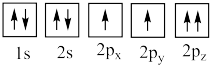
C.
 D.
D.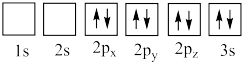
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B、C、D为短周期主族元素并且原子序数依次增大,其中只有A、B、C在同一周期。A元素原子核外成对电子数是未成对电子数的2倍;B元素最外层有3个未成对电子;C元素核外有3对成对电子;D元素是所在周期中原子半径最小的;E元素位于周期表的第四周期第九列。请根据相关信息,应化学用语回答下列问题:
(1)A的基态原子核中核外有___ 种运动状态不同的电子;B的基态原子中电子占据最高能级的电子云轮廓图为____ 。D的基态原子核外有____ 种能量不同的电子。
(2)B的氢化物BH3的VSEPR模型为____ ,其分子空间构型为_____ ;A、B、C三种元素的第一电离能由大到小的顺序为_____ (填元素符号)。
(3)BO2-中B原子的杂化轨道类型为____ ;与AB-互为等电子体的分子有_____ ,离子有_____ 。(分别写出1种)
(4)由A、C与氢形成H2A2C4分子中,1mol该分子中含有π键的数目为____ 。
(5)E元素位于元素周期表中的___ 区,E3+的一种配离子[E(BH3)5D]2+中,E3+的配位数为____ ,配位原子为____ 、____ 。
(1)A的基态原子核中核外有
(2)B的氢化物BH3的VSEPR模型为
(3)BO2-中B原子的杂化轨道类型为
(4)由A、C与氢形成H2A2C4分子中,1mol该分子中含有π键的数目为
(5)E元素位于元素周期表中的
您最近一年使用:0次