下图为元素周期表的一部分,请参照元素①~⑦在表中的位置,回答下列问题:

(1)元素⑥在周期表中的位置是___________ 。
(2)③④⑤的简单离子半径由大到小的顺序为___________ (用离子符号和“>”表示)。
(3)④和⑦形成的化合物中含有化学键类型为___________ 。
(4)④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物发生反应的离子方程式为___________ 。

(1)元素⑥在周期表中的位置是
(2)③④⑤的简单离子半径由大到小的顺序为
(3)④和⑦形成的化合物中含有化学键类型为
(4)④的最高价氧化物对应的水化物与⑥的最高价氧化物对应的水化物发生反应的离子方程式为
更新时间:2023-07-12 13:56:05
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】元素X、Y、Z、M、R均为短周期主族元素,且原子序数依次增大。已知:Y为地壳中含量最多的元素;M原子的最外层电子数与次外层电子数之比为3:4;R-、Z+、X+的离子半径逐渐减小;化合物XR常温下为气体。请回答下列问题:
(1)M元素周期表中的位置为____ ;Z+的结构示意图为____ 。
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式:____ 。
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:____ 。
(4)R的非金属性强于M的,下列能证明这一事实的是____ (填字母)。
(1)M元素周期表中的位置为
(2)写出X、Y、R按原子个数之比1:1:1形成的化合物的电子式:
(3)X与Y可分别形成10电子分子和18电子分子,写出18电子分子转化成10电子分子的化学方程式:
(4)R的非金属性强于M的,下列能证明这一事实的是
| A.常温下的R单质熔沸点比M单质的高 |
| B.R的简单氢化物比M的更稳定 |
| C.一定条件下,R和M的单质都能与NaOH溶液反应 |
| D.最高价氧化物对应水化物的酸性强弱:R>M |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】五种短周期元素的某些性质如表所示(请用相应的元素符号或化学式作答)
(1)R元素在元素周期表中的位置∶第_______ 周期,第_______ 族。
(2)用电子式表示W与Y形成化合物W2Y的过程_______
(3)Q、W、Y的离子半径由大到小的顺序为_______ ,1molR4中含有共价键数目为_______ 。
(4)X2Z2的结构式_______ ,WYZ的电子式_______ 。
(5)W3Q与WZ还原性强弱为W3Q_______ WZ(填">"、"<"或"="),WZ溶于Z2Y的化学方程式为_______ 。
(6)Z2Y2能使硫酸酸化的KMnO4溶液褪色,写出该反应的离子方程式_______ 。
| 元素 | 元素的相关信息 |
| Q | 最高价氧化物对应的水化物能与其气态氢化物发生化合反应生成盐 |
| R | 其最高价和最低价的代数和为2 |
| W | 在短周期元素中,其原子半径最大 |
| X | 其原子的最外层电子数是次外层电子数的2倍, Y是地壳中含量最多的元素 |
| Z | 是元素周期表中原子半径最小的元紫 |
(2)用电子式表示W与Y形成化合物W2Y的过程
(3)Q、W、Y的离子半径由大到小的顺序为
(4)X2Z2的结构式
(5)W3Q与WZ还原性强弱为W3Q
(6)Z2Y2能使硫酸酸化的KMnO4溶液褪色,写出该反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答下列问题。
(1)下列叙述中,正确的是_______
(2)请利用原子结构知识对下列结论进行说明和论证。
结论1:同周期的主族元素,从左到右,元素原子失电子能力越来越弱。______ 。
结论2:碱金属元素,从上到下,元素原子失电子能力越来越强。______ 。
(1)下列叙述中,正确的是_______
| A.同周期元素中,ⅦA族元素的原子半径最大 |
| B.ⅥA族元素的原子,其原子半径越大,越容易得到电子 |
| C.常温时,0族元素的单质都是气体 |
| D.在元素周期表中,从ⅢB族到ⅡB族10个纵列的元素都是金属元素 |
结论1:同周期的主族元素,从左到右,元素原子失电子能力越来越弱。
结论2:碱金属元素,从上到下,元素原子失电子能力越来越强。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据表格中关于四种元素的相关信息,按要求回答下列问题:
(1)完成表中空白:①_______ ②_______ ③_______ ④_______
(2)丁元素的最高价氧化物对应水化物的化学式为_______ ,其与丙元素的最高价氧化物对应水化物反应的离子方程式为_______ 。
(3)乙与丁两元素形成化合物的电子式为_______ 。
(4)甲元素的氢化物中最简单的是_______ (填化学式),该氢化物光照时可与氯气发生取代反应生成一氯代物,其化学方程式为_______ 。
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子序数 | 11 | ③ | ||
| 元素符号 | ① | Cl | ||
| 原子结构示意图 | ② | |||
| 位置 | 第二周期第ⅣA族 | 第三周期第ⅢA族 | ④ |
(1)完成表中空白:①
(2)丁元素的最高价氧化物对应水化物的化学式为
(3)乙与丁两元素形成化合物的电子式为
(4)甲元素的氢化物中最简单的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,表中的每个字母代表一种短周期元素。
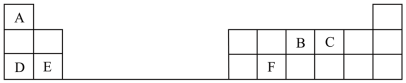
请填写下列空白:
(1)A与B形成 的电子式为
的电子式为________ ;C的原子结构示意图为________ 。
(2)B的最高价氧化物对应的水化物的化学式为_______ ;D、E的最高价氧化物对应的水化物中碱性较弱的是_______  用化学式表示
用化学式表示 ;
;
(3)F的氧化物与氢氧化钠溶液反应的离子方程式为______________ 。

请填写下列空白:
(1)A与B形成
 的电子式为
的电子式为(2)B的最高价氧化物对应的水化物的化学式为
 用化学式表示
用化学式表示 ;
; (3)F的氧化物与氢氧化钠溶液反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】易混易错题组
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气_______ 过氧化钠 _________ 四氯化碳________
(2)写出下列物质的结构式
二氧化碳________ 过氧化氢 _________ 次氯酸________
(学法题)正确书写化合物的电子式需要注意的问题是_____________
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:___________
②原子半径由大到小的顺序为:___________
③离子半径由大到小的顺序为:___________
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-________ Cl- ②Fe2+________ Fe3+ ③O2-_________ Mg2+
(学法题)粒子半径大小比较方法(两点即可)___________
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气
(2)写出下列物质的结构式
二氧化碳
(学法题)正确书写化合物的电子式需要注意的问题是
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:
②原子半径由大到小的顺序为:
③离子半径由大到小的顺序为:
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-
(学法题)粒子半径大小比较方法(两点即可)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】锂离子电池在生产生活中应用广泛,LiFePO4、LiPF6和LiAsF6均可作锂离子电池的电极材料。回答下列问题:
(1)基态锂原子的轨道表达式为_______ 。
(2)O2-和F-半径更大的是_______ ;O、F、Fe的第一电离能由大到小的顺序为_______ 。
(3)H3AsO4的酸性强于H3AsO3的原因为_______ 。
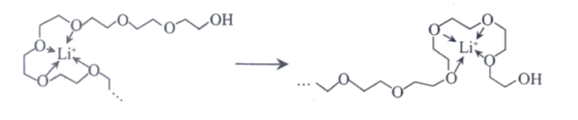
(4)锂离子电池工作时,Li+可在离子导体中迁移。Li+沿聚乙二醇分子中的碳氧链迁移的过程如图所示,该迁移过程属于_______ (填“物理变化”或“化学变化”)。
(5)以LiPF6和LiAsF6作锂离子电池的负极材料时,放电过程的实质是Li+从负极材料脱嵌。相同条件下,Li+更易在_______ (填“LiPF6”或“LiAsF6”)电极中脱嵌,解释其原因为_______ 。
(1)基态锂原子的轨道表达式为
(2)O2-和F-半径更大的是
(3)H3AsO4的酸性强于H3AsO3的原因为
(4)锂离子电池工作时,Li+可在离子导体中迁移。Li+沿聚乙二醇分子中的碳氧链迁移的过程如图所示,该迁移过程属于

(5)以LiPF6和LiAsF6作锂离子电池的负极材料时,放电过程的实质是Li+从负极材料脱嵌。相同条件下,Li+更易在
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】工业合成氨是利用氮气和氢气在一定条件下反应生成的。氨是重要的工业原料。请回答下列问题:
(1)氮元素在周期表中的位置是第_______ 周期第_______ 族;氮原子结构示意图为_______ 。
(2)写出氨分子的电子式______ ;指出分子中化学键类型是_____ 。
(3)写成合成氨的化学方程式:________________________ ;该反应是放热反应,则相同条件下“1molN2和3molH2”的能量与“2molNH3”的能量较高的是________________ 。
(1)氮元素在周期表中的位置是第
(2)写出氨分子的电子式
(3)写成合成氨的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下面是同学们熟悉的物质:
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3 ⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是______ ;只含有离子键的是 ______ ;既含有共价键又含有离子键的是 ______ ;不存在化学键的是 ______ ;电解质有____________ ;
非电解质有___________ ( 填编号)
(2)将NaHSO4溶于水,破坏NaHSO4中的化学键是_____________ ,写出其电离方程式________ ;NaHSO4在熔融状态下电离,破坏的化学键是_____________ ,写出其电离方程式____________ .
(3)写出②与⑨发生反应的化学方程式:____________ .
(4)写出在稀溶液中⑥和⑩反应的离子方程式:____________ .
①O2 ②干冰 ③NaBr ④H2SO4 ⑤Na2CO3 ⑥NH4Cl ⑦NaHSO4 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,只含有共价键的是
非电解质有
(2)将NaHSO4溶于水,破坏NaHSO4中的化学键是
(3)写出②与⑨发生反应的化学方程式:
(4)写出在稀溶液中⑥和⑩反应的离子方程式:
您最近一年使用:0次



