1 . 下表是元素周期表的一部分,回答下列问题。
(1)原子结构示意图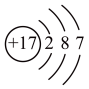 所表示的原子是
所表示的原子是___________ 。
(2)H2O分子的电子式为___________ (填序号)。
a.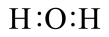 b.
b.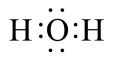 c.
c. 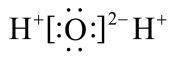
(3)根据元素在周期表中的位置推测Na、Al和Cl原子半径由大到小的顺序为___________ 。
(4)重水是核能开发中的重要原料。核素 H与
H与 H之间互称
H之间互称___________ 。
(5)已知:
据此推断,F、Cl两元素非金属性较强的是___________ (填元素符号)。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | H | ||||||
| 二 | O | F | |||||
| 三 | Na | Al | Cl |
 所表示的原子是
所表示的原子是(2)H2O分子的电子式为
a.
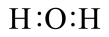 b.
b.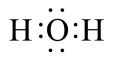 c.
c. 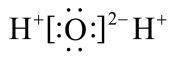
(3)根据元素在周期表中的位置推测Na、Al和Cl原子半径由大到小的顺序为
(4)重水是核能开发中的重要原料。核素
 H与
H与 H之间互称
H之间互称(5)已知:
| H2+F2=2HF | 在暗处能剧烈化合并发生爆炸,生成的氟化氢很稳定 |
H2+Cl2 2HCl 2HCl | 光照或点燃发生反应,生成的氯化氢较稳定 |
您最近一年使用:0次
解题方法
2 . 下表是元素周期表的一部分。
回答问题:
(1)门捷列夫科学地预言了“类铝”元素Ga, Ga在元素周期表中的位置是第_______ 周期、第_______ 族。
(2)第三周期主族元素中,金属性最强的元素原子结构示意图为_______ 。
(3)碳元素的一种放射性核素 C可用于文物年代的测定,
C可用于文物年代的测定, C 的原子核内中子数为
C 的原子核内中子数为_______ 。
(4)某研究小组探究氯与溴非金属性的强弱关系,过程如下:
[预测]非金属性: Cl>Br。
[设计与实验]如图所示,在点滴板的2个孔穴中分别滴入3滴新制氯水,然后向其中之一滴加3滴NaBr溶液。

[证据与分析]滴加NaBr溶液的孔穴中,溶液颜色变深,说明有Br2生成。
[结论]预测_______ (选项“正确”或“不正确”)。
[解释]从原子结构的角度解释为_______ 。
族 周期 | I A | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | C | ||||||
| 3 | Na | Mg | Al | Si | P | S | Cl |
| 4 | Ga | Br |
回答问题:
(1)门捷列夫科学地预言了“类铝”元素Ga, Ga在元素周期表中的位置是第
(2)第三周期主族元素中,金属性最强的元素原子结构示意图为
(3)碳元素的一种放射性核素
 C可用于文物年代的测定,
C可用于文物年代的测定, C 的原子核内中子数为
C 的原子核内中子数为(4)某研究小组探究氯与溴非金属性的强弱关系,过程如下:
[预测]非金属性: Cl>Br。
[设计与实验]如图所示,在点滴板的2个孔穴中分别滴入3滴新制氯水,然后向其中之一滴加3滴NaBr溶液。

[证据与分析]滴加NaBr溶液的孔穴中,溶液颜色变深,说明有Br2生成。
[结论]预测
[解释]从原子结构的角度解释为
您最近一年使用:0次
3 . 下表为第三周期元素的部分信息:
请回答下列问题:
(1)画出Mg的原子结构示意图_______ 。
(2)根据原子半径递变规律,推测Al原子半径_______ 0.160nm(选填“大于”或“小于”)
(3)根据上表信息,推测Cl元素的最高正化合价是_______ 。
(4)上表中其单质能广泛用作半导体材料的元素是_______ 。
(5)某学习小组为探究钠与镁金属性的强弱关系,进行如下实验设计:
【实验操作】将大小接近的金属钠块和镁条分别放入等体积的冷水中,如下图:

【实验现象】钠比镁与水反应更剧烈。
【实验结论】钠与镁金属性的强弱关系为_______ 。
| 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第三周期 | 元素符号 | Na | Mg | Al | Si | P | S | Cl | Ar |
| 原子半径/nm | 0.186 | 0.160 | 0.117 | 0.110 | 0.102 | 0.099 | / | ||
| 最高正化合价或最低负化合价 | +1 | +2 | +3 | +4 -4 | +5 -3 | +6 -2 | -1 | 0 | |
请回答下列问题:
(1)画出Mg的原子结构示意图
(2)根据原子半径递变规律,推测Al原子半径
(3)根据上表信息,推测Cl元素的最高正化合价是
(4)上表中其单质能广泛用作半导体材料的元素是
(5)某学习小组为探究钠与镁金属性的强弱关系,进行如下实验设计:
【实验操作】将大小接近的金属钠块和镁条分别放入等体积的冷水中,如下图:

【实验现象】钠比镁与水反应更剧烈。
【实验结论】钠与镁金属性的强弱关系为
您最近一年使用:0次
4 . 科学研究中,常采用控制变量的方法。某化学兴趣小组的同学针对反应 设计实验探究化学反应速率的影响因素,用传感器采集数据,生成如下图象:
设计实验探究化学反应速率的影响因素,用传感器采集数据,生成如下图象:
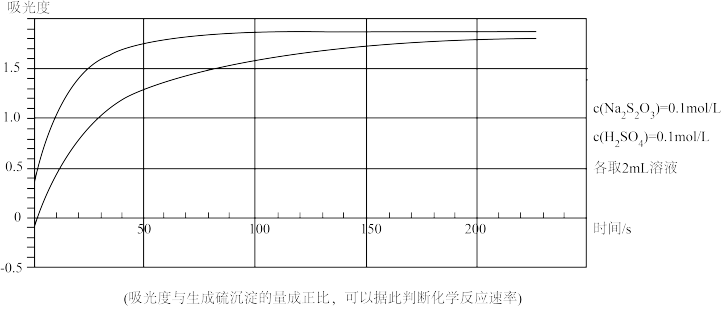
请回答下列问题:
(1)图象表明,其他条件不变时,改变温度,60℃比40℃时反应速率_______ (选填“快”或“慢”)。
(2)除温度外,还可以探究该反应速率的影响因素是_______ (写一条)。
(3) 是有毒、有污染的气体,实验中在试管口放一浸碱棉团,其作用是
是有毒、有污染的气体,实验中在试管口放一浸碱棉团,其作用是_______ 。
(4)若将 通入品红溶液,可观察到溶液的颜色变化是
通入品红溶液,可观察到溶液的颜色变化是_______ 。
(5)实验室里,通常将反应后的溶液先加入盐酸酸化,无明显现象,然后再加入 溶液来检验
溶液来检验 的存在,写出该反应的离子方程式
的存在,写出该反应的离子方程式_______ 。
 设计实验探究化学反应速率的影响因素,用传感器采集数据,生成如下图象:
设计实验探究化学反应速率的影响因素,用传感器采集数据,生成如下图象:
请回答下列问题:
(1)图象表明,其他条件不变时,改变温度,60℃比40℃时反应速率
(2)除温度外,还可以探究该反应速率的影响因素是
(3)
 是有毒、有污染的气体,实验中在试管口放一浸碱棉团,其作用是
是有毒、有污染的气体,实验中在试管口放一浸碱棉团,其作用是(4)若将
 通入品红溶液,可观察到溶液的颜色变化是
通入品红溶液,可观察到溶液的颜色变化是(5)实验室里,通常将反应后的溶液先加入盐酸酸化,无明显现象,然后再加入
 溶液来检验
溶液来检验 的存在,写出该反应的离子方程式
的存在,写出该反应的离子方程式
您最近一年使用:0次
5 . (1)下列不属于化石燃料的是_______ 。
A.煤 B.石油 C.天然气 D.氢气
(2)下列关于化工生产的描述中正确的是________ 。
A.要依据化学反应原理确定生产过程
B.原料的选择不必考虑环境问题
C.生产条件的选择只需要考虑转化率
D.生产中的“三废”可以直接排放
(3)我国化工专家侯德榜提出了“联合制碱法”,该法制备的“碱”是指______ 。
A.Na2CO3 B.Na2O C.NaOH D.NaCl
(4)铁在自然界主要以氧化物、硫化物等形式存在,生铁的冶炼就是在高温下用____ 将铁从其氧化物中还原出来。钢铁在潮湿的空气中更容易发生 _________ (填 “化学腐蚀”或“电化学腐蚀”)。
A.煤 B.石油 C.天然气 D.氢气
(2)下列关于化工生产的描述中正确的是
A.要依据化学反应原理确定生产过程
B.原料的选择不必考虑环境问题
C.生产条件的选择只需要考虑转化率
D.生产中的“三废”可以直接排放
(3)我国化工专家侯德榜提出了“联合制碱法”,该法制备的“碱”是指
A.Na2CO3 B.Na2O C.NaOH D.NaCl
(4)铁在自然界主要以氧化物、硫化物等形式存在,生铁的冶炼就是在高温下用
您最近一年使用:0次
6 . (1)珍爱生命,远离毒品。下列物质中属于毒品的是______ 。
A、青霉素 B、海洛因 C、阿司匹林 D、复方氢氧化铝
(2)材料与人类生活密切相关。下列物品与对应的材料不匹配的是_____ 。
A、陶瓷艺术品------硅酸盐材料 B、羊毛-------合成纤维
C、不锈钢餐具------合金材料 D、棉花------天然纤维
(3)为改善气候和环境,下列做法不可行的是_________ 。
A、多种树,提高森林覆盖率 B、少开车,提倡绿色出行
C、工业废水直接排放到大海 D、响应”地球一小时”活动
(4)小海经医生诊断患有轻度贫血,在饮食上他应选择富含_________ 元素的食物,同时适量补充蛋白质含量高的食物,蛋白质在体内经完全水解后的最终产物是_______________ 。
A、青霉素 B、海洛因 C、阿司匹林 D、复方氢氧化铝
(2)材料与人类生活密切相关。下列物品与对应的材料不匹配的是
A、陶瓷艺术品------硅酸盐材料 B、羊毛-------合成纤维
C、不锈钢餐具------合金材料 D、棉花------天然纤维
(3)为改善气候和环境,下列做法不可行的是
A、多种树,提高森林覆盖率 B、少开车,提倡绿色出行
C、工业废水直接排放到大海 D、响应”地球一小时”活动
(4)小海经医生诊断患有轻度贫血,在饮食上他应选择富含
您最近一年使用:0次
7 . (1)我省拥有非常丰富的海洋资源,合理开发利用海洋资源,造福海南人民。
①目前国际上“海水淡化”的主要方法有______________________ (任写一种);
②我省著名的莺歌海盐场是重要的海水晒盐基地。海水晒盐的原理是海水受热使水分_________ ,当NaCl达到其饱和浓度时,以固态形式析出;
③海水经过处理后获得的饱和食盐水可以通过_________ 法制得NaOH、Cl2和H2等重要的化工原料;
④从氯碱工业的副产品中能够得到一种含氯消毒剂,有效成分为NaClO,该消毒剂起作用的原理是利用了NaClO的__________ (填“强氧化性”或“强还原性”)。
(2)合成氨是重要的化学工业之一,其部分生产工艺如下图所示

请回答下列问题:
①操作Ⅰ的名称是______ 。
a.蒸馏 b.过滤 c.干馏
②合成氨反应中催化剂的主要作用是________________________ ;
③从合成塔中出来的气体除了NH3之外,还有_________________ (写化学式);
④合成氨工业中,操作Ⅱ的工艺称为“循环操作”,使用该工艺的好处是_________ 。
①目前国际上“海水淡化”的主要方法有
②我省著名的莺歌海盐场是重要的海水晒盐基地。海水晒盐的原理是海水受热使水分
③海水经过处理后获得的饱和食盐水可以通过
④从氯碱工业的副产品中能够得到一种含氯消毒剂,有效成分为NaClO,该消毒剂起作用的原理是利用了NaClO的
(2)合成氨是重要的化学工业之一,其部分生产工艺如下图所示

请回答下列问题:
①操作Ⅰ的名称是
a.蒸馏 b.过滤 c.干馏
②合成氨反应中催化剂的主要作用是
③从合成塔中出来的气体除了NH3之外,还有
④合成氨工业中,操作Ⅱ的工艺称为“循环操作”,使用该工艺的好处是
您最近一年使用:0次
8 . 品味生活,感知化学
(1)“美食名粽,品位海南”,2017年5月20日海南名粽展销会拉开帷幕。海南粽子的主要食材有:糯米、猪肉、咸蛋黄等。
①以上食材中富含淀粉的是________________ ;
②从平衡膳食的角度看,吃海南粽子时,还应补充适量的_____________ (填营养素名称);
③海南粽子经过真空包装,并添加一定的抗氧化剂后销往各地,抗氧化剂所起的作用是________________
(填“着色”或“防腐”或“调味”);
④粽叶一般选择新鲜的植物叶子,剥下的粽叶为实现无害化、资源化处理,写出一种合理的处理方法_________________________ 。
(2)下图是一辆大气环境监测汽车,请回答下列问题:

①汽车轮胎所用的主要材料是_________________ 。
②汽车外壳会喷上各种颜色的油漆,一方面能起到美化作用,另一方面油漆还能为钢铁材料起到________________ 作用;
③汽车的内饰材料若不合格,易产生一些挥发性有毒物质如________ (填“甲醛”或“甲烷”或“乙醇”)而对车内空气造成污染;
④目前,大气环境监测公布的主要污染物有硫的氧化物、氮的氧化物和________ (填字母)。
a.二氧化碳 b.氮气 c.可吸入颗粒物
(1)“美食名粽,品位海南”,2017年5月20日海南名粽展销会拉开帷幕。海南粽子的主要食材有:糯米、猪肉、咸蛋黄等。
①以上食材中富含淀粉的是
②从平衡膳食的角度看,吃海南粽子时,还应补充适量的
③海南粽子经过真空包装,并添加一定的抗氧化剂后销往各地,抗氧化剂所起的作用是
(填“着色”或“防腐”或“调味”);
④粽叶一般选择新鲜的植物叶子,剥下的粽叶为实现无害化、资源化处理,写出一种合理的处理方法
(2)下图是一辆大气环境监测汽车,请回答下列问题:

①汽车轮胎所用的主要材料是
②汽车外壳会喷上各种颜色的油漆,一方面能起到美化作用,另一方面油漆还能为钢铁材料起到
③汽车的内饰材料若不合格,易产生一些挥发性有毒物质如
④目前,大气环境监测公布的主要污染物有硫的氧化物、氮的氧化物和
a.二氧化碳 b.氮气 c.可吸入颗粒物
您最近一年使用:0次
2017-06-17更新
|
232次组卷
|
3卷引用:海南省2016-2017学年高二普通高中基础会考化学试题
9 . 图1为铁在一定条件下的转化关系图。

请回答:
(1)“曾青得铁则化为铜”的反应有:Fe + CuSO4 = FeSO4 + Cu,该反应的还原剂是_____________ (填化学式);
(2)工业上,向500-600℃的铁屑中通入Cl2生产FeCl3,向FeCl3溶液中滴加KSCN溶液,观察到的现象是溶液变成____________ 色;
(3)图2为原电池装置示意图,此装置可以把化学能转化为_________ 能,其中铁作_____ 极;

(4)Fe3O4中Fe既有+2价又有+3价,则+2价和+3价Fe的个数比为__________ 。

请回答:
(1)“曾青得铁则化为铜”的反应有:Fe + CuSO4 = FeSO4 + Cu,该反应的还原剂是
(2)工业上,向500-600℃的铁屑中通入Cl2生产FeCl3,向FeCl3溶液中滴加KSCN溶液,观察到的现象是溶液变成
(3)图2为原电池装置示意图,此装置可以把化学能转化为

(4)Fe3O4中Fe既有+2价又有+3价,则+2价和+3价Fe的个数比为
您最近一年使用:0次
2017-06-17更新
|
382次组卷
|
2卷引用:海南省2016-2017学年高二普通高中基础会考化学试题
10 . 下表是元素周期表的一部分,请回答:
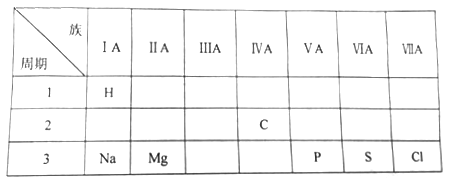
(1)周期表中第三周期第IIA族的元素是__________ ;
(2)P、S、Cl三种元素中,非金属性最强的是________ (填元素符号);
(3)钠元素最高价氧化物对应的水化物化学式是________ ,常温下该水化物溶液的pH____ 7(填“>”或“<”或“=”);
(4)如图为木炭在氧气中燃烧的能量变化图,此反应为____ 反应(填“放热”或“吸热”)。


(1)周期表中第三周期第IIA族的元素是
(2)P、S、Cl三种元素中,非金属性最强的是
(3)钠元素最高价氧化物对应的水化物化学式是
(4)如图为木炭在氧气中燃烧的能量变化图,此反应为

您最近一年使用:0次



