解题方法
1 . 分析原电池的工作原理,制作简易电池。
(1)某原电池实验装置如图1所示。_______ (填“铜片”或“锌片”)。
②写出铜片上发生的电极反应:_______ 。
(2)小组同学制作的水果电池如图2所示。_______ (填字母)。
a.水果汁中含有自由移动的离子
b.该装置使氧化反应和还原反应分别在两极进行
②电流表指针偏转,说明该装置实现了化学能向_______ 的转化。
(1)某原电池实验装置如图1所示。
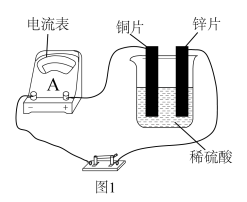
②写出铜片上发生的电极反应:
(2)小组同学制作的水果电池如图2所示。

a.水果汁中含有自由移动的离子
b.该装置使氧化反应和还原反应分别在两极进行
②电流表指针偏转,说明该装置实现了化学能向
您最近一年使用:0次
2 . 从海带浸泡液(碘元素主要以 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。 的作用为
的作用为_______ (填“氧化剂”或“还原剂”)。
(2)为提高①的化学反应速率,可采取的措施是_______ (写出一条即可)。
(3)补全②的离子方程式:_______ 。
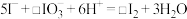
(4)②中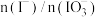 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。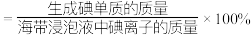
分析图中信息,选择最佳条件:_______ 。
 存在)中获取
存在)中获取 ,含碘物质的转化过程如下。
,含碘物质的转化过程如下。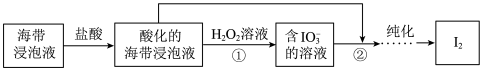
 的作用为
的作用为(2)为提高①的化学反应速率,可采取的措施是
(3)补全②的离子方程式:
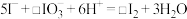
(4)②中
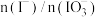 和pH对碘离子的氧化率的影响如下图所示。
和pH对碘离子的氧化率的影响如下图所示。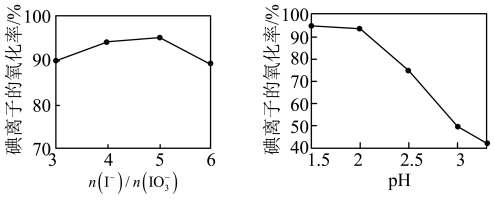
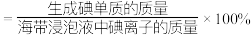
分析图中信息,选择最佳条件:
您最近一年使用:0次
3 . 补齐物质与其用途之间的连线_______ 。
| 物质 用途 A.乙酸――――――a.清除水垢 B.氧化铁 b.作供氧剂 C.次氯酸钠 c.作红色颜料 D.过氧化钠 d.作消毒剂 |
您最近一年使用:0次
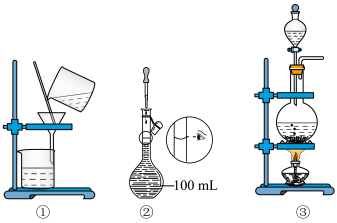
4 . 选择完成下列实验的装置。 浓盐酸的混合物制
浓盐酸的混合物制 ,选用
,选用_______ (填序号,下同)。
(2)用 溶液和
溶液和 制取
制取 后,若回收
后,若回收 选用
选用_______ 。
(3)配制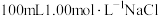 溶液,选用
溶液,选用_______ 。
 浓盐酸的混合物制
浓盐酸的混合物制 ,选用
,选用(2)用
 溶液和
溶液和 制取
制取 后,若回收
后,若回收 选用
选用(3)配制
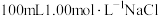 溶液,选用
溶液,选用
您最近一年使用:0次
5 . “民以食为天”,对元素周期表中有关元素的认识可使我们更好地了解食品的营养和安全。
结合上述材料,回答下列问题:
(1)仅含a、b、d三种元素的营养物质有___________。
(2)成熟水果会释放出由a和b按原子数目比 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。
(3)某些元素的单质或化合物常用于食品加工和保存。下列说法正确的是___________。
(4)土豆中富含淀粉。淀粉___________。
(5)由a、b、d和e四种元素形成的物质可用作糕点膨松剂。下列说法正确的是___________。
| 周期 | ⅠA | 0 | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | |||||
| 3 | e | f | g | h |
(1)仅含a、b、d三种元素的营养物质有___________。
| A.脂肪 | B.葡萄糖 | C.蛋白质 | D.氨基酸 |
 组成的气体。该气体分子___________。
组成的气体。该气体分子___________。A.分子式为 | B.呈四面体结构 |
| C.呈三角锥形结构 | D.所有原子共平面 |
| A.a的单质可与植物油发生加成反应 | B.c的单质充入食品包装袋中可防腐 |
| C.f的单质制作的容器可用于贮存酸菜 | D.e和h形成的化合物可用于腌制食品 |
| A.遇碘溶液变色 | B.可水解得到乙醇 |
| C.由a、b、g三种元素组成 | D.水解的最终产物能发生银镜反应 |
| A.非金属性:b>a>d | B.原子半径:e>b>d |
| C.e的最高价氧化物的水化物是强碱 | D.b、d、e原子具有相同的电子层数 |
您最近一年使用:0次
6 . 半胱氨酸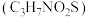 是人体细胞正常活动的必需氨基酸之一。
是人体细胞正常活动的必需氨基酸之一。
(1)组成半胱氨酸的元素中,位于元素周期表第三周期的是_______ 。
(2)非金属性N强于C。
①事实依据: 的酸性比
的酸性比
_______ (填“强”或“弱”)。
②从原子结构角度解释:N和C位于同一周期,原子核外电子层数相同,_______ ,原子半径N小于C,得电子能力N强于C。
(3)半胱氨酸分子中的硫原子被硒(Se)原子取代后称为硒代半胱氨酸,硒代半胱氨酸分子是潜在的抗癌分子药物。Se与O、S在元素周期表中位于同一主族。下列推测正确的是_______ (填字母)。
a.Se的最低化合价为 价
价
b.原子半径:
c.将 通入
通入 溶液中,可生成S
溶液中,可生成S
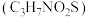 是人体细胞正常活动的必需氨基酸之一。
是人体细胞正常活动的必需氨基酸之一。(1)组成半胱氨酸的元素中,位于元素周期表第三周期的是
(2)非金属性N强于C。
①事实依据:
 的酸性比
的酸性比
②从原子结构角度解释:N和C位于同一周期,原子核外电子层数相同,
(3)半胱氨酸分子中的硫原子被硒(Se)原子取代后称为硒代半胱氨酸,硒代半胱氨酸分子是潜在的抗癌分子药物。Se与O、S在元素周期表中位于同一主族。下列推测正确的是
a.Se的最低化合价为
 价
价b.原子半径:

c.将
 通入
通入 溶液中,可生成S
溶液中,可生成S
您最近一年使用:0次
7 . 金属钛(Ti)具有许多优异的性能,是航空、军工、电力等领域的必需材料。以金红石为原料制取金属钛,其中发生的化学反应之一:

(1)作还原剂的物质是_______ ,钛元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了2molMg,则生成Ti的物质的量为_______ mol,转移电子的物质的量为_______ mol。

(1)作还原剂的物质是
(2)若反应中消耗了2molMg,则生成Ti的物质的量为
您最近一年使用:0次
8 . 已知X、Y为短周期中的两种元素,原子序数X>Y,且X、Y的最外层电子数都是5个,Y元素的单质在空气中的含量最高,则:
(1)X是___________ (填元素符号);
(2)Y最简单氢化物的化学式是___________ ;
(3)X、Y两种元素的非金属性强弱是X___________ Y(填“>”或“<”);
(4)Y的简单氢化物与其最高价氧化物对应的水化物反应的离子方程式为___________ 。
(1)X是
(2)Y最简单氢化物的化学式是
(3)X、Y两种元素的非金属性强弱是X
(4)Y的简单氢化物与其最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
9 . 苯甲酸有杀菌和抑制细菌生长的作用。在食品工业中,可作酱油、泡菜、苹果酒、果汁等的防腐剂,结构简式为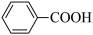 ,请回答下列问题:
,请回答下列问题:
(2)苯甲酸是一种弱酸,其分子中所含的官能团是
(3)苯甲酸的酸性强于碳酸,可与
 溶液反应,补充完整下列方程式:
溶液反应,补充完整下列方程式: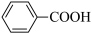
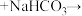
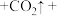
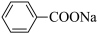
您最近一年使用:0次
解题方法
10 . 非金属元素及其化合物在生产生活中有着重要地位。请根据题意填空:
(1)能用来杀菌消毒,见光易分解的弱酸是___________ (填“HClO”或“HCl”);
(2)实验室常用浓硫酸作干燥剂。浓硫酸能用来干燥___________ (填“ ”或“
”或“ ”);
”);
(3)芯片的设计、制造能力关乎国家发展大计。构成芯片的基本材料是___________ (填“ ”或“Si”)。
”或“Si”)。
(1)能用来杀菌消毒,见光易分解的弱酸是
(2)实验室常用浓硫酸作干燥剂。浓硫酸能用来干燥
 ”或“
”或“ ”);
”);(3)芯片的设计、制造能力关乎国家发展大计。构成芯片的基本材料是
 ”或“Si”)。
”或“Si”)。
您最近一年使用:0次



