2024·山东青岛·二模
1 . 过渡元素镍钛在分子捕捉、量子材料等方向日益重要。回答下列问题:
(1)某Ni离子与 、
、 形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为
形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为______ ,Ni的化合价为______ ,杂化轨道数为______ 。 与Ni离子形成配位键时的配位原子为
与Ni离子形成配位键时的配位原子为______ ,键角∠H-N-H______ (填“>”或“<”)107.3°。
(2)部分钛酸锶晶胞结构如图乙。晶体Ⅰ的化学式为Ⅰ_____ ,该系列晶体的化学式可表示为_____ (用含n的式子表示,n为Ti原子个数),当 时,晶体化学式为
时,晶体化学式为______ 。
(1)某Ni离子与
 、
、 形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为
形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为 与Ni离子形成配位键时的配位原子为
与Ni离子形成配位键时的配位原子为(2)部分钛酸锶晶胞结构如图乙。晶体Ⅰ的化学式为Ⅰ
 时,晶体化学式为
时,晶体化学式为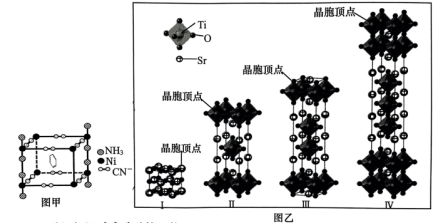
您最近一年使用:0次
2 . 爱护水资源,落实长江大保护。
(1)树立保护水体意识。下列做法正确的有___________ 。
A.节约用水 B.工业用水重复利用 C.洗衣污水集中处理
(2)掌握水的净化方法。日常生活中,我们常使用活性炭制作净水器滤芯,是利用活性炭的___________ 性,为降低水的硬度,我们常选择的方法是___________ 。
(3)学习净水材料制备。高铁酸钾(K2FeO4)是一种新型非氯高效水处理消毒剂,主要用于饮用水处理,制备高铁酸钾的一种模拟流程如图(部分反应条件未标出):___________ 。
②反应A、B、C、D中属于复分解反应的是___________ 。
③反应A的化学方程式是___________ 。
(1)树立保护水体意识。下列做法正确的有
A.节约用水 B.工业用水重复利用 C.洗衣污水集中处理
(2)掌握水的净化方法。日常生活中,我们常使用活性炭制作净水器滤芯,是利用活性炭的
(3)学习净水材料制备。高铁酸钾(K2FeO4)是一种新型非氯高效水处理消毒剂,主要用于饮用水处理,制备高铁酸钾的一种模拟流程如图(部分反应条件未标出):
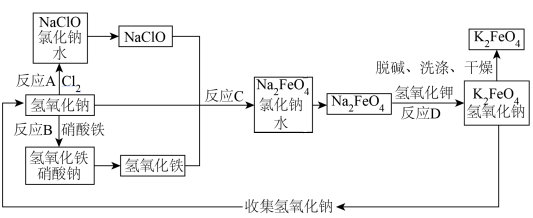
②反应A、B、C、D中属于复分解反应的是
③反应A的化学方程式是
您最近一年使用:0次
3 . 为测定某过氧化钠样品的纯度,将2g该样品与足量水发生反应(杂质不参与反应):2Na2O2+2H2O=4NaOH+O2↑,生成气体质量与时间的关系如图所示。
(1)生成氧气的质量是___________ g。
(2)列式计算该样品中过氧化钠的质量分数为___________ 。
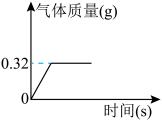
(1)生成氧气的质量是
(2)列式计算该样品中过氧化钠的质量分数为
您最近一年使用:0次
4 . 根据如图实验装置,请回答:___________ 。
(2)检查装置A气密性的方法是夹紧止水夹,___________ ,则气密性良好。
(3)用H2O2制取氧气,选择的发生装置为___________ (填字母),反应的化学方程式为___________ 。
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为___________ ,在F中气体应从导管___________ (填“b”或“c”)端通入。
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为___________ (填字母)。用装置E收集甲烷,利用了甲烷___________ 的物理性质;用装置C而不用装置D收集甲烷,原因是___________ 。
②设计实验证明CH4中含有氢元素:检验其纯度后,___________ 。

(2)检查装置A气密性的方法是夹紧止水夹,
(3)用H2O2制取氧气,选择的发生装置为
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷。
①选择的发生装置为
②设计实验证明CH4中含有氢元素:检验其纯度后,
您最近一年使用:0次
5 . 利用物质的性质能帮助我们开展科学探究。
(1)判断化学变化。如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是___________ 。
实验结论:稀盐酸和氢氧化钠溶液反应的化学方程式为___________ 。
(1)判断化学变化。如图,在稀盐酸和氢氧化钠溶液中分别滴加几滴无色酚酞溶液,观察到能使无色酚酞变红的物质是

| 编号 | 实验操作 | 实验现象 | 实验分析 |
| 实验一 | 取一定量稀盐酸于小烧杯中,加入氢氧化钠溶液 | 无明显现象 | 稀盐酸与氢氧化钠溶液混合后有新物质生成 |
| 实验二 | 取实验一所得溶液少量于试管中,滴入几滴无色酚酞溶液 | 无明显现象 | |
| 实验三 | 取实验一所得溶液少量, |
您最近一年使用:0次
6 . 含碳物质种类繁多。请回答下列问题:
(1)葡萄糖(C6H12O6)中C、H、O原子的数目之比是___________ 。
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是___________ (填字母序号)。
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C2H5OH)是___________ (填“可再生”或“不可再生”)能源,乙醇完成燃烧的化学方程式是___________ 。该反应中,化学能转变为___________ 能。
(1)葡萄糖(C6H12O6)中C、H、O原子的数目之比是
(2)石墨烯和金刚石均为碳单质,但导电性差异很大,原因是
a.原子的排列方式不同 b.原子在不断运动 c.原子的体积很小
(3)乙醇(C2H5OH)是
您最近一年使用:0次
7 . 化学与生产生活密切相关,回答下列问题:
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是___________ 。
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是___________ 。
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是___________ 。
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的___________ 。
(1)在我市新农村建设中,许多家庭兴建了沼气池。沼气的主要成分是
(2)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,原因是
(3)许多矿石中含有铁元素,菱铁矿的主要成分是FeCO3,其中铁元素的化合价是
(4)大米的主要成分是淀粉,淀粉属于六大基本营养素中的
您最近一年使用:0次
2024高三·全国·专题练习
8 . 化学让生活更美好,各类水处理剂能让水源水质得到提升,达到饮用水的标准。生活中较常见的水处理剂有氯气、次氯酸钠、漂白粉(主要成分为次氯酸钙)、二氧化氯、明矾、硫酸铁、高铁酸钠等。
(1)氯气常用于自来水的消毒,请写出氯气溶于水的离子方程式:___________ 。
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.加热时,当NaOH与Cl2反应生成的n(NaClO)∶n(NaClO3)=5∶1时,NaOH与Cl2反应的化学方程式为___________ 。
(3)氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO 、Cl-的转化率与pH关系如图所示。
、Cl-的转化率与pH关系如图所示。___________ 。某工厂污水中含CN-a mg·L-1,现用ClO2将CN-氧化,生成了两种无毒无害的气体,处理50 m3这种污水,至少需要ClO2___________ mol。
(4)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,则Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(1)氯气常用于自来水的消毒,请写出氯气溶于水的离子方程式:
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.加热时,当NaOH与Cl2反应生成的n(NaClO)∶n(NaClO3)=5∶1时,NaOH与Cl2反应的化学方程式为
(3)氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO
 、Cl-的转化率与pH关系如图所示。
、Cl-的转化率与pH关系如图所示。
(4)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,则Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运。通过氨热分解法制取氢气,其反应的化学方程式如下: 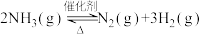
(1)根据下表数据,写出氨热分解法的热化学方程式___________ 。相关化学键的键能数据
(2)已知该反应的∆S=198.9×10-3kJ·mol-1·K-1,判断在300℃时反应是否能自发进行___________ (填“是”或“否”),理由是___________ 。
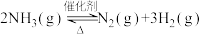
(1)根据下表数据,写出氨热分解法的热化学方程式
| 化学键 | N≡N | H-H | N-H |
| 键能E/(kJ·mol-1) | 946 | 436.0 | 390.8 |
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 黄铁矿[主要成分为二硫化亚铁(FeS2)]、焦炭和适量空气混合加热发生如下反应:
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为___________ mol。
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2.将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g) S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0
iii.SO2(g)+3CO(g) COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0
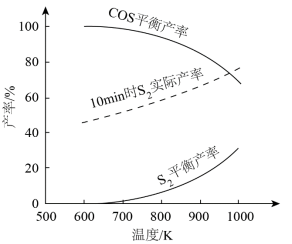
理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。___________ 。
②随温度升高,S2平衡产率上升,推测其原因是___________ 。
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为___________ 。
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2.将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g)
 S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0iii.SO2(g)+3CO(g)
 COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。
②随温度升高,S2平衡产率上升,推测其原因是
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为
您最近一年使用:0次



