2025高三·全国·专题练习
解题方法
1 . 根据信息书写方程式或描述反应过程。
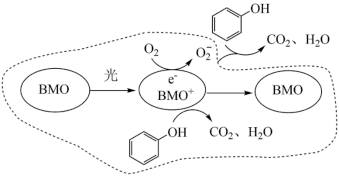
(1)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。___________ 。
②写出 与苯酚反应的离子方程式:
与苯酚反应的离子方程式:___________ 。
(2)氯化银可以溶于氨水中,写出该反应的离子方程式:___________ 。
(1)BMO(Bi2MoO6)是一种高效光催化剂,可用于光催化降解苯酚,弱酸性条件下降解苯酚的反应原理如下图所示。
②写出
 与苯酚反应的离子方程式:
与苯酚反应的离子方程式:(2)氯化银可以溶于氨水中,写出该反应的离子方程式:
您最近一年使用:0次
2025高三·全国·专题练习
解题方法
2 .  有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应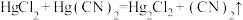 用于制备
用于制备 。
。
(1)上述反应的氧化剂是___________ 。
(2)写出 的结构简式
的结构简式___________ , 的空间构型是
的空间构型是___________ ;1mol 分子中
分子中 键为
键为___________ mol。
(3) 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式___________ 。
(4)基态N价层电子排布式为___________ 。
 有较强的配位能力,许多金属离子都可以与
有较强的配位能力,许多金属离子都可以与 形成稳定的配合。反应
形成稳定的配合。反应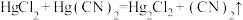 用于制备
用于制备 。
。(1)上述反应的氧化剂是
(2)写出
 的结构简式
的结构简式 的空间构型是
的空间构型是 分子中
分子中 键为
键为(3)
 被称为拟卤素,性质与卤素相似,写出
被称为拟卤素,性质与卤素相似,写出 与氢氧化钠溶液反应的离子方程式
与氢氧化钠溶液反应的离子方程式(4)基态N价层电子排布式为
您最近一年使用:0次
2025高三·全国·专题练习
3 . 回答下列问题。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为___________ ;
②该氯原子的摩尔质量是___________ ;
③m g该氯原子的物质的量为___________ ;
④n g该氯原子所含的电子数为___________ 。
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为___________ ,R的相对原子质量为___________ 。含R的质量为1.6 g的Na2R,其物质的量为___________ 。
(1)某氯原子的质量是a g,12C原子的质量是b g,用NA表示阿伏加德罗常数的值。
①该氯原子的相对原子质量为
②该氯原子的摩尔质量是
③m g该氯原子的物质的量为
④n g该氯原子所含的电子数为
(2)12.4 g Na2R含Na+ 0.4 mol,则Na2R的摩尔质量为
您最近一年使用:0次
2025高三上·全国·专题练习
4 . 一块表面已被氧化为氧化钠的钠块17.0 g,投入50 g水中,最多能产生0.2 g气体,则:
(1)涉及的化学方程式为_______ ,_______ 。
(2)钠块中钠的质量是_______ g。
(3)钠块中氧化钠的质量是_______ g。
(4)原来钠块中被氧化的钠的质量是_______ g。
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是_______ 。
(1)涉及的化学方程式为
(2)钠块中钠的质量是
(3)钠块中氧化钠的质量是
(4)原来钠块中被氧化的钠的质量是
(5)设所得溶液的体积为50 mL,求所得溶液溶质物质的量浓度是
您最近一年使用:0次
2025高三上·全国·专题练习
5 . 某消毒小组人员用18.4mol•L-1的浓硫酸配制500mL0.1mol•L-1的稀硫酸用于84消毒液消毒能力的实验探究,在配制过程中,下列操作中能使所配溶液的浓度偏低的有___________ (填代号)。
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④转移过程中,有少量液体溅出
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
①用量筒量取98%的硫酸时俯视
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③转移前,容量瓶中含有少量蒸馏水
④转移过程中,有少量液体溅出
⑤定容时,加蒸馏水超过标线,又用胶头滴管吸出
您最近一年使用:0次
2025高三·全国·专题练习
解题方法
6 . 请回答下列问题:
(1)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质:
铬铁矿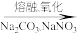 熔块
熔块
该步骤的主要反应为FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为
Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为___________ 。
(2)酸性条件下,MnO(OH)2将I-氧化为I2:MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平)。配平该反应的方程式,其化学计量数依次为___________ 。
(1)重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·Cr2O3,还含有硅、铝等杂质:
铬铁矿
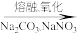 熔块
熔块该步骤的主要反应为FeO·Cr2O3+Na2CO3+NaNO3
 Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为
Na2CrO4+Fe2O3+CO2↑+NaNO2。上述反应配平后FeO·Cr2O3与NaNO3的化学计量数比为(2)酸性条件下,MnO(OH)2将I-氧化为I2:MnO(OH)2+I-+H+→Mn2++I2+H2O(未配平)。配平该反应的方程式,其化学计量数依次为
您最近一年使用:0次
7 . 某试样含有 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗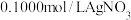 溶液
溶液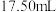 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液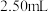 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数_______ 、_______ 。
 、
、 及㤢性物质。称取试样
及㤢性物质。称取试样 ,溶解后配制到
,溶解后配制到 容量瓶中。吸取
容量瓶中。吸取 ,在
,在 介质中用
介质中用 将
将 还原为
还原为 ,除去过量的
,除去过量的 后调至中性测定
后调至中性测定 ,消耗
,消耗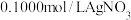 溶液
溶液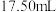 。另吸取
。另吸取 试液用
试液用 酸化后加热除去
酸化后加热除去 ,再调至中性,滴定过剩
,再调至中性,滴定过剩 时消耗了上述
时消耗了上述 溶液
溶液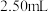 。计算试样中
。计算试样中 、
、 的质量分数
的质量分数
您最近一年使用:0次
2024高三·全国·专题练习
8 . 化学让生活更美好,各类水处理剂能让水源水质得到提升,达到饮用水的标准。生活中较常见的水处理剂有氯气、次氯酸钠、漂白粉(主要成分为次氯酸钙)、二氧化氯、明矾、硫酸铁、高铁酸钠等。
(1)氯气常用于自来水的消毒,请写出氯气溶于水的离子方程式:___________ 。
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.加热时,当NaOH与Cl2反应生成的n(NaClO)∶n(NaClO3)=5∶1时,NaOH与Cl2反应的化学方程式为___________ 。
(3)氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO 、Cl-的转化率与pH关系如图所示。
、Cl-的转化率与pH关系如图所示。___________ 。某工厂污水中含CN-a mg·L-1,现用ClO2将CN-氧化,生成了两种无毒无害的气体,处理50 m3这种污水,至少需要ClO2___________ mol。
(4)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,则Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(1)氯气常用于自来水的消毒,请写出氯气溶于水的离子方程式:
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.加热时,当NaOH与Cl2反应生成的n(NaClO)∶n(NaClO3)=5∶1时,NaOH与Cl2反应的化学方程式为
(3)氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO
 、Cl-的转化率与pH关系如图所示。
、Cl-的转化率与pH关系如图所示。
(4)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,则Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运。通过氨热分解法制取氢气,其反应的化学方程式如下: 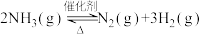
(1)根据下表数据,写出氨热分解法的热化学方程式___________ 。相关化学键的键能数据
(2)已知该反应的∆S=198.9×10-3kJ·mol-1·K-1,判断在300℃时反应是否能自发进行___________ (填“是”或“否”),理由是___________ 。
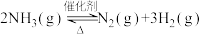
(1)根据下表数据,写出氨热分解法的热化学方程式
| 化学键 | N≡N | H-H | N-H |
| 键能E/(kJ·mol-1) | 946 | 436.0 | 390.8 |
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 黄铁矿[主要成分为二硫化亚铁(FeS2)]、焦炭和适量空气混合加热发生如下反应:
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为___________ mol。
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2.将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g) S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0
iii.SO2(g)+3CO(g) COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0
理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。___________ 。
②随温度升高,S2平衡产率上升,推测其原因是___________ 。
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为___________ 。
i.3FeS2+2C+3O2=3S2+Fe3O4+2CO
(1)反应i生成1molS2时,转移电子的物质的量为
(2)反应i所得气体经冷凝回收S2后,尾气中还含有CO和SO2.将尾气通过催化剂进行处理,发生反应ii,同时发生副反应iii。
ii.2SO2(g)+4CO(g)
 S2(g)+4CO2(g) ΔH<0
S2(g)+4CO2(g) ΔH<0iii.SO2(g)+3CO(g)
 COS(g)+2CO2(g) ΔH<0
COS(g)+2CO2(g) ΔH<0理论分析及实验结果表明,600~1000K范围内,SO2平衡转化率接近100%。其他条件相同,不同温度下,S2、COS平衡产率和10min时S2实际产率如图。
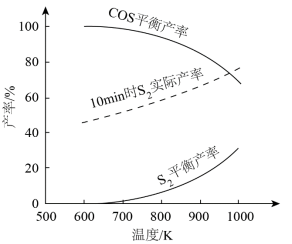
②随温度升高,S2平衡产率上升,推测其原因是
③900K,在10min后继续反应足够长时间,推测S2实际产率的变化趋势可能为
您最近一年使用:0次



