2024高三·上海·专题练习
解题方法
1 . 溴的三种化合物的沸点如下表所示:
解释三种卤化物沸点差异的原因_______ 。
| 溴的卤化物 | AlF3 | AlCl3 | AlBr3 |
| 沸点 | 1500 | 370 | 430 |
您最近一年使用:0次
2024高三·上海·专题练习
2 . 已知反应Al2Br6(l) 2Al(g) +6Br(g) ΔH
2Al(g) +6Br(g) ΔH
①Al2Br6(s) Al2Br6(l) ΔH1
Al2Br6(l) ΔH1
②Al(s) Al(g) ΔH2
Al(g) ΔH2
③Br2(l) Br2(g) ΔH3
Br2(g) ΔH3
④Br2(g) 2Br(g) ΔH4
2Br(g) ΔH4
⑤2Al(s) + 3Br2(l) Al2Br6(s) ΔH5
Al2Br6(s) ΔH5
则ΔH=_______ 。
由图可知,若该反应自发,则该反应的_______ 。
 2Al(g) +6Br(g) ΔH
2Al(g) +6Br(g) ΔH①Al2Br6(s)
 Al2Br6(l) ΔH1
Al2Br6(l) ΔH1②Al(s)
 Al(g) ΔH2
Al(g) ΔH2③Br2(l)
 Br2(g) ΔH3
Br2(g) ΔH3④Br2(g)
 2Br(g) ΔH4
2Br(g) ΔH4⑤2Al(s) + 3Br2(l)
 Al2Br6(s) ΔH5
Al2Br6(s) ΔH5则ΔH=
由图可知,若该反应自发,则该反应的

您最近一年使用:0次
2024高三·上海·专题练习
3 . PtF6是极强的氧化剂,Xe和PtF6可制稀有气体离子化合物。
六氟合铂酸氙([XeF]+[Pt2F11]-)的制备方式如图所示:
2.上述过程中属于氧化还原反应的是_______。
3.氟气通入氙(Xe)会产生XeF2、XeF4、XeF6三种氟化物气体。现将1 mol的Xe和9 mol的F2同时通入50 L的容器中,反应10 min后,测得容器内共有8.9 mol气体,且三种氟化物的比例为XeF2∶XeF4∶XeF6 = 1∶6∶3,则10 min内XeF4的速率v(XeF4) = _______ 。
六氟合铂酸氙([XeF]+[Pt2F11]-)的制备方式如图所示:
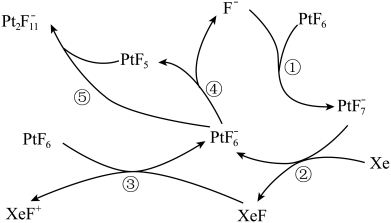
| A.PtF6 | B.PtF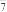 | C.F- | D.XeF+ |
| A.② | B.③ | C.④ | D.⑤ |
您最近一年使用:0次
2024高三·上海·专题练习
4 . 氟单质常温下能腐蚀Fe、Ag等金属,但工业上却可用Cu制容器储存,其原因是_______ 。
您最近一年使用:0次
真题
解题方法
5 . 已知 可二聚为下图的二聚体:
可二聚为下图的二聚体:
(2)将该二聚体溶于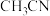 生成
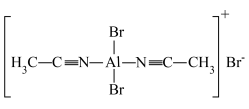
生成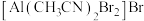 (结构如图所示),已知其配离子为四面体形,中心原子杂化方式为
(结构如图所示),已知其配离子为四面体形,中心原子杂化方式为_______ ,其中配体是_______ , 该配合物中有
该配合物中有 键
键_______  。
。
 可二聚为下图的二聚体:
可二聚为下图的二聚体: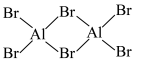
| A.极性键 | B.非极性键 | C.离子键 | D.金属键 |
(2)将该二聚体溶于
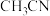 生成
生成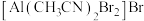 (结构如图所示),已知其配离子为四面体形,中心原子杂化方式为
(结构如图所示),已知其配离子为四面体形,中心原子杂化方式为 该配合物中有
该配合物中有 键
键 。
。
您最近一年使用:0次
真题
解题方法
6 . 液态氟化氢(HF)的电离方式为: ,其中X为
,其中X为_______ 。 的结构为
的结构为 ,其中
,其中 与HF依靠
与HF依靠_______ 相连接。
 ,其中X为
,其中X为 的结构为
的结构为 ,其中
,其中 与HF依靠
与HF依靠
您最近一年使用:0次
7 . 萤石( )与浓硫酸共热可制备HF气体,写出该反应的化学方程式:
)与浓硫酸共热可制备HF气体,写出该反应的化学方程式:_______ ,该反应中体现浓硫酸的性质是_______ 。
A.强氧化性 B.难挥发性 C.吸水性 D.脱水性
 )与浓硫酸共热可制备HF气体,写出该反应的化学方程式:
)与浓硫酸共热可制备HF气体,写出该反应的化学方程式:A.强氧化性 B.难挥发性 C.吸水性 D.脱水性
您最近一年使用:0次
8 . 过渡元素镍钛在分子捕捉、量子材料等方向日益重要。回答下列问题:
(1)某Ni离子与 、
、 形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为
形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为______ ,Ni的化合价为______ ,杂化轨道数为______ 。 与Ni离子形成配位键时的配位原子为
与Ni离子形成配位键时的配位原子为______ ,键角∠H-N-H______ (填“>”或“<”)107.3°。
(2)部分钛酸锶晶胞结构如图乙。晶体Ⅰ的化学式为Ⅰ_____ ,该系列晶体的化学式可表示为_____ (用含n的式子表示,n为Ti原子个数),当 时,晶体化学式为
时,晶体化学式为______ 。
(1)某Ni离子与
 、
、 形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为
形成的晶体能捕捉苯分子,结构如图甲所示。该晶体中非金属元素电负性由大到小的顺序为 与Ni离子形成配位键时的配位原子为
与Ni离子形成配位键时的配位原子为(2)部分钛酸锶晶胞结构如图乙。晶体Ⅰ的化学式为Ⅰ
 时,晶体化学式为
时,晶体化学式为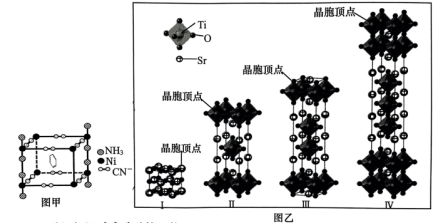
您最近一年使用:0次
2024高三·全国·专题练习
9 . 化学让生活更美好,各类水处理剂能让水源水质得到提升,达到饮用水的标准。生活中较常见的水处理剂有氯气、次氯酸钠、漂白粉(主要成分为次氯酸钙)、二氧化氯、明矾、硫酸铁、高铁酸钠等。
(1)氯气常用于自来水的消毒,请写出氯气溶于水的离子方程式:___________ 。
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.加热时,当NaOH与Cl2反应生成的n(NaClO)∶n(NaClO3)=5∶1时,NaOH与Cl2反应的化学方程式为___________ 。
(3)氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO 、Cl-的转化率与pH关系如图所示。
、Cl-的转化率与pH关系如图所示。___________ 。某工厂污水中含CN-a mg·L-1,现用ClO2将CN-氧化,生成了两种无毒无害的气体,处理50 m3这种污水,至少需要ClO2___________ mol。
(4)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,则Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(1)氯气常用于自来水的消毒,请写出氯气溶于水的离子方程式:
(2)氯气能用于制备易于保存、使用方便的漂白液,但若温度过高会发生副反应生成NaCl、NaClO3.加热时,当NaOH与Cl2反应生成的n(NaClO)∶n(NaClO3)=5∶1时,NaOH与Cl2反应的化学方程式为
(3)氯气消毒时,会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此人们已开始研究并试用新的自来水消毒剂,如二氧化氯(ClO2)、臭氧等。ClO2被世界卫生组织(WHO)列为A级高效、安全灭菌消毒剂,将逐渐取代Cl2成为自来水的消毒剂。ClO2气体具有强氧化性,其还原产物ClO
 、Cl-的转化率与pH关系如图所示。
、Cl-的转化率与pH关系如图所示。
(4)高铁酸钠(Na2FeO4)在水中既能消毒杀菌,其产物Fe(OH)3胶体又能净水除去悬浮杂质,是一种理想的水处理剂。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,则Cl2、ClO2(pH≤2时)、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运。通过氨热分解法制取氢气,其反应的化学方程式如下: 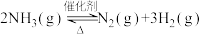
(1)根据下表数据,写出氨热分解法的热化学方程式___________ 。相关化学键的键能数据
(2)已知该反应的∆S=198.9×10-3kJ·mol-1·K-1,判断在300℃时反应是否能自发进行___________ (填“是”或“否”),理由是___________ 。
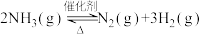
(1)根据下表数据,写出氨热分解法的热化学方程式
| 化学键 | N≡N | H-H | N-H |
| 键能E/(kJ·mol-1) | 946 | 436.0 | 390.8 |
您最近一年使用:0次



