解题方法
1 . 化学电池的发明,是贮能和供能技术的巨大进步。
(1)如图所示装置中, 片是
片是_______ (填“正极”或“负极”),该极的电极反应式_______ 。_______ (写化学方程式)反应释放的能量直接转变为电能;能证明化学能转化为电能的实验现象是:电流表指针偏转、铜片上_______ 。
(1)如图所示装置中,
 片是
片是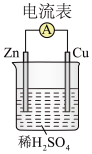
您最近一年使用:0次
名校
2 . 如图是氮元素的各种价态与物质类别的对应关系:_____ 。从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的化合物有_______ 。
(2)实验室将浓氨水加入生石灰中可以快速制取NH3的化学方程式为_________ 。
(3)浓硝酸、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应使用___________ 。
(4)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为_____________ 。

(2)实验室将浓氨水加入生石灰中可以快速制取NH3的化学方程式为
(3)浓硝酸、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应使用
(4)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为
您最近一年使用:0次
3 . 为解决二氧化碳的过量排放带来的气候变暖、海洋酸化的负面效应,二氧化碳的捕集及转化成为高价值的低碳烯烃已成为热门的科研项目。回答下列问题:
I.高温条件下二氧化碳可以氢化制备乙烯。
(1)已知下列反应的热化学方程式:
i. ;
;
ii.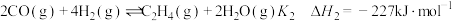 ;
;
反应iii: 的
的
_______  ,平衡常数
,平衡常数
_______ (用 、
、 表示)。
表示)。
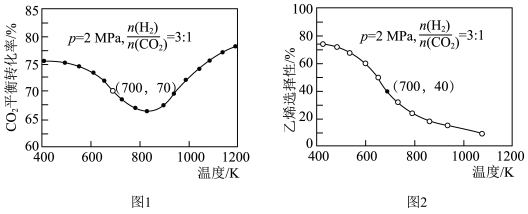
(2)研究表明,合成气体在 、起始
、起始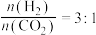 时,
时, 平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性
平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性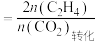 ]:
]: 平衡转化率随温度升高出现先下降后升高可能的原因是
平衡转化率随温度升高出现先下降后升高可能的原因是_______ 。
②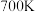 时,反应i的
时,反应i的
_______ (列出计算式即可)。
(3)关于上述反应,下列说法正确的是_______(填选项字母)。
II.二氧化碳电催化还原制乙烯。
(4)科学家研究利用电催化还原 制乙烯,其工作原理如图所示,涂有
制乙烯,其工作原理如图所示,涂有 催化剂的铜电极作阴极,阴极的电极反应式为
催化剂的铜电极作阴极,阴极的电极反应式为_______ ;当阴极生成 气体时,理论上阳极生成气体的物质的量为
气体时,理论上阳极生成气体的物质的量为_______ 。
I.高温条件下二氧化碳可以氢化制备乙烯。
(1)已知下列反应的热化学方程式:
i.
 ;
;ii.
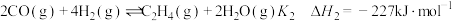 ;
;反应iii:
 的
的
 ,平衡常数
,平衡常数
 、
、 表示)。
表示)。(2)研究表明,合成气体在
 、起始
、起始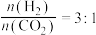 时,
时, 平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性
平衡转化率随温度的变化如图1所示,乙烯选择性随温度的变化如图2所示[乙烯选择性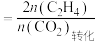 ]:
]:
 平衡转化率随温度升高出现先下降后升高可能的原因是
平衡转化率随温度升高出现先下降后升高可能的原因是②
 时,反应i的
时,反应i的
(3)关于上述反应,下列说法正确的是_______(填选项字母)。
A.提高投料比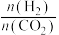 , , 的平衡转化率减小 的平衡转化率减小 |
| B.使用高效催化剂可提高平衡时乙烯的体积分数 |
| C.若在恒容、绝热容器中进行,温度不变则反应达到平衡 |
D.体系内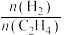 比值不变反应达到平衡状态 比值不变反应达到平衡状态 |
II.二氧化碳电催化还原制乙烯。
(4)科学家研究利用电催化还原
 制乙烯,其工作原理如图所示,涂有
制乙烯,其工作原理如图所示,涂有 催化剂的铜电极作阴极,阴极的电极反应式为
催化剂的铜电极作阴极,阴极的电极反应式为 气体时,理论上阳极生成气体的物质的量为
气体时,理论上阳极生成气体的物质的量为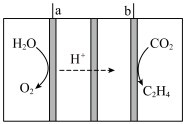
您最近一年使用:0次
4 . 二氧化氯(ClO2)是国际公认的广谱、高效和安全的杀菌剂。
(1)制备C1O2的一种方法是在酸性条件下用草酸(碳的价态+3价)和氯酸钠反应,配平该反应的化学方程式,并标出电子转移的方向和数目:________ 。
_____H2C2O4+_____NaClO3+____H2SO4→_____ Na2SO4+___CO2↑+_____ClO2↑+___ H2O
(2)上述反应中被氧化的元素是____ ,氧化产物是_____ 。
(3)若反应中生成1.12L(标况) ClO2,转移电子数目为________ 。
(4)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,计算ClO2的消毒能力是等质量Cl2的_____ 倍(保留2位小数)。
(5)若以NaClO2为原料制备ClO2,需要加入具有____ (填“氧化性”或“还原性”)的物质。
(1)制备C1O2的一种方法是在酸性条件下用草酸(碳的价态+3价)和氯酸钠反应,配平该反应的化学方程式,并标出电子转移的方向和数目:
_____H2C2O4+_____NaClO3+____H2SO4→_____ Na2SO4+___CO2↑+_____ClO2↑+___ H2O
(2)上述反应中被氧化的元素是
(3)若反应中生成1.12L(标况) ClO2,转移电子数目为
(4)ClO2具有强氧化性,若ClO2和Cl2在消毒时自身均被还原为Cl-,计算ClO2的消毒能力是等质量Cl2的
(5)若以NaClO2为原料制备ClO2,需要加入具有
您最近一年使用:0次
名校
解题方法
5 . 实验室用石墨电极电解加有酚酞的饱和NaCl溶液,装置如图1所示。氯碱工业用图2所示装置制备NaOH等工业原料。
(1)a为电解池的_____ 极,a处的电极反应式为________ 。
(2)该电解池中发生的总反应的化学方程式为____________ 。
(3)下列与电解饱和食盐水有关的说法,正确的是________ (填字母)。
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.a电极附近溶液变红
Ⅱ.利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如上图2所示。
(4)气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是______ ,气体Y是____ 。
(5)阳离子交换膜避免了Cl2与NaOH发生反应,写出Cl2 与NaOH常温下反应的离子方程式__________ 。
(6)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3混合溶液,经测定ClO-、 的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原与被氧化的氯元素的物质的量之比为_____。
的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原与被氧化的氯元素的物质的量之比为_____。
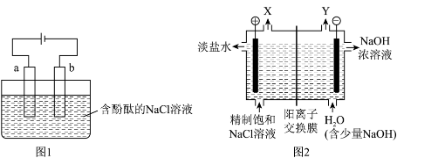
(1)a为电解池的
(2)该电解池中发生的总反应的化学方程式为
(3)下列与电解饱和食盐水有关的说法,正确的是
A.通电使NaCl发生电离
B.在溶液中,阴离子向电极a移动
C.a电极附近溶液变红
Ⅱ.利用实验室装置制备NaOH,不仅有安全隐患,而且存在Cl2与NaOH的副反应,氯碱工业采用改进后的装置,如上图2所示。
(4)气体X和气体Y被阳离子交换膜分隔开,避免混合爆炸。气体X是
(5)阳离子交换膜避免了Cl2与NaOH发生反应,写出Cl2 与NaOH常温下反应的离子方程式
(6)某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3混合溶液,经测定ClO-、
 的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原与被氧化的氯元素的物质的量之比为_____。
的浓度之比为1:3,则Cl2与NaOH溶液反应时被还原与被氧化的氯元素的物质的量之比为_____。| A.21:5 | B.4:1 | C.3:1 | D.11:3 |
您最近一年使用:0次
名校
解题方法
6 . 2016年IUPAC确认了四种新元素,其中一种为Mc,中文名为“镆”元素Mc可由反应: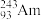 +
+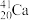 =
=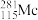 +3
+3 得到。
得到。
(1)该元素的质子数为___________ 。287Mc与288Mc互为________ 。
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:__________ ,该分子内存在的共价键类型有___________ 。
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为_______ ,+5价简单含氧酸的化学式为_________ 。
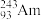 +
+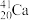 =
=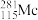 +3
+3 得到。
得到。(1)该元素的质子数为
(2)Mc位于元素周期表中第ⅤA族,同族元素N的一种氢化物为H2N-NH2,写出该化合物分子的电子式:
(3)该族中的另一元素P能呈现多种化合价,其中+3价氧化物的化学式为
您最近一年使用:0次
2024·上海·模拟预测
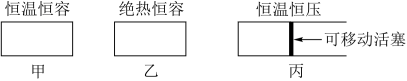
7 . 某研究组模拟三种已装固体V2O5催化剂的密闭容器装置,发生的反应为:2SO2(g)+O2(g) 2SO3(g) ΔH1=-197.7kJ·mol-1
2SO3(g) ΔH1=-197.7kJ·mol-1
(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2molSO2、1molO2投料,达平衡时;三个容器中SO2的转化率从大到小的顺序为___________ (用“甲、乙、丙”表示)。
(3)400℃,在容器丙中投入4molSO2、2molO2进行反应时,放出akJ热量;若在500℃,投入2molSO2、1molO2进行反应,放出bkJ热量,则a___________ 2b(填“﹥”、“﹤”或“=”)。
 2SO3(g) ΔH1=-197.7kJ·mol-1
2SO3(g) ΔH1=-197.7kJ·mol-1(1)在初始体积与温度相同的条件下,甲、乙、丙中均按2molSO2、1molO2投料,达平衡时;三个容器中SO2的转化率从大到小的顺序为
| A.温度不变 | B.密度保持不变 | C.压强保持不变 | D.O2浓度保持不变 |
(3)400℃,在容器丙中投入4molSO2、2molO2进行反应时,放出akJ热量;若在500℃,投入2molSO2、1molO2进行反应,放出bkJ热量,则a
您最近一年使用:0次
2024·上海·模拟预测
8 .  与环氧丙烷(
与环氧丙烷( )在一定条件下反应制得碳酸丙烯酯。
)在一定条件下反应制得碳酸丙烯酯。
 是
是(2)环氧丙烷中,O原子的杂化轨道类型是
(3)沸点:环氧丙烷
 (填“>”或“<”),解释其原因:
(填“>”或“<”),解释其原因:
您最近一年使用:0次
9 . 锑白 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的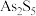 、
、 、
、 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: 、
、 、
、 、
、 、
、 、
、 、
、 ;
;
② ,
, 。
。
回答下列问题:
(1)粉碎辉锑矿的目的是_______ 。
(2)滤渣I的成分除不溶性杂质外还有PbS、S、_______ (填化学式)。 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为_______ 。
(3)“除砷”时氧化剂与还原剂的物质的量之比为_______ (P转化为最高价态)。
(4)若浸取液 、
、 浓度均为
浓度均为 ,
,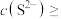
_______  才能使二者完全沉淀(当离子浓度
才能使二者完全沉淀(当离子浓度 时认为沉淀完全),此时
时认为沉淀完全),此时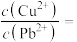
_______ 。
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:_______ ;随温度升高,脱氯率降低可能的原因为_______ 。
 是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为
是优良的无机白色颜料,可用作阻燃剂、催化剂、油漆等。一种采用辉锑矿(主要成分为 ,含少量的
,含少量的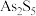 、
、 、
、 和
和 等)提取锑白的工艺流程如图所示:
等)提取锑白的工艺流程如图所示: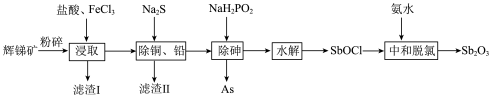
 、
、 、
、 、
、 、
、 、
、 、
、 ;
;②
 ,
, 。
。回答下列问题:
(1)粉碎辉锑矿的目的是
(2)滤渣I的成分除不溶性杂质外还有PbS、S、
 在“浸取”时发生反应的离子方程式为
在“浸取”时发生反应的离子方程式为(3)“除砷”时氧化剂与还原剂的物质的量之比为
(4)若浸取液
 、
、 浓度均为
浓度均为 ,
,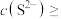
 才能使二者完全沉淀(当离子浓度
才能使二者完全沉淀(当离子浓度 时认为沉淀完全),此时
时认为沉淀完全),此时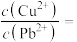
(5)“中和脱氯”时脱氯率与反应温度的关系如图所示:

您最近一年使用:0次
名校
10 . 按要求完成下列试题:
(1)新戊烷用系统命名法时的名称:____________ 。
(2)写出乙炔和溴水按物质的量之比为1:1反应的化学方程式:____________ 。
(3)工业合成氨的化学方程式:____________ 。
(4)铁和稀硝酸按物质的量之比为1:1反应的离子方程式:____________ 。
(5)分子式为C6H14的烃结构中含有4个甲基,且一氯代物只有两种的结构简式为:____________ 。
(1)新戊烷用系统命名法时的名称:
(2)写出乙炔和溴水按物质的量之比为1:1反应的化学方程式:
(3)工业合成氨的化学方程式:
(4)铁和稀硝酸按物质的量之比为1:1反应的离子方程式:
(5)分子式为C6H14的烃结构中含有4个甲基,且一氯代物只有两种的结构简式为:
您最近一年使用:0次



