1 . 赤铜矿(主要成分为 ,含少量
,含少量 、
、 )含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备
)含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备 晶体的流程为:
晶体的流程为:
(1) 晶体结构如下图所示。晶体中存在的作用力包括离子键、
晶体结构如下图所示。晶体中存在的作用力包括离子键、_______ 。_______ 。 发生反应的离子方程式为
发生反应的离子方程式为_______ 。检验氧化完全的试剂为_______ (填化学式)。
(4)沉铁。离子浓度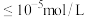 时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则
时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则 的
的 为
为_______ 。
(5)试从产率、试剂选择角度评价该制备流程并提出修改建议_______ 。
 ,含少量
,含少量 、
、 )含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备
)含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备 晶体的流程为:
晶体的流程为:

(1)
 晶体结构如下图所示。晶体中存在的作用力包括离子键、
晶体结构如下图所示。晶体中存在的作用力包括离子键、

 发生反应的离子方程式为
发生反应的离子方程式为(4)沉铁。离子浓度
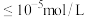 时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则
时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则 的
的 为
为(5)试从产率、试剂选择角度评价该制备流程并提出修改建议
您最近一年使用:0次
名校
2 . 按照要求填空
(1)现有下列各组物质:① 和
和 、②
、②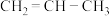 和
和 、③
、③ 和
和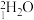 、④
、④ 和
和 、⑤
、⑤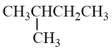 和
和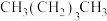 、⑥
、⑥ 和
和 、⑦
、⑦ 和
和
属于同系物的是___________ (填序号)。
(2)把下列物质的沸点按由高到低的顺序排列___________ 。(填入编号)
①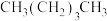 ②
②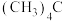 ③十一烷④
③十一烷④
(3)戊烷的同分异构体有___________ 种
(4)已知乳酸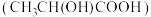 是身体代谢产物之一,该物质所含官能团的名称
是身体代谢产物之一,该物质所含官能团的名称___________ 。 乳酸分别与足量
乳酸分别与足量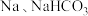 反应产生气体体积之比为:
反应产生气体体积之比为:___________ 。
(5)某有机物的键线式为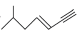 该分子最多有
该分子最多有___________ 个碳原子共面,最多有___________ 个碳原子共线。
(1)现有下列各组物质:①
 和
和 、②
、②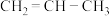 和
和 、③
、③ 和
和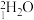 、④
、④ 和
和 、⑤
、⑤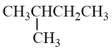 和
和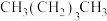 、⑥
、⑥ 和
和 、⑦
、⑦ 和
和
属于同系物的是
(2)把下列物质的沸点按由高到低的顺序排列
①
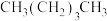 ②
②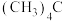 ③十一烷④
③十一烷④
(3)戊烷的同分异构体有
(4)已知乳酸
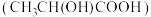 是身体代谢产物之一,该物质所含官能团的名称
是身体代谢产物之一,该物质所含官能团的名称 乳酸分别与足量
乳酸分别与足量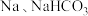 反应产生气体体积之比为:
反应产生气体体积之比为:(5)某有机物的键线式为
 该分子最多有
该分子最多有
您最近一年使用:0次
名校
3 . 按要求回答下列问题:
(1)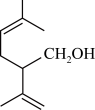 的分子式为
的分子式为___________ ,所含官能团的名称为___________ 。
(2) 分子中有
分子中有___________ 个碳原子共平面,最多有___________ 个原子共平面。
(3)有机物X的分子式为 ,已知:
,已知: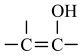 结构极不稳定。
结构极不稳定。
①若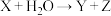 且Y最终能通过氧化反应转化为Z,则X的结构简式为
且Y最终能通过氧化反应转化为Z,则X的结构简式为___________ ,该物质的核磁共振氢谱有___________ 组峰。
②若X能与NaOH溶液发生中和反应,且分子中含有2个官能团,则核磁共振氢谱有三组峰的物质的结构简式可能为___________ (写出一种)。
③若X能发生银镜反应,且 最多可还原出
最多可还原出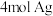 ,则相应的四元环化合物共有
,则相应的四元环化合物共有___________ 种,写出X(官能团以外的原子均用R表示)与新制的 浊液反应的方程式:
浊液反应的方程式:___________ 。
(1)
 的分子式为
的分子式为(2)
 分子中有
分子中有(3)有机物X的分子式为
 ,已知:
,已知: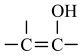 结构极不稳定。
结构极不稳定。①若
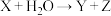 且Y最终能通过氧化反应转化为Z,则X的结构简式为
且Y最终能通过氧化反应转化为Z,则X的结构简式为②若X能与NaOH溶液发生中和反应,且分子中含有2个官能团,则核磁共振氢谱有三组峰的物质的结构简式可能为
③若X能发生银镜反应,且
 最多可还原出
最多可还原出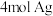 ,则相应的四元环化合物共有
,则相应的四元环化合物共有 浊液反应的方程式:
浊液反应的方程式:
您最近一年使用:0次
解题方法
4 . 现有下列几种有机物或微粒:
(1)上述物质中属于芳香烃的是________ (填编号,下同),互为同分异构体的是_________ 。
(2)④与等物质的量的HBr发生加成反应的产物可能为___________ (填结构简式)。
(3)⑧中只含碳、氢、氧三种元素,其分子结构模型中小球表示原子,球与球之间的短线代表单键或双键。⑧中所含官能团的名称为___________ 。
(4)⑤的一种同分异构体B为芳香族化合物,其核磁共振氢谱图如图所示:___________ ,下列关于B的说法正确的是___________ (填字母)。
A.该物质可与氢气反应,1mol该物质最多消耗氢气的物质的量为4mol
B.在光照条件下,该物质可以和氯水发生取代反应
C.该物质可以使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,均发生氧化反应
(5)⑦是最简单的碳正离子,它的中心原子的杂化方式为___________ ; 并不稳定,原因是
并不稳定,原因是___________ 。
①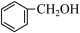 ②
②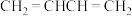 ③
③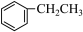 ④
④ ⑤
⑤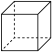 ⑥
⑥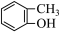 ⑦
⑦ ⑧
⑧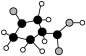
(1)上述物质中属于芳香烃的是
(2)④与等物质的量的HBr发生加成反应的产物可能为
(3)⑧中只含碳、氢、氧三种元素,其分子结构模型中小球表示原子,球与球之间的短线代表单键或双键。⑧中所含官能团的名称为
(4)⑤的一种同分异构体B为芳香族化合物,其核磁共振氢谱图如图所示:

A.该物质可与氢气反应,1mol该物质最多消耗氢气的物质的量为4mol
B.在光照条件下,该物质可以和氯水发生取代反应
C.该物质可以使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,均发生氧化反应
(5)⑦是最简单的碳正离子,它的中心原子的杂化方式为
 并不稳定,原因是
并不稳定,原因是
您最近一年使用:0次
名校
解题方法
5 . 人类的一切活动都离不开能量,而许多能量的利用与化学反应中的能量变化密切相关。回答下列问题。
(1)在2.0L恒温恒容密闭容器中充入2.0 mol N2和6.0 mol H2,发生反应: ,反应至t min时测得H2的物质的量为3.6 mol。
,反应至t min时测得H2的物质的量为3.6 mol。
①0~t min内,平均反应速率v(NH3)=_______ mol·L-1·min-1(用含t的代数式表示)。
②反应至t min时,容器内压强与反应初始时压强之比为_______ 。
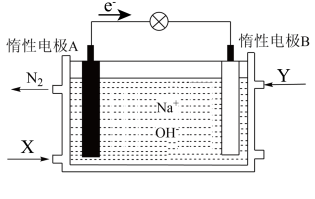
(2)将燃料和氧化剂的化学能直接转化为电能的电化学反应装置称作燃料电池。肼(N2H4,N呈-2价)—过氧化氢(H2O2)碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示,已知电池总反应式为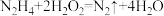 。
。_____ (填“正”或“负”)极,物质X是____ (填“N2H4”或“H2O2”)。
②电极B上的电极反应式为____ ,电池工作时,OH-流向_____ (填“电极A”或“电极B”)。
③电池工作过程中,若A极区产生14g N2,则转移的电子数目为______ (用阿伏加德罗常数的值NA表示)。
(1)在2.0L恒温恒容密闭容器中充入2.0 mol N2和6.0 mol H2,发生反应:
 ,反应至t min时测得H2的物质的量为3.6 mol。
,反应至t min时测得H2的物质的量为3.6 mol。①0~t min内,平均反应速率v(NH3)=
②反应至t min时,容器内压强与反应初始时压强之比为
(2)将燃料和氧化剂的化学能直接转化为电能的电化学反应装置称作燃料电池。肼(N2H4,N呈-2价)—过氧化氢(H2O2)碱性燃料电池由于其较高的能量密度而备受关注,其工作原理如图所示,已知电池总反应式为
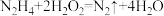 。
。
②电极B上的电极反应式为
③电池工作过程中,若A极区产生14g N2,则转移的电子数目为
您最近一年使用:0次
解题方法
6 . 咔唑( )是一种新型有机液体储氢材料,其分子式为
)是一种新型有机液体储氢材料,其分子式为 。
。
(2)写出一个能比较碳和氮非金属性强弱的化学方程式:
您最近一年使用:0次
名校
解题方法
7 . 现代社会的一切活动都离不开能源,为了更好的利用化学反应中的物质和能量变化,需要关注化学反应的快慢和程度。
Ⅰ.化学变化过程中均存在物质变化与能量变化,某化学兴趣小组进行如图1所示实验,以验证此结论。请回答下列问题。___________ 生成物成键释放的能量 填“大于”或“小于”
填“大于”或“小于” ;反应②中,反应物的总能量
;反应②中,反应物的总能量___________ 生成物的总能量 填“高于”或“低于”
填“高于”或“低于” 。
。
Ⅱ.某小组利用Na2S2O3溶液和稀硫酸的反应,通过比较反应完全所用时间长短验证不同因素对化学反应速率的影响。实验设计如表所示:
(2) 和稀硫酸反应的离子方程式为
和稀硫酸反应的离子方程式为___________ 。
(3)依据化学反应原理判断平均用时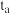
___________ 5(填“>”“=”或“<”)。
(4)通过对比实验a和c,验证稀 的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案
的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案___________ 。
Ⅲ.某同学用等质量的锌粉先后与盐酸及相同体积、未知浓度的盐酸反应,记录相关数据,并作出这两个反应过程中放出气体的体积随反应时间的变化曲线图(如图2所示)。___________  (填“>”“=”或“<”),若用
(填“>”“=”或“<”),若用 硫酸代替上述实验中的
硫酸代替上述实验中的 盐酸,二者的反应速率是否相同?理由是
盐酸,二者的反应速率是否相同?理由是___________ 。
(6)为控制反应速率,防止因反应过快而难以测量 体积,且不改变生成
体积,且不改变生成 的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。
的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。
Ⅰ.化学变化过程中均存在物质变化与能量变化,某化学兴趣小组进行如图1所示实验,以验证此结论。请回答下列问题。

 填“大于”或“小于”
填“大于”或“小于” ;反应②中,反应物的总能量
;反应②中,反应物的总能量 填“高于”或“低于”
填“高于”或“低于” 。
。Ⅱ.某小组利用Na2S2O3溶液和稀硫酸的反应,通过比较反应完全所用时间长短验证不同因素对化学反应速率的影响。实验设计如表所示:
| 实验编号 |  |  溶液 溶液 | 稀 溶液 溶液 | 反应完全所用时间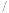 秒 秒 | ||
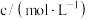 |  | 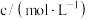 |  | s | ||
| a | 298 | 0.1 | 10 | 0 | 10 | 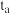 |
| b | 323 | 0.1 | 10 | 0.2 | 10 | 5 |
| c | 298 | 0.1 | 10 | 0.2 | 5 | 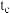 |
(2)
 和稀硫酸反应的离子方程式为
和稀硫酸反应的离子方程式为(3)依据化学反应原理判断平均用时
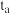
(4)通过对比实验a和c,验证稀
 的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案
的浓度对反应速率的影响。该小组发现实验c存在不科学性,请提出对实验c的改进方案Ⅲ.某同学用等质量的锌粉先后与盐酸及相同体积、未知浓度的盐酸反应,记录相关数据,并作出这两个反应过程中放出气体的体积随反应时间的变化曲线图(如图2所示)。
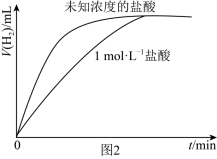
 (填“>”“=”或“<”),若用
(填“>”“=”或“<”),若用 硫酸代替上述实验中的
硫酸代替上述实验中的 盐酸,二者的反应速率是否相同?理由是
盐酸,二者的反应速率是否相同?理由是(6)为控制反应速率,防止因反应过快而难以测量
 体积,且不改变生成
体积,且不改变生成 的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。
的量,事先在盐酸中加入等体积的下列溶液以减慢反应速率。下列试剂中,不可行的是___________。| A.蒸馏水 | B. 溶液 溶液 | C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
8 . 亚硝酸钠( )是一种常用工业盐,具备多种用途,回答下列问题:
)是一种常用工业盐,具备多种用途,回答下列问题:
(1) 中N元素的化合价为
中N元素的化合价为_____ 。
(2)误食 能致人中毒,其中毒机制是把人血红蛋白内的
能致人中毒,其中毒机制是把人血红蛋白内的 转化为
转化为 ,这说明
,这说明 具有
具有_____ 性;服用维生素C可以缓解 中毒状况,这说明维生素C具有
中毒状况,这说明维生素C具有_____ 性;下列物质中能实现 转化为
转化为 的物质是
的物质是_____ (填字母)。
a. b.
b. c.Fe
c.Fe
(3)将 和NO按1∶1的比例通入NaOH溶液中可制得
和NO按1∶1的比例通入NaOH溶液中可制得 此反应的离子方程式为
此反应的离子方程式为_____ 。
(4)为了防止钢铁零件生锈,工厂常用 使钢铁零件表面生成致密保护层,处理过程中的一步反应为
使钢铁零件表面生成致密保护层,处理过程中的一步反应为 (亚铁酸钠)+
(亚铁酸钠)+_____ 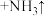 (未配平),请将上述反应中各物质的化学计量系数配平:
(未配平),请将上述反应中各物质的化学计量系数配平:_____ 。
_____Fe+_____ _____NaOH→_____
_____NaOH→_____ _____+_____
_____+_____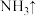 。
。
 )是一种常用工业盐,具备多种用途,回答下列问题:
)是一种常用工业盐,具备多种用途,回答下列问题:(1)
 中N元素的化合价为
中N元素的化合价为(2)误食
 能致人中毒,其中毒机制是把人血红蛋白内的
能致人中毒,其中毒机制是把人血红蛋白内的 转化为
转化为 ,这说明
,这说明 具有
具有 中毒状况,这说明维生素C具有
中毒状况,这说明维生素C具有 转化为
转化为 的物质是
的物质是a.
 b.
b. c.Fe
c.Fe(3)将
 和NO按1∶1的比例通入NaOH溶液中可制得
和NO按1∶1的比例通入NaOH溶液中可制得 此反应的离子方程式为
此反应的离子方程式为(4)为了防止钢铁零件生锈,工厂常用
 使钢铁零件表面生成致密保护层,处理过程中的一步反应为
使钢铁零件表面生成致密保护层,处理过程中的一步反应为 (亚铁酸钠)+
(亚铁酸钠)+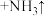 (未配平),请将上述反应中各物质的化学计量系数配平:
(未配平),请将上述反应中各物质的化学计量系数配平:_____Fe+_____
 _____NaOH→_____
_____NaOH→_____ _____+_____
_____+_____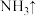 。
。
您最近一年使用:0次
名校
9 . 完成下列问题。
(1)中科院的科研人员在Na−Fe3O4和HMCM−22的表面将CO2转化为烷烃,其过程如图。___________ 。
②写出X的所有同分异构体的结构简式___________ 。
③关于X和Y的说法正确的是___________ (填字母)。
A.最简式相同 B.都易使酸性KMnO4溶液褪色
C.都有4种一氯代物 D.X和Y互称同分异构体
(2)“立方烷”是一种人工合成的烃,其分子为正方体结构,其碳架结构如图所示。___________ ;“立方烷”有多种同分异构体,其中一种属于芳香烃的同分异构体的结构简式是___________ 。
②“立方烷”的二氯代物具有同分异构体的数目是___________ 。
(1)中科院的科研人员在Na−Fe3O4和HMCM−22的表面将CO2转化为烷烃,其过程如图。

②写出X的所有同分异构体的结构简式
③关于X和Y的说法正确的是
A.最简式相同 B.都易使酸性KMnO4溶液褪色
C.都有4种一氯代物 D.X和Y互称同分异构体
(2)“立方烷”是一种人工合成的烃,其分子为正方体结构,其碳架结构如图所示。

②“立方烷”的二氯代物具有同分异构体的数目是
您最近一年使用:0次
名校
解题方法
10 . 研究不同价态硫元素之间的转化是合理利用硫元素的基本途径。回答下列问题:
I.如图是硫元素的“价—类”二维图。___________ ; 属于
属于___________ (填“酸性氧化物”或“碱性氧化物”)。
(2) 的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是___________(填字母)。
的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是___________(填字母)。
(3) 易被氧化而变质,验证其已变质的实验操作及现象是
易被氧化而变质,验证其已变质的实验操作及现象是___________ 。
II.某化学兴趣小组,设计如图实验装置(夹持装置已省略),验证 的部分性质。
的部分性质。___________ 。
(5)装置A中发生反应的化学方程式为___________ ,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(6)装置B中湿润的品红溶液褪色,证明 有
有___________ (填“漂白性”或“氧化性”);装置C中产生白色沉淀,该白色沉淀为___________ (填化学式)。
(7)装置D中产生黄色浑浊,发生反应的离子方程式为___________ ( 过量)。
过量)。
I.如图是硫元素的“价—类”二维图。

 属于
属于(2)
 的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是___________(填字母)。
的过度排放易造成硫酸型酸雨,减少酸雨的产生可采取的措施是___________(填字母)。| A.把工厂烟囱造高 | B.煤使用之前先脱硫 |
| C.逐渐用新能源代替含硫煤 | D.加强空气中二氧化硫的监测 |
(3)
 易被氧化而变质,验证其已变质的实验操作及现象是
易被氧化而变质,验证其已变质的实验操作及现象是II.某化学兴趣小组,设计如图实验装置(夹持装置已省略),验证
 的部分性质。
的部分性质。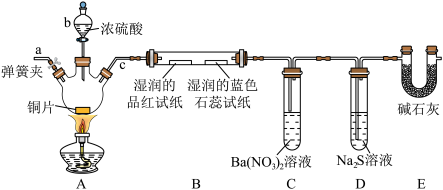
(5)装置A中发生反应的化学方程式为
(6)装置B中湿润的品红溶液褪色,证明
 有
有(7)装置D中产生黄色浑浊,发生反应的离子方程式为
 过量)。
过量)。
您最近一年使用:0次

 2
2

