名校
1 . 一定条件下,在体积为 的密闭容器中发生反应
的密闭容器中发生反应 ,
, 的物质的量与时间变化图象如图:
的物质的量与时间变化图象如图: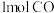 和
和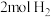 ,则达平行时,CO和
,则达平行时,CO和 的转化率之比为
的转化率之比为________ ;
(2)若起始时加入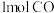 和
和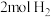 ,达平衡后,使容器内物质全部发生完全燃烧,将产物通过足量的
,达平衡后,使容器内物质全部发生完全燃烧,将产物通过足量的 固体,则固体增重
固体,则固体增重________ ;
(3)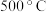 时,从反应开始到达到化学平衡,以
时,从反应开始到达到化学平衡,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是________ ;(用 ,
, 表示)
表示)
(4) 时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是
时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是________ ;
a. 的物质的量增加
的物质的量增加
b.正反应速率加快,逆反应速率减慢
c.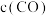 和
和 均减小
均减小
d.重新平衡时 减小
减小
(5)向含有 和
和 的稀溶液中加入足量的铁屑,最终产生气体的物质的量为
的稀溶液中加入足量的铁屑,最终产生气体的物质的量为________ ,溶解铁屑的质量为________ g。
 的密闭容器中发生反应
的密闭容器中发生反应 ,
, 的物质的量与时间变化图象如图:
的物质的量与时间变化图象如图: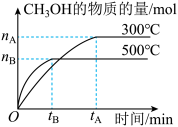
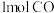 和
和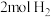 ,则达平行时,CO和
,则达平行时,CO和 的转化率之比为
的转化率之比为(2)若起始时加入
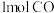 和
和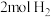 ,达平衡后,使容器内物质全部发生完全燃烧,将产物通过足量的
,达平衡后,使容器内物质全部发生完全燃烧,将产物通过足量的 固体,则固体增重
固体,则固体增重(3)
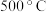 时,从反应开始到达到化学平衡,以
时,从反应开始到达到化学平衡,以 的浓度变化表示的化学反应速率是
的浓度变化表示的化学反应速率是 ,
, 表示)
表示)(4)
 时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是
时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是a.
 的物质的量增加
的物质的量增加b.正反应速率加快,逆反应速率减慢
c.
 和
和 均减小
均减小d.重新平衡时
 减小
减小(5)向含有
 和
和 的稀溶液中加入足量的铁屑,最终产生气体的物质的量为
的稀溶液中加入足量的铁屑,最终产生气体的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 碳在地壳中的含量很低,但是含有碳元素的有机物却分布极广。
(1)观察下面几种烷烃的球棍模型:______________ (填字母,下同),与C互为同分异构体的是______________ .
(2)写出下列链状烷烃的分子式:
①含有30个氢原子的烷烃的分子式为______________ .
②假如某烷烃的相对分子质量为142,则该烷烃的分子式为______________ .
(3)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室模拟上述过程,其设计的模拟装置如图.
①装置B有三种功能:a.控制气流速度;b.均匀混合气体;c.______________ .
②设 ,若理论上欲获得最多的氯化氢,则x值应
,若理论上欲获得最多的氯化氢,则x值应______________ .
③装置D的石棉中均匀混有 粉末,其作用是
粉末,其作用是__________________________________________ .
④装置E的作用是______________ (填序号).
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(1)观察下面几种烷烃的球棍模型:
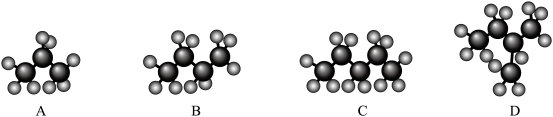
(2)写出下列链状烷烃的分子式:
①含有30个氢原子的烷烃的分子式为
②假如某烷烃的相对分子质量为142,则该烷烃的分子式为
(3)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室模拟上述过程,其设计的模拟装置如图.
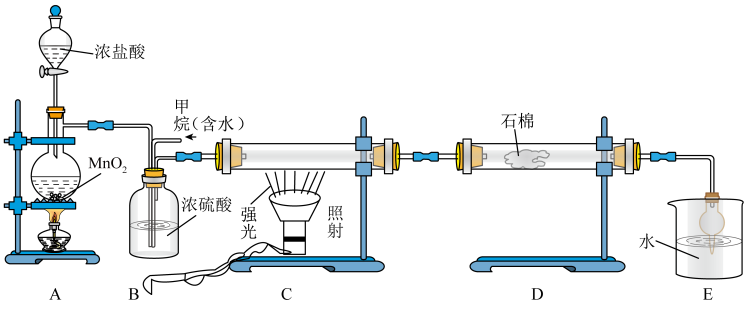
①装置B有三种功能:a.控制气流速度;b.均匀混合气体;c.
②设
 ,若理论上欲获得最多的氯化氢,则x值应
,若理论上欲获得最多的氯化氢,则x值应③装置D的石棉中均匀混有
 粉末,其作用是
粉末,其作用是④装置E的作用是
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
您最近一年使用:0次
名校
3 . 某恒温条件下,将6mol的 和4mol的
和4mol的 充入1L恒容密闭容器中,发生如下反应:
充入1L恒容密闭容器中,发生如下反应: 。下图是
。下图是 的浓度随时间变化的关系图。回答下列问题:
的浓度随时间变化的关系图。回答下列问题: 的平均反应速率是
的平均反应速率是___________  。
。
(2)
___________ 2.5min(填“>”“<”或“=”),原因是___________ 。
(3)反应进行到10min时,
___________  (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是___________ 。
(4)反应达平衡时, 的转化率为
的转化率为___________ 。若反应开始前容器内压强为 ,平衡时容器内压强为
,平衡时容器内压强为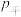 ,则
,则
___________ 。
 和4mol的
和4mol的 充入1L恒容密闭容器中,发生如下反应:
充入1L恒容密闭容器中,发生如下反应: 。下图是
。下图是 的浓度随时间变化的关系图。回答下列问题:
的浓度随时间变化的关系图。回答下列问题: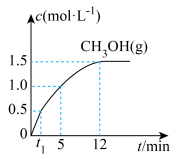
 的平均反应速率是
的平均反应速率是 。
。(2)

(3)反应进行到10min时,

 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是(4)反应达平衡时,
 的转化率为
的转化率为 ,平衡时容器内压强为
,平衡时容器内压强为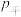 ,则
,则
您最近一年使用:0次
名校
4 . I.回答下列问题:
(1)请用以下物质的序号填空:
①NaCl② ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨He⑩
⑨He⑩
其中只含有共价键的化合物有___________ ,含有非极性共价键的离子化合物有___________ ,含有极性共价键的离子化合物有___________ ,不含共价键的化合物有___________ 。
(2)X、Y两种主族元素能形成 型化合物,已知
型化合物,已知 中共有38个电子,若
中共有38个电子,若 为常见元素形成的离子化合物,其电子式为
为常见元素形成的离子化合物,其电子式为___________ ;若 为共价化合物,其结构式为
为共价化合物,其结构式为___________ 。
II.已知:在常温常压下,断开1molAB(g)分子中的化学键使其分别生成气态原子A(g)和B(g)所吸收的能量叫做键能。几种共价键的键能如下表所示:
(3)2molHBr(g)和 反应生成2molHF(g)和
反应生成2molHF(g)和
___________ (填“吸收”或“放出”)___________ KJ能量。
(1)请用以下物质的序号填空:
①NaCl②
 ③NaOH④
③NaOH④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨He⑩
⑨He⑩
其中只含有共价键的化合物有
(2)X、Y两种主族元素能形成
 型化合物,已知
型化合物,已知 中共有38个电子,若
中共有38个电子,若 为常见元素形成的离子化合物,其电子式为
为常见元素形成的离子化合物,其电子式为 为共价化合物,其结构式为
为共价化合物,其结构式为II.已知:在常温常压下,断开1molAB(g)分子中的化学键使其分别生成气态原子A(g)和B(g)所吸收的能量叫做键能。几种共价键的键能如下表所示:
| 共价键 |  |  |  |  |  |  |  |
键能 | 266 | 159 | 327 | 565 | 363 | 193 | 347 |
 反应生成2molHF(g)和
反应生成2molHF(g)和
您最近一年使用:0次
名校
解题方法
5 . 硫及其化合物是十分重要的化工原料。
Ⅰ.工业上一般以硫磺或其他含硫矿物为原料制备硫酸。金属冶炼时产生的含二氧化硫废气经回收后也可用于制备硫酸。___________ 。
(2)用98.3%的浓硫酸吸收 而不用水的原因为
而不用水的原因为___________ 。
Ⅱ.某同学设计如图实验测定硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气)___________ (答操作)。
(4)已知开始时量气管读数为 mL,最终读数为
mL,最终读数为 mL(均折合成标准状况,且
mL(均折合成标准状况,且 )。则锌与稀硫酸发生反应的最低硫酸浓度为
)。则锌与稀硫酸发生反应的最低硫酸浓度为___________ mol/L。
Ⅲ.实验小组为探究 与
与 溶液的反应,进行了以下实验。
溶液的反应,进行了以下实验。
实验一:用如下装置(夹持、加热仪器略)制备 ,将足量
,将足量 通入
通入 溶液中,迅速反应,得到无色溶液A和白色沉淀B,经分析得出,沉淀B可能为
溶液中,迅速反应,得到无色溶液A和白色沉淀B,经分析得出,沉淀B可能为 、(微溶)或二者的混合物。
、(微溶)或二者的混合物。 溶液,未出现白色沉淀。
溶液,未出现白色沉淀。
(5)实验二可判断B中不含 。做出判断的理由为
。做出判断的理由为___________ 。
(6)由实验二可知,实验一中, 与
与 溶液反应的离子方程式是
溶液反应的离子方程式是___________ 。
根据物质性质分析, 与
与 溶液应该可以发生氧化还原反应。
溶液应该可以发生氧化还原反应。
实验三:将实验一所得混合物隔绝空气放置一段时间,有Ag和 生成。
生成。
(7)根据实验一、二、三,可得结论为___________ 。
Ⅰ.工业上一般以硫磺或其他含硫矿物为原料制备硫酸。金属冶炼时产生的含二氧化硫废气经回收后也可用于制备硫酸。

(2)用98.3%的浓硫酸吸收
 而不用水的原因为
而不用水的原因为Ⅱ.某同学设计如图实验测定硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气)

(4)已知开始时量气管读数为
 mL,最终读数为
mL,最终读数为 mL(均折合成标准状况,且
mL(均折合成标准状况,且 )。则锌与稀硫酸发生反应的最低硫酸浓度为
)。则锌与稀硫酸发生反应的最低硫酸浓度为Ⅲ.实验小组为探究
 与
与 溶液的反应,进行了以下实验。
溶液的反应,进行了以下实验。实验一:用如下装置(夹持、加热仪器略)制备
 ,将足量
,将足量 通入
通入 溶液中,迅速反应,得到无色溶液A和白色沉淀B,经分析得出,沉淀B可能为
溶液中,迅速反应,得到无色溶液A和白色沉淀B,经分析得出,沉淀B可能为 、(微溶)或二者的混合物。
、(微溶)或二者的混合物。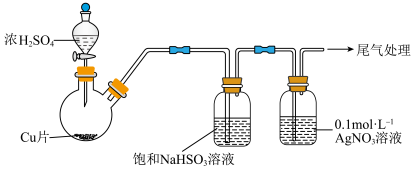
 溶液,未出现白色沉淀。
溶液,未出现白色沉淀。(5)实验二可判断B中不含
 。做出判断的理由为
。做出判断的理由为(6)由实验二可知,实验一中,
 与
与 溶液反应的离子方程式是
溶液反应的离子方程式是根据物质性质分析,
 与
与 溶液应该可以发生氧化还原反应。
溶液应该可以发生氧化还原反应。实验三:将实验一所得混合物隔绝空气放置一段时间,有Ag和
 生成。
生成。(7)根据实验一、二、三,可得结论为
您最近一年使用:0次
名校
解题方法
6 . 用一种具有“卯榫”结构的双极膜组装电解池(如图),可实现大电流催化电解 溶液制氨。
溶液制氨。_____ ,阳极反应式:_____ 。
(2)工作时,在双极膜界面处 发生解离产生
发生解离产生 和
和 ,产生的
,产生的 移向
移向_____ 极(填“a”或“b”),每生成 ,双极膜处有
,双极膜处有_____ mol的 解离。
解离。
(3)电解过程中,阳极室中KOH的物质的量_____ (填“增加”“不变”或“减少”)
(4)相比于平面结构双极膜,“卯榫”结构可增加接触面积,有利于_____ 。
 溶液制氨。
溶液制氨。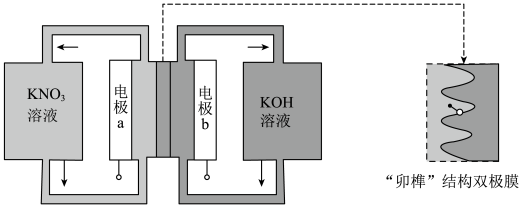
(2)工作时,在双极膜界面处
 发生解离产生
发生解离产生 和
和 ,产生的
,产生的 移向
移向 ,双极膜处有
,双极膜处有 解离。
解离。(3)电解过程中,阳极室中KOH的物质的量
(4)相比于平面结构双极膜,“卯榫”结构可增加接触面积,有利于
您最近一年使用:0次
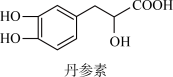
7 . 丹参素能明显抑制血小板的聚集,其结构如图所示。___________ 。
(2)丹参素___________ (填“是”或“否”)属于芳香烃。
(3)下列反应类型中丹参素不能发生的___________ (填序号)。
①加成反应 ②取代反应 ③氧化反应 ④加聚反应
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有___________ 性。
(5)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗___________ molNaOH;1mol丹参素与足量Na反应,可以产生___________ mol 。
。
已知:①在表示有机化合物的组成和结构时,如果将碳、氢元素符号省略,只表示分子中键的连接情况和官能团,每个拐点或终点均表示有一个碳原子,则得到键线式。如丙烯可表示为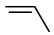 ,乙醇可表示为
,乙醇可表示为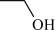 。
。
③苯酚(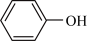 )是最简单的酚,酚羟基在水中可微弱电离,产生
)是最简单的酚,酚羟基在水中可微弱电离,产生 而显弱酸性
而显弱酸性
(2)丹参素
(3)下列反应类型中丹参素不能发生的
①加成反应 ②取代反应 ③氧化反应 ④加聚反应
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有
(5)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗
 。
。
您最近一年使用:0次
解题方法
8 . 认识有机物组成和结构对有机物的学习非常重要。
Ⅰ.根据下列有机物的空间填充模型,填空。_______ 种;
(2)乙中σ键与π键的个数比为_______ ;
(3)丙中碳原子的杂化方式_______ ;
(4)丁的结构简式为_______ ;
(5)分子中所有原子一定在同一平面内的是_______ (填序号)。
Ⅱ.中药小柴胡可以用来治疗感冒发烧,其主要成分之一是山奈酚,结构如图所示。_______ mol  。
。
Ⅲ.以下是几种烃分子的球棍模型:_______ 。
(8)写出D的键线式_______ 。
Ⅰ.根据下列有机物的空间填充模型,填空。
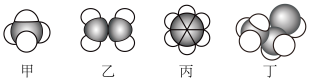
(2)乙中σ键与π键的个数比为
(3)丙中碳原子的杂化方式
(4)丁的结构简式为
(5)分子中所有原子一定在同一平面内的是
Ⅱ.中药小柴胡可以用来治疗感冒发烧,其主要成分之一是山奈酚,结构如图所示。
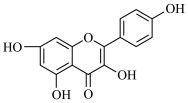
 。
。Ⅲ.以下是几种烃分子的球棍模型:
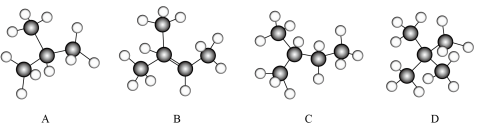
(8)写出D的键线式
您最近一年使用:0次
名校
9 . 电池的应用对人类社会的发展作出了巨大贡献。试运用化学反应与电能知识回答下列问题。
(1)用下图甲、乙所示装置进行实验。请回答下列问题:___________ ;乙中:化学能→___________ 。
②乙装置中锌棒上发生的反应为___________ ;若反应前Zn棒和Cu棒的质量相同,当导线中转移0.1mol电子时,两金属电极的质量之差为___________ g。
(2)某实验小组设计了如图所示原电池装置。___________ (填“铝棒”或“镁棒”),Al棒上发生的电极反应式为___________ 。
②若电解质溶液X为稀硫酸,Mg棒上发生的电极反应式是___________ ,外导线中电子的流动方向是___________ (填“Al→Mg”或“Mg→Al”)。
(1)用下图甲、乙所示装置进行实验。请回答下列问题:
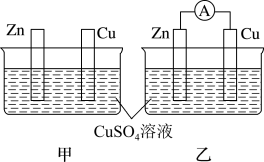
②乙装置中锌棒上发生的反应为
(2)某实验小组设计了如图所示原电池装置。

②若电解质溶液X为稀硫酸,Mg棒上发生的电极反应式是
您最近一年使用:0次
名校
解题方法
10 . 下面是以硫黄为原料制备硫酸的工业流程。已知SO₃的熔点是:16.8℃,沸点是44.8℃。___________ 。
(2)每轮反应后都要进行热交换降温的目的是___________ 。
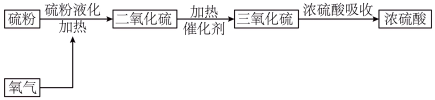
(2)每轮反应后都要进行热交换降温的目的是
您最近一年使用:0次



