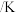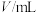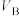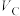名校
解题方法
1 . 酸性 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为 。某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
。某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
(1)实验中a的最小值为___________ ,探究温度变化对反应速率影响情况的两组实验是___________ 。
(2)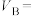
___________ ,
___________ ,利用实验B中数据计算,用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
___________ 。
(3)他们发现,A组实验中收集的 体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。
体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。 时间内速率变快的主要原因可能:一是
时间内速率变快的主要原因可能:一是______________ ;二是______________ 。
 溶液与
溶液与 溶液反应的离子方程式为
溶液反应的离子方程式为 。某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。
。某同学设计如下表所示方案探究温度、浓度改变对该反应速率的影响情况。实验序号 | 实验温度 | 参加反应的物质 | 溶液颜色褪至无色所需时间/s | ||||
|
|
| |||||
| c/mol/L |
| c/mol/L |
| |||
A | 298 | 2 | 0.03 | 4 | a | 0 |
|
B | TB | 2 | 0.03 | 3 | a |
| 10 |
C | 318 | 2 | 0.03 |
| a | 1 |
|
(2)
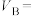

 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为
(3)他们发现,A组实验中收集的
 体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。
体积如图a所示;若使A组反应在绝热容器中进行,该反应的反应速率随着时间的变化如图b所示。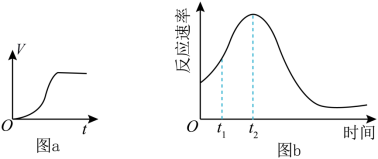
 时间内速率变快的主要原因可能:一是
时间内速率变快的主要原因可能:一是
您最近一年使用:0次
名校
2 . 聚氯乙烯英文缩写为PVC,是当今世界上产量最大、应用最广的热塑性塑料之一。
(1)工业上以乙烯和氯气为原料合成PVC的流程如下:
乙烯


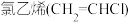

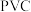
乙烯生成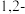 二氯乙烷的化学方程式为
二氯乙烷的化学方程式为_________________ ,反应类型是____________ 。
(2)一定条件下,乙炔( )经两步反应也可以得到聚氯乙烯,写出反应的化学方程式:
)经两步反应也可以得到聚氯乙烯,写出反应的化学方程式:___________ 、 __________ 。
(3)下列有关PVC的说法正确的是____________ (填字母)。
a.能使溴的四氯化碳溶液褪色 b.在空气中燃烧,但产物易引起环境污染
c.能使酸性 溶液褪色
溶液褪色
(4)下列物质不可能 是丙烯加成产物的是 _____________ 。
a.CH3CH2CH3 b.CH3CHClCH3 c.CH3CH2CH2Cl d.CH2ClCH=CH2
(1)工业上以乙烯和氯气为原料合成PVC的流程如下:
乙烯



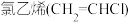

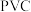
乙烯生成
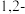 二氯乙烷的化学方程式为
二氯乙烷的化学方程式为(2)一定条件下,乙炔(
 )经两步反应也可以得到聚氯乙烯,写出反应的化学方程式:
)经两步反应也可以得到聚氯乙烯,写出反应的化学方程式:(3)下列有关PVC的说法正确的是
a.能使溴的四氯化碳溶液褪色 b.在空气中燃烧,但产物易引起环境污染
c.能使酸性
 溶液褪色
溶液褪色(4)下列物质
a.CH3CH2CH3 b.CH3CHClCH3 c.CH3CH2CH2Cl d.CH2ClCH=CH2
您最近一年使用:0次
名校
3 . 回答下列问题。
(1)将物质进行分类:①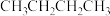 和
和 ②乙醇
②乙醇 与二甲醚
与二甲醚 ③D2O与H2O④
③D2O与H2O④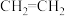 和
和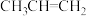 ⑤
⑤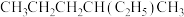 和
和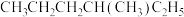 ,用序号回答下列问题:
,用序号回答下列问题:
A互为同分异构体的是__________ ;B属于同一种化合物的是__________ ;C互为同系物的是_________ 。
(2)分子中含有22个共价键的链状烷烃有多种同分异构体,写出其中含有三个甲基且等效氢有3种的结构简式:_____________________________________
(3)有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似。写出乙硅烷在空气中自燃的化学方程式:___________ 。
(4)若 、C2H4、C2H2、C6H6四种烃各为1g,在足量
、C2H4、C2H2、C6H6四种烃各为1g,在足量 中燃烧,消耗
中燃烧,消耗 最多的是:
最多的是:___________ 。
(5)写出CH3—CH=CH—CH3发生加聚反应的化学方程式:_______________ 。
(1)将物质进行分类:①
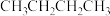 和
和 ②乙醇
②乙醇 与二甲醚
与二甲醚 ③D2O与H2O④
③D2O与H2O④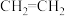 和
和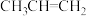 ⑤
⑤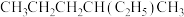 和
和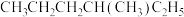 ,用序号回答下列问题:
,用序号回答下列问题:A互为同分异构体的是
(2)分子中含有22个共价键的链状烷烃有多种同分异构体,写出其中含有三个甲基且等效氢有3种的结构简式:
(3)有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似。写出乙硅烷在空气中自燃的化学方程式:
(4)若
 、C2H4、C2H2、C6H6四种烃各为1g,在足量
、C2H4、C2H2、C6H6四种烃各为1g,在足量 中燃烧,消耗
中燃烧,消耗 最多的是:
最多的是:(5)写出CH3—CH=CH—CH3发生加聚反应的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题。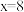 ,则此阴离子与图中带一个正电荷的阳离子形成一种常见化合物的化学式是
,则此阴离子与图中带一个正电荷的阳离子形成一种常见化合物的化学式是_______ 。
(2) 微粒A含有
微粒A含有 电子,下列微粒各
电子,下列微粒各 ,也含有
,也含有 电子的有:
电子的有:_______ (填序号)
① ②
② ③HF ④
③HF ④ ⑤
⑤ ⑥
⑥
(3)若A的阳离子为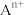 且质量数为a,则其质子数为
且质量数为a,则其质子数为_______ 。中子数为_______ (用含有a,n的代数式表达)
II.有以下8种物质:
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
试回答下列问题:
(4)不存在化学键的是_______ (填序号,下同)。
(5)既存在非极性共价键又存在极性共价键的是_______ 。
(6)只存在离子键的是_______ 。
(7)既存在离子键又存在共价键的是_______ 。
I.某微粒A的结构示意图为
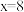 ,则此阴离子与图中带一个正电荷的阳离子形成一种常见化合物的化学式是
,则此阴离子与图中带一个正电荷的阳离子形成一种常见化合物的化学式是(2)
 微粒A含有
微粒A含有 电子,下列微粒各
电子,下列微粒各 ,也含有
,也含有 电子的有:
电子的有:①
 ②
② ③HF ④
③HF ④ ⑤
⑤ ⑥
⑥
(3)若A的阳离子为
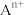 且质量数为a,则其质子数为
且质量数为a,则其质子数为II.有以下8种物质:
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧
试回答下列问题:
(4)不存在化学键的是
(5)既存在非极性共价键又存在极性共价键的是
(6)只存在离子键的是
(7)既存在离子键又存在共价键的是
您最近一年使用:0次
名校
5 . 元素周期表中钛的数据如图所示,47.87的含义是___________ ;Ti在元素周期表中的位置是___________ 。

您最近一年使用:0次
名校
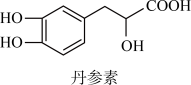
6 . 丹参素能明显抑制血小板的聚集,其结构如图所示。_______ 。
(2)丹参素在一定条件下能与 反应生成酯,该反应的类型属于
反应生成酯,该反应的类型属于_______ 反应。
(3)丹参素中含氧官能团有_______ (填名称)。
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有_______ 性。
(5)向稀的酸性 溶液中滴入几滴丹参素溶液,观察到的现象为
溶液中滴入几滴丹参素溶液,观察到的现象为_______ ,说明丹参素具有_______ 性(填“氧化”或“还原”)
(6)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗_______ mol ;
; 在一定条件下被氧化的生成物,其分子式为
在一定条件下被氧化的生成物,其分子式为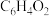 该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式
该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式_______ 。
①在表示有机化合物的组成和结构时,如果将碳、氢元素符号省略,只表示分子中的键的连接情况和官能团,每个拐点或终点均表示有一个碳原子,则得到键线式。如丙烯可表示为 ,乙醇可表示为
,乙醇可表示为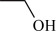 。
。
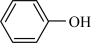
③苯酚(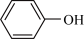 )是最简单的酚,酚羟基在水中可微弱电离,产生
)是最简单的酚,酚羟基在水中可微弱电离,产生 。
。
(2)丹参素在一定条件下能与
 反应生成酯,该反应的类型属于
反应生成酯,该反应的类型属于(3)丹参素中含氧官能团有
(4)向丹参素溶液中滴入2~3滴紫色石蕊试液,溶液颜色变红,说明丹参素溶液具有
(5)向稀的酸性
 溶液中滴入几滴丹参素溶液,观察到的现象为
溶液中滴入几滴丹参素溶液,观察到的现象为(6)根据丹参素结构,预测1mol丹参素和足量的氢氧化钠溶液反应时,最多能够消耗
 ;
; 在一定条件下被氧化的生成物,其分子式为
在一定条件下被氧化的生成物,其分子式为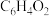 该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式
该分子有一个六元碳环,且4个氢原子的化学环境相同,该物质的键线式
您最近一年使用:0次
名校
7 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
I.气态分子中1mol化学键解离成气态原子所吸收的能量称为键能( ),一些共价键的键能如下表所示。
),一些共价键的键能如下表所示。
(1)请根据上表数据计算,在工业合成氨的反应中,当生成17.0g氨气时___________ (填“放出”或“吸收”)的热量为___________ kJ。
Ⅱ.实验室模拟工业合成氨时,在容积为5L的密闭容器内,开始时加入2.0molN2(g)和5.0molH2(g),在20min末,测得NH3(g)的物质的量是1.0mol。
(2)20min末时,N2的体积分数为___________ 。
(3)反应开始至20min,H2的平均反应速率为___________ 。
(4)20min末时,容器内的压强与起始压强之比为___________ 。
(5)一定条件下,将一定量CH4(g)与H2O(g)充入密闭容器中发生反应 ,下列措施可以提高化学反应速率的是
,下列措施可以提高化学反应速率的是___________ 。
a.恒容条件下充入He b.增大容器体积 c.升高温度
d.保持恒容投入更多的H2O(g) e.加入合适的催化剂
(6)下列化学反应过程中的能量变化能用下图表示的有___________ 。
b.乙烷在氧气中燃烧生成水和二氧化碳
c.钠和水反应
d.二氧化碳通过炽热的碳
e.
f.高温煅烧石灰石使其分解
I.气态分子中1mol化学键解离成气态原子所吸收的能量称为键能(
 ),一些共价键的键能如下表所示。
),一些共价键的键能如下表所示。| 共价键 | H-H |  | N-H |
键能( ) ) | 436 | 946 | 391 |
(1)请根据上表数据计算,在工业合成氨的反应中,当生成17.0g氨气时
Ⅱ.实验室模拟工业合成氨时,在容积为5L的密闭容器内,开始时加入2.0molN2(g)和5.0molH2(g),在20min末,测得NH3(g)的物质的量是1.0mol。
(2)20min末时,N2的体积分数为
(3)反应开始至20min,H2的平均反应速率为
(4)20min末时,容器内的压强与起始压强之比为
(5)一定条件下,将一定量CH4(g)与H2O(g)充入密闭容器中发生反应
 ,下列措施可以提高化学反应速率的是
,下列措施可以提高化学反应速率的是a.恒容条件下充入He b.增大容器体积 c.升高温度
d.保持恒容投入更多的H2O(g) e.加入合适的催化剂
(6)下列化学反应过程中的能量变化能用下图表示的有

b.乙烷在氧气中燃烧生成水和二氧化碳
c.钠和水反应
d.二氧化碳通过炽热的碳
e.

f.高温煅烧石灰石使其分解
您最近一年使用:0次
8 . A~H代表的几种有机物如下图所示,请按照要求填空。(黑球为碳原子、白球为氢原子)___________ (填字母,下同),与B互为同系物的物质是___________ ,和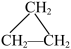 互为同分异构体的是
互为同分异构体的是___________ ,A~H表示的物质中,为同一物质的是___________ 。
(2)与D互为同分异构体的物质的结构简式是_______ ,D的一氯代物有________ 种。
(3)等质量的A~D物质完全燃烧时耗去O2的量最多的是___________ (填对应分子式)。
(4)A~H表示的物质中,能发生加成反应的是___________ (填字母)。
(5)G中共面的原子最多有___________ 个。
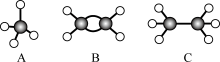


 互为同分异构体的是
互为同分异构体的是(2)与D互为同分异构体的物质的结构简式是
(3)等质量的A~D物质完全燃烧时耗去O2的量最多的是
(4)A~H表示的物质中,能发生加成反应的是
(5)G中共面的原子最多有
您最近一年使用:0次
9 . A-E可表示常见有机物,请从A-E中选择适当的物质,回答下列问题:___________ (写结构简式)。
(2)能使酸性高锰酸钾溶液褪色的物质有___________ 、___________ (写结构简式)。
(3)E的官能团名称为___________ 。
(4)写出D和E反应的化学方程式:___________ 。
(5)等质量的A、B、C完全燃烧,耗氧最多的是___________ (填分子式)。
(6) 的名称是
的名称是___________ 。

(2)能使酸性高锰酸钾溶液褪色的物质有
(3)E的官能团名称为
(4)写出D和E反应的化学方程式:
(5)等质量的A、B、C完全燃烧,耗氧最多的是
(6)
 的名称是
的名称是
您最近一年使用:0次
名校
解题方法
10 . 完成下列问题。
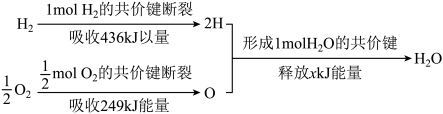
(1)下图表示氢气燃烧生成水蒸气的物质及能量变化。
已知1 mol氢气完全燃烧生成水蒸气时放出热量245 kJ。___________ 。
(2)恒温下,将1 mol N2和3 mol H2置于体积为2 L的密闭容器中进行反应。若5 min时测得氢气浓度为0.9 mol/L,则用氨气表示5 min内的化学反应速率为___________ 。
(3)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,在恒容密闭容中充入4 mol CO和4 mol NO发生 反应。
反应。
①为提高此反应的速率,下列措施可行的是___________ (填字母)。
A.充入氦气 B.降低温度 C.使用适合催化剂 D.移出CO2
②下列事实能说明该反应达到平衡状态的是___________ (填字母)
A.容器中NO和CO的体积分数之比不再变化
B.容器中混合气体的平均相对分子质量不再变化
C.2v正(NO)=v逆(N2)
D.相同时间内断裂N2中 数与形成CO2中C=O数之比为1∶2
数与形成CO2中C=O数之比为1∶2
(4)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn + O2=2ZnO。则该电池的负极材料是___________ 。
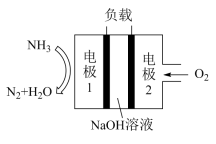
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,负极的电极反应式为___________ 。若电路中消耗0.1molNH3,则标准状况下消耗氧气的体积为:___________ 。
(1)下图表示氢气燃烧生成水蒸气的物质及能量变化。
已知1 mol氢气完全燃烧生成水蒸气时放出热量245 kJ。
(2)恒温下,将1 mol N2和3 mol H2置于体积为2 L的密闭容器中进行反应。若5 min时测得氢气浓度为0.9 mol/L,则用氨气表示5 min内的化学反应速率为
(3)消除NO污染物,可在一定条件下,用CO与NO反应生成CO2和N2,在恒容密闭容中充入4 mol CO和4 mol NO发生
 反应。
反应。①为提高此反应的速率,下列措施可行的是
A.充入氦气 B.降低温度 C.使用适合催化剂 D.移出CO2
②下列事实能说明该反应达到平衡状态的是
A.容器中NO和CO的体积分数之比不再变化
B.容器中混合气体的平均相对分子质量不再变化
C.2v正(NO)=v逆(N2)
D.相同时间内断裂N2中
 数与形成CO2中C=O数之比为1∶2
数与形成CO2中C=O数之比为1∶2(4)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是2Zn + O2=2ZnO。则该电池的负极材料是
②瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池的示意图如图,该燃料电池工作时,负极的电极反应式为
您最近一年使用:0次