1 . 化学电源在生产生活中有着广泛的应用,同学们常常通过设计实验和查阅资料的方式学习化学电源的相关知识。
(1)图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
(2)将上述乙装置中电解质稀 溶液换为足量
溶液换为足量 溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是_______ (填“ “或“
“或“ ”),正极的电极反应是
”),正极的电极反应是_______ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差 ,则导线上通过的
,则导线上通过的
_____ mol。
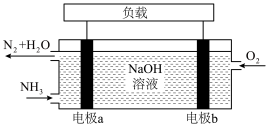
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:_______ (填“正极”或“负极”)
②电解质溶液中 离子向
离子向_______ 电极移动(填“a”或“b”)
③电极 的电极反应式为
的电极反应式为_______ 。
(1)图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

| A.甲中锌片是负极,乙中铜片是正极 |
| B.甲烧杯锌片表面有气泡产生,乙烧杯铜片表面有气泡产生 |
| C.乙中电子从铜片经导线流向锌片 |
D.乙溶液中 向锌片方向移动 向锌片方向移动 |
(2)将上述乙装置中电解质稀
 溶液换为足量
溶液换为足量 溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。①原电池的负极是
 “或“
“或“ ”),正极的电极反应是
”),正极的电极反应是②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差
 ,则导线上通过的
,则导线上通过的
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:
②电解质溶液中
 离子向
离子向③电极
 的电极反应式为
的电极反应式为
您最近一年使用:0次
名校
2 . 按要求完成下列填空。
(1)化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,图为 和
和 反应生成
反应生成 过程中的能量变化:
过程中的能量变化:_______ 反应(填“吸热”或“放热”)。
②该反应中,每生成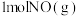 ,放出(或吸收)热量
,放出(或吸收)热量_______  。
。
③某实验小组进行如图甲所示实验,反应过程_______ (填“a”或“b”)的能量变化可用图乙表示。
①写出上述反应的化学反应方程式_______ 。
②若实验探究温度对该反应速率的影响,则a=_____ 采用比较实验的序号是_____ (填实验序号)。
(1)化学反应中的能量变化是由化学反应中旧化学键断裂时吸收的能量与新化学键形成时放出的能量不同引起的,图为
 和
和 反应生成
反应生成 过程中的能量变化:
过程中的能量变化: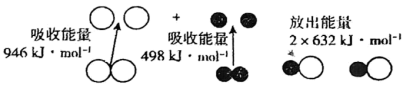
②该反应中,每生成
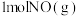 ,放出(或吸收)热量
,放出(或吸收)热量 。
。③某实验小组进行如图甲所示实验,反应过程

| 实验序号 | 反应温度(℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL |  | V/mL |  | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | a |
| C | 25 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
②若实验探究温度对该反应速率的影响,则a=
您最近一年使用:0次
3 . 硅单质及其化合物应用广泛。请回答下列问题:
(1)传统的无机非金属材料多为硅酸盐材料,主要包括___________ 、水泥和玻璃。
(2) 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是___________ (用化学方程式表示)。
(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是___________(填字母)。
(4)新型陶瓷材料氮化硅( )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下: 。若生成标准状况下33.6LCO时,反应过程中转移的电子数为
。若生成标准状况下33.6LCO时,反应过程中转移的电子数为___________  。
。
(1)传统的无机非金属材料多为硅酸盐材料,主要包括
(2)
 是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是
是玻璃的主要成分之一,保存氢氧化钠溶液的玻璃瓶应用橡胶塞的原因是(3)沙子可用作建筑材料和制玻璃的原料,下列说法不正确的是___________(填字母)。
A. 能与水反应 能与水反应 | B. 在一定条件下能与氧化钙反应 在一定条件下能与氧化钙反应 |
C. 是制作光导纤维的主要原料 是制作光导纤维的主要原料 | D. 能与稀硫酸反应 能与稀硫酸反应 |
 )可应用于原子反应堆,一种制备氮化硅的反应如下:
)可应用于原子反应堆,一种制备氮化硅的反应如下: 。若生成标准状况下33.6LCO时,反应过程中转移的电子数为
。若生成标准状况下33.6LCO时,反应过程中转移的电子数为 。
。
您最近一年使用:0次
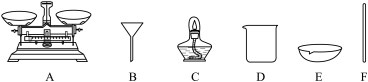
4 . Ⅰ.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。___________ ,C的化学式是___________ 。
(4)加入过量A的目的是___________ 。
(5)加入过量B的目的是___________ 。
(6)加热煮沸的目的是___________ 。
(7)操作Ⅰ的名称是___________ 。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是

(4)加入过量A的目的是
(5)加入过量B的目的是
(6)加热煮沸的目的是
(7)操作Ⅰ的名称是
您最近一年使用:0次
解题方法
5 . 如图所示将锌、铜通过导线相连,置于硫酸溶液中。___________ 能转化为___________ 能。
(2) 电极为
电极为___________ 极,发生___________ (填“氧化”或“还原”)反应,电极方程式为___________ 。
(3)外电路电流由___________ (填“锌”或“铜”,下同)电极经导线流向___________ 电极。
(4)标准状况下,若反应过程中溶解了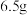 锌,则生成的氢气的体积为
锌,则生成的氢气的体积为___________  。
。

(2)
 电极为
电极为(3)外电路电流由
(4)标准状况下,若反应过程中溶解了
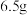 锌,则生成的氢气的体积为
锌,则生成的氢气的体积为 。
。
您最近一年使用:0次
6 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。请回答下列问题:
(1)下列物质不属于硅酸盐的是___________(填字母)。
(2)可用于制作计算机芯片和太阳能电池的是___________ (填化学式), 是玻璃的主要成分之一,
是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程式为
与氢氧化钠溶液反应的化学方程式为___________ 。
(3)工艺师常用___________ (填物质名称)来雕刻玻璃,该反应的化学方程式为___________ 。
(4)用 溶液浸泡过的棉花不易燃烧,说明
溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。
(5)工业上常用 制备硅单质,该反应中有元素化合价升高的物质是
制备硅单质,该反应中有元素化合价升高的物质是___________ (填化学式,下同),氧化剂是___________ 。
(1)下列物质不属于硅酸盐的是___________(填字母)。
| A.陶瓷 | B.玻璃 | C.水泥 | D.生石灰 |
(2)可用于制作计算机芯片和太阳能电池的是
 是玻璃的主要成分之一,
是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程式为
与氢氧化钠溶液反应的化学方程式为(3)工艺师常用
(4)用
 溶液浸泡过的棉花不易燃烧,说明
溶液浸泡过的棉花不易燃烧,说明 可用作
可用作(5)工业上常用
 制备硅单质,该反应中有元素化合价升高的物质是
制备硅单质,该反应中有元素化合价升高的物质是
您最近一年使用:0次
7 . 下列各过程主要表现了浓硫酸的哪些性质?请将答案的序号分别填在横线上。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体___________ 。
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸___________ 。
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体___________ 。
(4)常温下可以用铁或铝的容器贮存浓硫酸___________ 。
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末___________ 。
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体___________ 。
①强酸性 ②强氧化性 ③高沸点、难挥发性 ④脱水性 ⑤吸水性
(1)用氯化钠固体和浓硫酸在加热条件下制氯化氢气体
(2)用磷矿物[主要成分是磷酸钙]和硫酸反应制磷酸
(3)浓硫酸干燥氢气、氧气、氯气、二氧化硫等气体
(4)常温下可以用铁或铝的容器贮存浓硫酸
(5)胆矾放在盛浓硫酸的干燥器中变成白色粉末
(6)不能用浓硫酸干燥溴化氢、碘化氢和硫化氢等气体
您最近一年使用:0次
解题方法
8 . 回答下列问题。
(1)利用VSEPR模型推断分子或离子的立体构型。
CS2___________ ;AlBr3(共价分子)___________ 。
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
平面形分子___________ ,三角锥形分子___________ ,四面体形分子___________ 。
(1)利用VSEPR模型推断分子或离子的立体构型。
CS2
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:

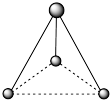
平面形分子
您最近一年使用:0次
解题方法
9 . 根据已学知识,请你回答下列问题:
(1)含有8个质子,10个中子的原子的化学符号___________ 。
(2)最外层电子排布为4s24p1的原子的核电荷数为___________ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是___________ 。
(4)根据VSEPR模型,H3O+的分子立体结构为:___________ 。
(5)周期表中最活泼的非金属元素原子的轨道表示式为___________ 。
(1)含有8个质子,10个中子的原子的化学符号
(2)最外层电子排布为4s24p1的原子的核电荷数为
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是
(4)根据VSEPR模型,H3O+的分子立体结构为:
(5)周期表中最活泼的非金属元素原子的轨道表示式为
您最近一年使用:0次
解题方法
10 . 按要求填空。
(1)基态铝原子核外电子共有___________ 种不同能级的电子,最高能级的电子云有___________ 种不同的伸展方向,有___________ 种不同运动状态的电子。
(2)S的基态原子核外有___________ 个未成对电子,Si的基态原子核外电子排布式为___________ 。基态Si原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子数为___________ 。
(3)可正确表示原子轨道的是___________(填字母)。
(4)基态Fe原子有___________ 个未成对电子,Fe3+的电子排布式为___________ ;Cu+基态核外电子排布式为___________ 。
(5)某元素的原子最外层电子排布式为nsnnpn+2,则n=___________ ;原子中能量最高的是___________ 能级电子。
(6)第四周期中最外层仅有1个电子的所有基态原子的电子排布式为___________ ,第四周期中,3d轨道半充满的元素符号是___________ 。
(1)基态铝原子核外电子共有
(2)S的基态原子核外有
(3)可正确表示原子轨道的是___________(填字母)。
| A.2s | B.2d | C.3p | D.3f |
(5)某元素的原子最外层电子排布式为nsnnpn+2,则n=
(6)第四周期中最外层仅有1个电子的所有基态原子的电子排布式为
您最近一年使用:0次



