根据已学知识,请你回答下列问题:
(1)含有8个质子,10个中子的原子的化学符号___________ 。
(2)最外层电子排布为4s24p1的原子的核电荷数为___________ 。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是___________ 。
(4)根据VSEPR模型,H3O+的分子立体结构为:___________ 。
(5)周期表中最活泼的非金属元素原子的轨道表示式为___________ 。
(1)含有8个质子,10个中子的原子的化学符号
(2)最外层电子排布为4s24p1的原子的核电荷数为
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是
(4)根据VSEPR模型,H3O+的分子立体结构为:
(5)周期表中最活泼的非金属元素原子的轨道表示式为
更新时间:2024-05-24 22:57:33
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】11.0 g由12H和818O组成的水分子,其中含中子数为_______ mol,电子数为________ mol。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有① 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、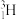 ,以上四组微粒或物质中:
,以上四组微粒或物质中:
(1)属于互为同位素关系的是_______ ;
(2)互为同素异形体关系的是_______ ;
(3)第②组代表的各物质的物理性质相同吗?_______ ;化学性质相同吗?_______ ;
(4)由①和④的各核素组成的三原子化合物(水)的相对分子质量中最小的一种摩尔质量是____ 。
 、
、 、
、 ;②H2、D2、T2;③石墨、金刚石;④
;②H2、D2、T2;③石墨、金刚石;④ 、
、 、
、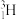 ,以上四组微粒或物质中:
,以上四组微粒或物质中:(1)属于互为同位素关系的是
(2)互为同素异形体关系的是
(3)第②组代表的各物质的物理性质相同吗?
(4)由①和④的各核素组成的三原子化合物(水)的相对分子质量中最小的一种摩尔质量是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)元素原子的价电子构型为3s23p3,它属于第________ 周期,是______ 族,元素符号是________ 。
(2)在HCl分子中,由H原子的一个____ 轨道与Cl原子的一个_____ 轨道形成一个____ 键;在Cl2分子中两个Cl原子以2个____ 轨道形成一个 ____ 键。
(2)在HCl分子中,由H原子的一个
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】钴(Co)及其化合物是一种应用广泛的金属及其化合物,可用做催化剂、半导体等;草酸铵(NH4)2C2O4用于制取草酸钴的反应为(NH4)2C2O4+CoCl=CoC2O4+2NH4Cl。
(1)27Co在元素周期表的位置是_______ 。其基态原子的价层电子排布式_______ 。
(2)NH 中的氮原子的杂化轨道类型是
中的氮原子的杂化轨道类型是_______ 。NH 的空间构型是
的空间构型是_______ 。
(1)27Co在元素周期表的位置是
(2)NH
 中的氮原子的杂化轨道类型是
中的氮原子的杂化轨道类型是 的空间构型是
的空间构型是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式:___________ ;写出基态 原子的价层电子排布图:
原子的价层电子排布图:___________ ;
(2)Mg基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了___________ 。
(3)常温下,等浓度的氟乙酸比氯乙酸的酸性更___________ (填“强”或“弱”),从物质结构角度说明其原因:___________ 。
(1)写出基态S原子的核外电子排布式:
 原子的价层电子排布图:
原子的价层电子排布图:(2)Mg基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(3)常温下,等浓度的氟乙酸比氯乙酸的酸性更
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)X射线衍射测定等发现,I3AsF6中存在I 。I
。I 的空间结构为
的空间结构为___ ,中心原子的杂化形式为___ 。
(2)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为CH2=CH—CH2OH。请回答下列问题:
①基态镍原子的价电子排布图为____ 。
②烯丙醇分子中碳原子的杂化类型是___ 。
(3)乙炔是有机合成的一种重要原料。将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀。基态Cu+的简化电子排布式为____ 。
(1)X射线衍射测定等发现,I3AsF6中存在I
 。I
。I 的空间结构为
的空间结构为(2)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为CH2=CH—CH2OH。请回答下列问题:
①基态镍原子的价电子排布图为
②烯丙醇分子中碳原子的杂化类型是
(3)乙炔是有机合成的一种重要原料。将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀。基态Cu+的简化电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN3)是一种弱酸,其分子结构可表示为H—N=N≡N,肼(N2H4)被亚硝酸氧化时便可得到氢叠氮酸(HN3),发生的反应为N2H4+HNO2=2H2O+HN3。HN3的酸性和醋酸相近,可微弱电离出H+和N3-。试回答下列问题:
(1)下列有关说法正确的是___ (填序号)。
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.HNO2是强酸
(2)叠氮酸根(N3-)能与许多金属离子等形成配合物,如:[Co(N3)(NH3)5]SO4,在该配合物中钴显___ 价,配位数是___ 。
(5)根据价层电子对互斥理论判断N3-的空间构型为___ 。与N3-互为等电子体的分子有___ (写一种即可)。
(1)下列有关说法正确的是
A.HN3中含有5个σ键
B.HN3中的三个氮原子均采用sp2杂化
C.HN3、HNO2、H2O、N2H4都是极性分子
D.HNO2是强酸
(2)叠氮酸根(N3-)能与许多金属离子等形成配合物,如:[Co(N3)(NH3)5]SO4,在该配合物中钴显
(5)根据价层电子对互斥理论判断N3-的空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】用价层电子对互斥理论预测下列粒子的立体结构。
(1)H2Se____________ ;
(2)BCl3____________ ;
(3)PCl3____________ ;
(4)CO2____________ ;
(5)SO2____________ ;
(6)SO42-________________ 。
(1)H2Se
(2)BCl3
(3)PCl3
(4)CO2
(5)SO2
(6)SO42-
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】人类从石器时代经历了漫长的青铜时代才进入铁器时代,是铜支撑了人类文明数千年的发展,而黄铜矿(主要成分为CuFeS2)是工业炼铜的最主要矿物原料。回答下列问题:
(1)基态Cu原子的价电子排布式为_______ ;其基态原子有_______ 种空间运动状态。
(2)铁元素常见价态有Fe2+和Fe3+,稳定性:Fe2+_______ Fe3+(填“>”“<”“=”),原因是_______ 。
(3)SO2、SO3、SO 、SO
、SO 四种含硫微粒中,中心原子为sp3杂化的是
四种含硫微粒中,中心原子为sp3杂化的是_______ ;SO 的空间构型是
的空间构型是_______ 。
(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用−
表示,与之相反的用− 表示,称为电子的自旋量子数。对于基态Cu原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋量子数。对于基态Cu原子,其价电子自旋磁量子数的代数和为_______ 。
(1)基态Cu原子的价电子排布式为
(2)铁元素常见价态有Fe2+和Fe3+,稳定性:Fe2+
(3)SO2、SO3、SO
 、SO
、SO 四种含硫微粒中,中心原子为sp3杂化的是
四种含硫微粒中,中心原子为sp3杂化的是 的空间构型是
的空间构型是(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用−
表示,与之相反的用− 表示,称为电子的自旋量子数。对于基态Cu原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋量子数。对于基态Cu原子,其价电子自旋磁量子数的代数和为
您最近一年使用:0次

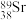 可用于医疗领域中的核素治疗,从而近距离精准杀伤病变细胞。
可用于医疗领域中的核素治疗,从而近距离精准杀伤病变细胞。 二者互为
二者互为 的空间构型为
的空间构型为

