根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的核外电子排布式:___________ ;写出基态 原子的价层电子排布图:
原子的价层电子排布图:___________ ;
(2)Mg基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了___________ 。
(3)常温下,等浓度的氟乙酸比氯乙酸的酸性更___________ (填“强”或“弱”),从物质结构角度说明其原因:___________ 。
(1)写出基态S原子的核外电子排布式:
 原子的价层电子排布图:
原子的价层电子排布图:(2)Mg基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(3)常温下,等浓度的氟乙酸比氯乙酸的酸性更
更新时间:2023-06-23 22:20:58
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】合成氨是人类科学技术发展史上的一项重大成就:催化剂,高温高压条件下: +
+ ⇌
⇌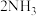
目前合成氨工业中使用的催化剂铁触媒中主要成分为Fe3O4(Fe2O3和FeO),还含有少量的K2O、Al2O3、CuO、TiO2、Cr2O3等。回答问题:
(1)基态N原子中,有___________ 种空间运动状态不同的电子。
(2)与 同族且相邻周期的元素
同族且相邻周期的元素 的基态原子价电子排布式为
的基态原子价电子排布式为___________ 。与钛同周期元素的基态原子中,未成对电子数与钛相同的元素有___________ 种。
(3)24Cr基态原子中未成对电子的自旋状态相同,则两种自旋状态的电子数之比为___________
(4)分析Cu、Zn的核外电子排布,推测Cu的第二电离能I2___________ Zn的第二电离能I2.(填写“大于”“小于”或“等于”)
(5)H+可与NH3形成NH 。NH
。NH 中H—N—H键角比NH3中H—N—H键角大,原因是
中H—N—H键角比NH3中H—N—H键角大,原因是___________ 。预测NH3中H—N—H键角___________ NF3中F—N—F键角(填写“大于”“小于”或“等于”)
(6)邻二氮菲( )分子中N杂化方式为
)分子中N杂化方式为___________ 。
 +
+ ⇌
⇌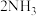
目前合成氨工业中使用的催化剂铁触媒中主要成分为Fe3O4(Fe2O3和FeO),还含有少量的K2O、Al2O3、CuO、TiO2、Cr2O3等。回答问题:
(1)基态N原子中,有
(2)与
 同族且相邻周期的元素
同族且相邻周期的元素 的基态原子价电子排布式为
的基态原子价电子排布式为(3)24Cr基态原子中未成对电子的自旋状态相同,则两种自旋状态的电子数之比为
(4)分析Cu、Zn的核外电子排布,推测Cu的第二电离能I2
(5)H+可与NH3形成NH
 。NH
。NH 中H—N—H键角比NH3中H—N—H键角大,原因是
中H—N—H键角比NH3中H—N—H键角大,原因是(6)邻二氮菲(
 )分子中N杂化方式为
)分子中N杂化方式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知元素周期表中共有18个纵列,如图实线表示元素周期表的边界。按电子排布,可把周期表划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入电子的能级符号。
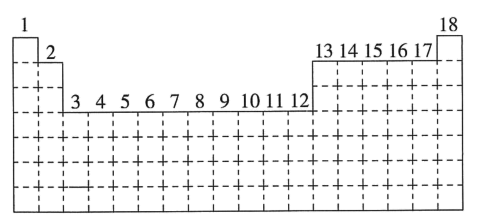
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影 和
和 表示d区和ds区
表示d区和ds区____ 。
(2)有的同学受这种划分的启发,认为d区内6、7纵列的部分元素可以排在另一区,你认为应排在_____ 区。
(3)请在元素周期表中用元素符号标出4s轨道处于半充满状态的元素____ 。

(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影
 和
和 表示d区和ds区
表示d区和ds区(2)有的同学受这种划分的启发,认为d区内6、7纵列的部分元素可以排在另一区,你认为应排在
(3)请在元素周期表中用元素符号标出4s轨道处于半充满状态的元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】A、B、C代表3种元素。请填空:
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:_______________________________ ,核外电子运动状态有_______ 种。
(2)B是原子序数为35的元素,其原子中有___________ 个电子层,有_________ 个能级。
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为_________________ ,其单质在一定条件下能与浓硫酸反应,试写出该反应方程式:____________ 。
(1)A的原子的3p轨道上只有1个电子的自旋方向与其他电子的自旋方向相反,写出该原子价电子的轨道表示式:
(2)B是原子序数为35的元素,其原子中有
(3)C元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,元C素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】回答下列问题
(1)基态二价铜离子的核外电子排布式为__________ 。已知高温下 比
比 更稳定,试从核外电子排布角度解释:
更稳定,试从核外电子排布角度解释:__________________________ 。
(2)镍的基态原子的价电子的电子排布图(轨道表示式)为_____________________ 。
(3)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为__________ ,铬原子的价电子排布式为____________________________ 。
(4)钴元素的常见价态为 和
和 。写出
。写出 价基态钴离子的价电子的电子排布图:
价基态钴离子的价电子的电子排布图:________________ 。
(5)基态钒原子的价层电子排布式是________________ 。
(6)Mn的价电子排布式为____________ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用____________ 理论解释。
(1)基态二价铜离子的核外电子排布式为
 比
比 更稳定,试从核外电子排布角度解释:
更稳定,试从核外电子排布角度解释:(2)镍的基态原子的价电子的电子排布图(轨道表示式)为
(3)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态
 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为(4)钴元素的常见价态为
 和
和 。写出
。写出 价基态钴离子的价电子的电子排布图:
价基态钴离子的价电子的电子排布图:(5)基态钒原子的价层电子排布式是
(6)Mn的价电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氮、磷、砷是同主族元素,均广泛用于农药、化肥等化工产品,请回答下列问题。
(1)画出基态砷原子价层电子的轨道表示式_______ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为_______ (填化学式)。NH3、PH3、AsH3稳定性由强到弱的顺序为_______ (填化学式)。
(3)水和氨中心原子的杂化类型相同,但H2O的键角小于NH3的,其原因为_______ 。
(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为_______ 。
(5)已知有关氮、磷的单键和三键的键能(kJ·mol-1)如表:
请你预测键长:N—N_______ N≡N(填“>”或“<”),从N2、N4、P2、P4的能量角度看,氮气以N2而白磷以P4形式存在的原因是_______ 。
(6)2022年起,曾经的“天价药”诺西那生钠正式实施医保价格,一针直降几十万元人民币。诺西那生钠,用于治疗脊髓性肌肉菱缩症(SMA)。其结构片段如图所示。
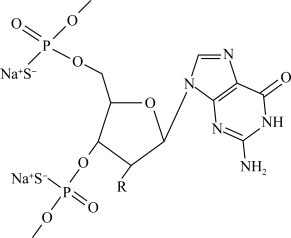 (R为OCH2CH2OCH3)
(R为OCH2CH2OCH3)
该结构片段中含有_______ 个手性碳原子。
(1)画出基态砷原子价层电子的轨道表示式
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
(3)水和氨中心原子的杂化类型相同,但H2O的键角小于NH3的,其原因为
(4)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的磷原子,其价电子自旋磁量子数的代数和为(5)已知有关氮、磷的单键和三键的键能(kJ·mol-1)如表:
| N—N | N≡N | P—-P | P≡P |
| 193 | 946 | 197 | 489 |
请你预测键长:N—N
(6)2022年起,曾经的“天价药”诺西那生钠正式实施医保价格,一针直降几十万元人民币。诺西那生钠,用于治疗脊髓性肌肉菱缩症(SMA)。其结构片段如图所示。
 (R为OCH2CH2OCH3)
(R为OCH2CH2OCH3)该结构片段中含有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】Ⅰ.按照要求将相应序号填入空白中:
① ②金刚石 ③CO ④CO2 ⑤37Cl ⑥
②金刚石 ③CO ④CO2 ⑤37Cl ⑥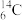 ⑦SO2 ⑧
⑦SO2 ⑧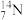 ⑨石墨 ⑩C60
⑨石墨 ⑩C60
(1)_______________ 互为同位素
(2)________________ 为酸性氧化物
(3)________________ 的质量数相等,但不能互为同位素
(4)________________ 互称同素异形体
Ⅱ.已知微粒间的相互作用有以下几种:
①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力(范德华力)
下面是某同学对一些变化过程破坏的微粒间的相互作用的判断:
A.干冰熔化②⑤
B.氢氧化钠溶于水①
C.氯化氢气体溶于水②④
D.冰熔化④⑤
E.Na2O2溶于水①②
其中判断正确选项的是_____
①
 ②金刚石 ③CO ④CO2 ⑤37Cl ⑥
②金刚石 ③CO ④CO2 ⑤37Cl ⑥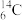 ⑦SO2 ⑧
⑦SO2 ⑧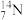 ⑨石墨 ⑩C60
⑨石墨 ⑩C60(1)
(2)
(3)
(4)
Ⅱ.已知微粒间的相互作用有以下几种:
①离子键 ②极性共价键 ③非极性共价键 ④氢键 ⑤分子间作用力(范德华力)
下面是某同学对一些变化过程破坏的微粒间的相互作用的判断:
A.干冰熔化②⑤
B.氢氧化钠溶于水①
C.氯化氢气体溶于水②④
D.冰熔化④⑤
E.Na2O2溶于水①②
其中判断正确选项的是
您最近一年使用:0次
【推荐2】有下列8种晶体,用序号回答下列问题:
A.水晶 B.冰醋酸 C.白磷 D.固态氩 E.氯化铵 F.铝 G.金刚石
(1)属于原子晶体的化合物是___ ,直接由原子构成的分子晶体是___ 。
(2)由极性分子构成的晶体是___ ;含有共价键的离子晶体是___ 。
(3)分子内存在化学键,但受热熔化时,化学键不发生变化的是___ ,受热熔化,需克服共价键的是___ 。
A.水晶 B.冰醋酸 C.白磷 D.固态氩 E.氯化铵 F.铝 G.金刚石
(1)属于原子晶体的化合物是
(2)由极性分子构成的晶体是
(3)分子内存在化学键,但受热熔化时,化学键不发生变化的是
您最近一年使用:0次

 相同,其基态原子的电子排布式为
相同,其基态原子的电子排布式为 中,存在的微粒间作用力有
中,存在的微粒间作用力有

