回答下列问题
(1)基态二价铜离子的核外电子排布式为__________ 。已知高温下 比
比 更稳定,试从核外电子排布角度解释:
更稳定,试从核外电子排布角度解释:__________________________ 。
(2)镍的基态原子的价电子的电子排布图(轨道表示式)为_____________________ 。
(3)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为__________ ,铬原子的价电子排布式为____________________________ 。
(4)钴元素的常见价态为 和
和 。写出
。写出 价基态钴离子的价电子的电子排布图:
价基态钴离子的价电子的电子排布图:________________ 。
(5)基态钒原子的价层电子排布式是________________ 。
(6)Mn的价电子排布式为____________ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用____________ 理论解释。
(1)基态二价铜离子的核外电子排布式为
 比
比 更稳定,试从核外电子排布角度解释:
更稳定,试从核外电子排布角度解释:(2)镍的基态原子的价电子的电子排布图(轨道表示式)为
(3)铬是一种硬而脆、抗腐蚀性强的金属,常用于电镀和制造特种钢。基态
 原子中,电子占据最高能层的符号为
原子中,电子占据最高能层的符号为(4)钴元素的常见价态为
 和
和 。写出
。写出 价基态钴离子的价电子的电子排布图:
价基态钴离子的价电子的电子排布图:(5)基态钒原子的价层电子排布式是
(6)Mn的价电子排布式为
2023高三·全国·专题练习 查看更多[1]
(已下线)题型72 基态粒子核外电子排布的表示方法
更新时间:2023-02-17 11:32:48
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】Goodenough等人因在锂离子电池及钴酸锂、磷酸铁锂等正极材料研究方面的卓越贡献而获得2019年诺贝尔化学奖。回答下列问题:
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为_______ 。
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。I1(Li)>I1(Na),原因是_______ 。I1(Be)>I1(B)>I1(Li),原因是_______ 。
(3)磷酸根离子的空间构型为_______ ,其中P的价层电子对数为_______ 、杂化轨道类型为_______ 。
(1)基态Fe2+与Fe3+离子中未成对的电子数之比为
(2)Li及其周期表中相邻元素的第一电离能(I1)如表所示。I1(Li)>I1(Na),原因是
(3)磷酸根离子的空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】基态原子的核外电子填充在6个轨道中的元素有___________ 种,填充在7个轨道中的元素有___________ 种。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】已知某元素原子的电子排布式是1s22s22p63s23p63d104s24p1。
(1)该元素的原子序数为___________ 。
(2)该元素位于第_______ 周期_________ 族。
(3)该原子的电子总数为_________ ,价电子总数为_________ 。
(1)该元素的原子序数为
(2)该元素位于第
(3)该原子的电子总数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素。相关信息如下:
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是________________ ,离子化合物YX5的电子式是_________ 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是________ 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐)。A晶体的晶胞为正方体(如图)。
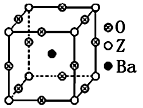
①制备A的化学方程式是_________________________________________ ;
②在A晶体中,Z的配位数为_______________ ;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的______________ 。
(4)R2+离子的外围电子层电子排布式为______________ 。R2O的熔点比R2S的________ (填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B。B晶体的晶胞为正方体(如图),若晶胞棱长为540.0 pm,则晶胞密度为___________________________ g·cm−3(列式并计算)。
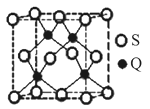 。
。
| X元素是宇宙中最丰富的元素 |
| Y元素基态原子的核外p电子数比s电子数少1 |
| Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
| R元素在元素周期表的第十一列 |
| Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐)。A晶体的晶胞为正方体(如图)。

①制备A的化学方程式是
②在A晶体中,Z的配位数为
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的
(4)R2+离子的外围电子层电子排布式为
(5)Q元素和硫(S)元素能够形成化合物B。B晶体的晶胞为正方体(如图),若晶胞棱长为540.0 pm,则晶胞密度为
 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】近期我国科研工作者研究的金属—氮—碳优异电催化 还原催化剂取得新进展。回答下列问题:
还原催化剂取得新进展。回答下列问题:
(1) 可用于考古,其中子数为
可用于考古,其中子数为___________ ,该基态原子价层电子轨道表示式为___________ 。
(2)研究发现钴—氮—碳优异电催化 还原催化剂活性最高,金属钴的核外电子排布式为
还原催化剂活性最高,金属钴的核外电子排布式为___________ ;基态 未成对电子数为
未成对电子数为___________ 。
(3)基态N原子中,电子占据的最高能层符号为___________ ,该能层具有的原子轨道数为___________ ,电子数为___________ 。
 还原催化剂取得新进展。回答下列问题:
还原催化剂取得新进展。回答下列问题:(1)
 可用于考古,其中子数为
可用于考古,其中子数为(2)研究发现钴—氮—碳优异电催化
 还原催化剂活性最高,金属钴的核外电子排布式为
还原催化剂活性最高,金属钴的核外电子排布式为 未成对电子数为
未成对电子数为(3)基态N原子中,电子占据的最高能层符号为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)①基态A原子的电子排布式为 ,则A元素位于第
,则A元素位于第_______ 周期第_______ 族,属于_______ 区元素。
②基态B原子的简化电子排布式为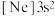 ,则B元素位于第
,则B元素位于第_______ 周期第_______ 族,属于_______ 区元素。
③基态C原子的电子排布式为 ,则C元素位于第
,则C元素位于第_______ 周期第_______ 族,属于_______ 区元素。
(2)①基态Fe原子有_______ 个未成对电子, 基态的核外电子排布式为
基态的核外电子排布式为_______ 。
②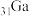 基态原子的价层电子排布式为
基态原子的价层电子排布式为_______ 。
③基态硼原子的电子排布式为_______ 。
④基态 的核外电子排布式为
的核外电子排布式为_______ 。
⑤ 是红棕色气体;X与氢元素可形成
是红棕色气体;X与氢元素可形成 ;X基态原子的价层电子轨道表示式是
;X基态原子的价层电子轨道表示式是_______ 。
(1)①基态A原子的电子排布式为
 ,则A元素位于第
,则A元素位于第②基态B原子的简化电子排布式为
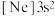 ,则B元素位于第
,则B元素位于第③基态C原子的电子排布式为
 ,则C元素位于第
,则C元素位于第(2)①基态Fe原子有
 基态的核外电子排布式为
基态的核外电子排布式为②
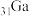 基态原子的价层电子排布式为
基态原子的价层电子排布式为③基态硼原子的电子排布式为
④基态
 的核外电子排布式为
的核外电子排布式为⑤
 是红棕色气体;X与氢元素可形成
是红棕色气体;X与氢元素可形成 ;X基态原子的价层电子轨道表示式是
;X基态原子的价层电子轨道表示式是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)在下列物质中,_____ 是晶体(填序号,下同),_____ 是非晶体。
①塑料 ②明矾 ③松香 ④玻璃 ⑤CuSO4·5H2O ⑥冰糖 ⑦石蜡 ⑧单晶硅 ⑨铝块 ⑩橡胶
(2)晶体和非晶体在外形上有差别,晶体一般都具有_____ ,而非晶体_____ ;另外非晶体具有物理性质_____ 的特点,而晶体具有物理性质_____ 的特点。
(1)在下列物质中,
①塑料 ②明矾 ③松香 ④玻璃 ⑤CuSO4·5H2O ⑥冰糖 ⑦石蜡 ⑧单晶硅 ⑨铝块 ⑩橡胶
(2)晶体和非晶体在外形上有差别,晶体一般都具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】自然界中许多固态物质都是晶体,它们们有规则的几何外形,如晶莹的雪花、玲珑剔透的石英、棱角分明的食盐固体和许多矿石。我们的生活因此而多美丽。
(1)区分晶体和非晶体最科学的方法是_________ (填选项序号,下同)
A.比较硬度 B.对固体进行X射线衍射 C.看是否有规则的几何外形
(2)下列各组物质的晶体中,化学键类型、晶体类型都相同的是
(3)下列物质性质的变化规律,与化学键的强弱无关的是
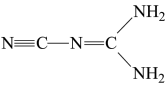
(4)某物质(结构简式如图所示)可溶于水、乙醇,熔点为209.5 ℃。下列说法不正确的是 。
(5)随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N 等已被发现。下列有关说法中,正确的是 。
等已被发现。下列有关说法中,正确的是 。
(1)区分晶体和非晶体最科学的方法是
A.比较硬度 B.对固体进行X射线衍射 C.看是否有规则的几何外形
(2)下列各组物质的晶体中,化学键类型、晶体类型都相同的是
| A.CO2和SO2 | B.NaCl和HCl | C.H2S和H2O | D.CF2Cl2和CH3COONa |
(3)下列物质性质的变化规律,与化学键的强弱无关的是
| A.金刚石的硬度、熔点、沸点都高于晶体硅 |
| B.Li、Na、K、Rb的熔点、沸点逐渐降低 |
| C.NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D.F2、Cl2、Br2、I2的熔点、沸点逐渐升高 |
(4)某物质(结构简式如图所示)可溶于水、乙醇,熔点为209.5 ℃。下列说法不正确的是 。

| A.该物质为共价晶体 |
| B.该物质分子中含有极性共价键 |
| C.该物质分子中σ键和π键的个数比为3∶1 |
| D.该物质分子中每个原子最外层均达到8电子稳定结构 |
(5)随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60、N
 等已被发现。下列有关说法中,正确的是 。
等已被发现。下列有关说法中,正确的是 。| A.H2 与 H3 中存在氢键 | B.O2 与 O4 互为同位素 |
| C.C60 分子中有范德华力 | D.N 中含有 24 个价电子 中含有 24 个价电子 |
您最近一年使用:0次

 和
和 的价层电子排布式
的价层电子排布式

