已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素。相关信息如下:
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是________________ ,离子化合物YX5的电子式是_________ 。
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是________ 个。
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐)。A晶体的晶胞为正方体(如图)。
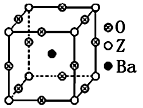
①制备A的化学方程式是_________________________________________ ;
②在A晶体中,Z的配位数为_______________ ;
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的______________ 。
(4)R2+离子的外围电子层电子排布式为______________ 。R2O的熔点比R2S的________ (填“高”或“低”)。
(5)Q元素和硫(S)元素能够形成化合物B。B晶体的晶胞为正方体(如图),若晶胞棱长为540.0 pm,则晶胞密度为___________________________ g·cm−3(列式并计算)。
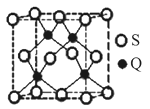 。
。
| X元素是宇宙中最丰富的元素 |
| Y元素基态原子的核外p电子数比s电子数少1 |
| Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
| R元素在元素周期表的第十一列 |
| Q元素在周期表里与R元素在同一个分区 |
请回答下列问题:
(1)YX3中心原子的杂化轨道类型是
(2)CO与Y2属于等电子体,1 个CO分子中含有的π键数目是
(3)工业上利用ZO2和碳酸钡在熔融状态下制取化合物A(A可看做一种含氧酸盐)。A晶体的晶胞为正方体(如图)。

①制备A的化学方程式是
②在A晶体中,Z的配位数为
③在A晶体中,若将Z元素置于立方体的体心,Ba元素置于立方体的顶点,则O元素处于立方体的
(4)R2+离子的外围电子层电子排布式为
(5)Q元素和硫(S)元素能够形成化合物B。B晶体的晶胞为正方体(如图),若晶胞棱长为540.0 pm,则晶胞密度为
 。
。
15-16高三下·吉林·阶段练习 查看更多[4]
四川省威远县龙会中学2019-2020学年高二12月月考化学试题(已下线)解密21 物质的结构与性质(教师版)——备战2018年高考化学之高频考点解密2016届吉林省吉林市高三第三次调研理综化学试卷2016届吉林省吉林市高三下第三次调研理综化学试卷
更新时间:2016-12-09 07:08:23
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】 、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):

(1) 、金刚石和石墨三者的关系是互为_______。
、金刚石和石墨三者的关系是互为_______。
(2)固态时, 属于
属于_______ (填“离子”“共价”或“分子”)晶体。
(3)试根据金刚石和 的结构特点判断两者熔点的高低,并说明理由
的结构特点判断两者熔点的高低,并说明理由_______ 。
(4)硅晶体的结构跟金刚石相似, 硅晶体中含有
硅晶体中含有 键的数目是
键的数目是_______  个。
个。
(5)石墨层状结构中,平均每个正六边形占有的碳原子数是_______ 。
 、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
(1)
 、金刚石和石墨三者的关系是互为_______。
、金刚石和石墨三者的关系是互为_______。| A.同分异构体 | B.同素异形体 | C.同系物 | D.同位素 |
 属于
属于(3)试根据金刚石和
 的结构特点判断两者熔点的高低,并说明理由
的结构特点判断两者熔点的高低,并说明理由(4)硅晶体的结构跟金刚石相似,
 硅晶体中含有
硅晶体中含有 键的数目是
键的数目是 个。
个。(5)石墨层状结构中,平均每个正六边形占有的碳原子数是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知:A.金刚石、B.MgF2、C.NH4Cl、D.NaNO3、E.干冰、F.固体碘,填写下列空白。(用序号填写)
(1)熔化时不需破坏化学键的是________ ,熔化时只需破坏共价键的是________ ,熔点最高的是________ ,熔点最低的是________ 。
(2)晶体中既存在离子键又存在共价键的是________ ,只存在离子键的是________ 。
(3)由极性键构成的非极性分子是________ 。
(1)熔化时不需破坏化学键的是
(2)晶体中既存在离子键又存在共价键的是
(3)由极性键构成的非极性分子是
您最近一年使用:0次
【推荐3】Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
回答下列问题:
(1)亚铁离子价电子层的电子排布式为_______
(2) Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是_______ ;
②六氰合亚铁离子(Fe(CN)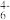 )中的配体CN-中C原子的杂化轨道类型是
)中的配体CN-中C原子的杂化轨道类型是_______ ,写出一种与CN-互为等电子体的单质分子的电子式_______ ;
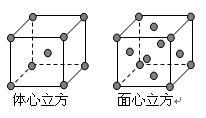
(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为_______ 。
元 素 | Mn | Fe | |
电离能/kJ·mol-1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
回答下列问题:
(1)亚铁离子价电子层的电子排布式为
(2) Fe原子或离子外围有较多能量相近的空轨道而能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子(Fe(CN)
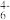 )中的配体CN-中C原子的杂化轨道类型是
)中的配体CN-中C原子的杂化轨道类型是(3)金属铁的晶体在不同温度下有两种堆积方式,晶胞分别如右图所示。体心立方晶胞和面心立方晶胞中实际含有的Fe原子个数之比为

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】按要求写出下列化学用语
(1)NaOH的电子式___________________ (2)S原子核外电子排布式___________
(3)O原子的电子排布图______________ (4)Cl-离子的结构示意图___________
(1)NaOH的电子式
(3)O原子的电子排布图
您最近一年使用:0次
【推荐2】某元素的激发态(不稳定状态)原子的电子排布式为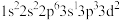 ,则该元素基态原子的电子排布式为
,则该元素基态原子的电子排布式为 _______ ;其最高价氧化物对应水化物的化学式是 ______ 。
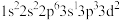 ,则该元素基态原子的电子排布式为
,则该元素基态原子的电子排布式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_____ (填字母)。
A. 碳与水蒸气反应
B. 铝和氧化铁反应
C. CaCO3受热分解
D. 氢气还原三氧化钨制取钨
E. 锌与盐酸反应
(2)获取能量变化的途径
①已知:
则:SiCl4(g)+2H2(g)= Si(s)+4HCl(g)的反应热
_____ 
②已知在常温常压下:
i、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)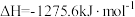
ii、H2O(l)=H2O(g)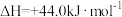
写出表示甲醇燃烧热的热化学方程式_____ 。
(3)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则负极的电极反应式为____________ 。
(4)最近科学家研制出超薄铁磁β-MnSe半导体,β-MnSe的晶胞结构如图所示。
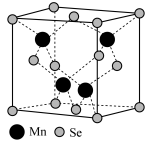
①β-MnSe中Mn的配位数为_______ 。
②Mn2+的价电子排布式为_______ 。
(1)下列反应中,属于放热反应的是
A. 碳与水蒸气反应
B. 铝和氧化铁反应
C. CaCO3受热分解
D. 氢气还原三氧化钨制取钨
E. 锌与盐酸反应
(2)获取能量变化的途径
①已知:
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能(kJ·mol-1) | 460 | 360 | 436 | 431 | 176 | 347 |


②已知在常温常压下:
i、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)
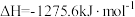
ii、H2O(l)=H2O(g)
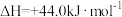
写出表示甲醇燃烧热的热化学方程式
(3)用甲烷或其他有机物、氧气为原料可设计成原电池,以CnH2nOn、O2为原料,硫酸溶液为电解质设计成燃料电池,则负极的电极反应式为
(4)最近科学家研制出超薄铁磁β-MnSe半导体,β-MnSe的晶胞结构如图所示。

①β-MnSe中Mn的配位数为
②Mn2+的价电子排布式为
您最近一年使用:0次
【推荐2】Wilson病是一种先天性铜代谢障碍性疾病,D-青霉胺具有排铜作用,用以治疗或控制Wilson病症。D-青霉胺结构简式如下:

回答下列问题:
(1)写出Cu的简化电子排布式:_______ 。
(2)D-青霉胺在用于临床治疗时对于症状改善较慢,常有并发症出现,因而近年采用锌剂(ZnSO4)替代治疗,ZnSO4可由硫化锌制备。立方硫化锌晶胞结构如图:

其中a代表S2-,b代表Zn2+。则该晶体中S2-的配位数为_______ ;若晶体的密度为ρ g/cm3,则1个晶胞的体积为_______ cm3(设NA为阿伏加德罗常数的值,列出计算式)。

回答下列问题:
(1)写出Cu的简化电子排布式:
(2)D-青霉胺在用于临床治疗时对于症状改善较慢,常有并发症出现,因而近年采用锌剂(ZnSO4)替代治疗,ZnSO4可由硫化锌制备。立方硫化锌晶胞结构如图:

其中a代表S2-,b代表Zn2+。则该晶体中S2-的配位数为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】晶胞
(1)概念:描述晶体结构的_______ 。
(2)结构:晶胞一般都是_______ ,晶体是由无数晶胞_______ 而成。
①无隙:相邻晶胞之间无任何间隙。
②并置:所有晶胞都是平行排列的,取向相同。
③所有晶胞的形状及其内部的原子种类、个数及几何排列是_______ 的。
(3)晶胞中粒子数目的计算
平行六面体(立方体形)晶胞中粒子数目的计算。
①晶胞的顶角原子是_______ 个晶胞共用;
②晶胞棱上的原子是_______ 个晶胞共用;
③晶胞面上的原子是_______ 个晶胞共用。
提示:由晶胞构成的晶体,其化学式不表示一个分子中原子的数目,只表示每个晶胞中各类原子的_______ 。
(1)概念:描述晶体结构的
(2)结构:晶胞一般都是
①无隙:相邻晶胞之间无任何间隙。
②并置:所有晶胞都是平行排列的,取向相同。
③所有晶胞的形状及其内部的原子种类、个数及几何排列是
(3)晶胞中粒子数目的计算
平行六面体(立方体形)晶胞中粒子数目的计算。
①晶胞的顶角原子是
②晶胞棱上的原子是
③晶胞面上的原子是
提示:由晶胞构成的晶体,其化学式不表示一个分子中原子的数目,只表示每个晶胞中各类原子的
您最近一年使用:0次



