 、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
(1)
 、金刚石和石墨三者的关系是互为_______。
、金刚石和石墨三者的关系是互为_______。| A.同分异构体 | B.同素异形体 | C.同系物 | D.同位素 |
 属于
属于(3)试根据金刚石和
 的结构特点判断两者熔点的高低,并说明理由
的结构特点判断两者熔点的高低,并说明理由(4)硅晶体的结构跟金刚石相似,
 硅晶体中含有
硅晶体中含有 键的数目是
键的数目是 个。
个。(5)石墨层状结构中,平均每个正六边形占有的碳原子数是
更新时间:2022-11-25 09:56:36
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】某种水性钠离子电池电极材料属于配位化合物,使用过程中电极 嵌入或脱嵌,变化如下:
嵌入或脱嵌,变化如下: ,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略
,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶胞示意图如图1,嵌入和脱嵌过程中
的晶胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑
均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:
,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:

回答下列问题:
(1)原子中电子有两种自旋状态,可分别用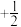 和
和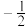 表示,称为电子的自旋磁量子数。则
表示,称为电子的自旋磁量子数。则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为_______ ;从结构上分析基态 、
、 ,
,_______ 更稳定,原因是_______ 。
(2)配位化合物X中,N原子的杂化类型是_______ , 的配位数是
的配位数是_______ ,X中 键和
键和 键的数目之比为
键的数目之比为_______ 。
(3)脱嵌过程该电极发生_______ 反应(填“氧化”或“还原”),作_______ 极(填“阴”或“阳”);格林绿、普鲁士蓝、普鲁士白的化学式可用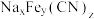 表示,后两者的化学式依次是
表示,后两者的化学式依次是_______ 、_______ 。
 嵌入或脱嵌,变化如下:
嵌入或脱嵌,变化如下: ,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略
,格林绿、普鲁士蓝、普鲁士白均为立方晶胞,省略 的晶胞示意图如图1,嵌入和脱嵌过程中
的晶胞示意图如图1,嵌入和脱嵌过程中 均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑
均填充在小立方体的体心,X为三种晶体中的其中一种,如果不考虑 ,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:
,所有微粒都只有一种化学环境,从X中切出的部分结构如图2所示:
回答下列问题:
(1)原子中电子有两种自旋状态,可分别用
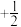 和
和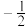 表示,称为电子的自旋磁量子数。则
表示,称为电子的自旋磁量子数。则 中电子自旋磁量子数的代数和为
中电子自旋磁量子数的代数和为 、
、 ,
,(2)配位化合物X中,N原子的杂化类型是
 的配位数是
的配位数是 键和
键和 键的数目之比为
键的数目之比为(3)脱嵌过程该电极发生
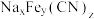 表示,后两者的化学式依次是
表示,后两者的化学式依次是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】铁及其化合物用途非常广泛,如二茂铁可用作火箭燃料添加剂,铁酸锶用于直流电机永久陶瓷磁铁。用环戊二烯钠法制备二茂铁(如图)的原理为C5H6+NaOH→C5H5Na+H2O;2C5H5Na+FeCl2→(C5H5)2Fe+2NaCl。

(1)铁元素的基态价电子排布式为________________ 。
(2)基态Na原子中,核外电子占据的最高能级的符号是________ ,占据该能层电子的电子云轮廓图形状为________ 。Na和K属于同一主族,但金属Na的熔点比金属K高,原因是______________ 。
(3)(C5H5)2Fe中阴离子 中的σ键总数为
中的σ键总数为____ 个。分子中的大π键可用符号II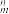 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Ⅱ
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Ⅱ ),则
),则 中的大π键应表示为
中的大π键应表示为________________ 。
(4)用二乙胺法合成二茂铁的原料有(C2H5)2NH、FeCl2·4H2O及C5H6。(C2H5)2NH分子中采用sp3杂化的原子是________ ;FeCl2·4H2O是一种配合物,其结构如图所示,Fe2+与配体之间形成的化学键称为____________ 。

(5)铁酸锶的晶胞结构如下图所示:

①晶胞中距离最近的两个氧原子的距离为________ cm(列出计算表达式即可)。
②该晶体的密度为_____________ g·cm-3(列出计算表达式即可)。

(1)铁元素的基态价电子排布式为
(2)基态Na原子中,核外电子占据的最高能级的符号是
(3)(C5H5)2Fe中阴离子
 中的σ键总数为
中的σ键总数为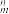 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Ⅱ
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Ⅱ ),则
),则 中的大π键应表示为
中的大π键应表示为(4)用二乙胺法合成二茂铁的原料有(C2H5)2NH、FeCl2·4H2O及C5H6。(C2H5)2NH分子中采用sp3杂化的原子是

(5)铁酸锶的晶胞结构如下图所示:

①晶胞中距离最近的两个氧原子的距离为
②该晶体的密度为
您最近一年使用:0次
【推荐1】碳是一种非常神奇的元素,它有着像C60、石墨和金刚石等这样结构和性质截然不同的单质,如下图所示,碳还是构成有机物的基本元素。请回答下列问题:

(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为___________ 。
(2)石墨属于___________ 晶体。
(3)金刚石中碳原子数目与C-C键数目之比为___________ 。
(4)青蒿素是从植物青蒿中提取的有机物,用于抗疟疾的药物。分子结构如下图所示,则青蒿素分子中含有___________ 个手性碳原子。


(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为
(2)石墨属于
(3)金刚石中碳原子数目与C-C键数目之比为
(4)青蒿素是从植物青蒿中提取的有机物,用于抗疟疾的药物。分子结构如下图所示,则青蒿素分子中含有

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有下列各组微粒或物质:
A、O2和O3
B、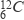 和
和 
C、CH3CH2CH2CH3和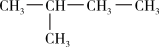
D、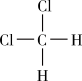 和
和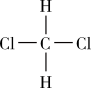
E、CH3CH2CH2CH3和
(1)________ 组两种微粒互为同位素;
(2)________ 组两种物质互为同素异形体;
(3)________ 组两种物质属于烃;
(4)________ 组两物质互为同分异构体;
(5)________ 组两物质是同一物质。
A、O2和O3
B、
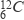 和
和 
C、CH3CH2CH2CH3和
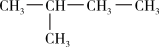
D、
 和
和
E、CH3CH2CH2CH3和

(1)
(2)
(3)
(4)
(5)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请将下列变化过程中破坏的微粒间作用力名称的编号填在横线上:
A共价键 B离子键 C金属键 D分子间作用力
(1)氢氧化钠熔化___ 。
(2)干冰升华___ 。
(3)二氧化硅熔化__ 。
(4)钠熔化__ 。
A共价键 B离子键 C金属键 D分子间作用力
(1)氢氧化钠熔化
(2)干冰升华
(3)二氧化硅熔化
(4)钠熔化
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】最常见、最熟知的原子晶体是周期表中_____ 族非金属元素的单质或化合物,如金刚石、二氧化硅和_________ 、_________ ,它们都有很高的熔点和硬度。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】共价晶体
| 概念 | 共价晶体是原子之间以 | |
| 构成粒子 | ||
| 微粒间的作用 | ||
| 物理性质 | 熔、沸点 | |
| 常见共价晶体 | 金刚石、单晶硅、碳化硅(SiC)、二氧化硅(SiO2)等。 | |
| 典型共价晶体 | 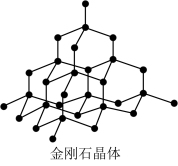 每个C原子形成4个C-C键,构成正四面体形成空间网状结构,其中n(C):n(C-C)=1:2 | 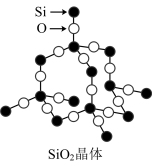 每个Si形成4个Si-O键,每个O形成2个O-Si键,向空间伸展形成网状结构,不存在单个分子,Si与O个数比为1:2,SiO2为化学式 |
您最近一年使用:0次



