(1)元素原子的价电子构型为3s23p3,它属于第________ 周期,是______ 族,元素符号是________ 。
(2)在HCl分子中,由H原子的一个____ 轨道与Cl原子的一个_____ 轨道形成一个____ 键;在Cl2分子中两个Cl原子以2个____ 轨道形成一个 ____ 键。
(2)在HCl分子中,由H原子的一个
更新时间:2020/11/24 13:53:09
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】根据原子核外电子排布规则,回答下列问题:
(1)写出基态S原子的简化核外电子排布式:_______ ;写出基态24Cr原子的价层电子排布式:_______ 。
(2)写出基态N原子的核外电子轨道表示式:_______ 。
(3)若将基态14Si的电子排布式写成1s22s22p63s23p14s1,则它违背了_______ 。
(4)已知Fe3+比Fe2+的稳定性更强,用电子排布解释其原因:_______ 。
(5)某原子的3d能级中有一个电子,其第四能层中的电子数为_______ 。
(1)写出基态S原子的简化核外电子排布式:
(2)写出基态N原子的核外电子轨道表示式:
(3)若将基态14Si的电子排布式写成1s22s22p63s23p14s1,则它违背了
(4)已知Fe3+比Fe2+的稳定性更强,用电子排布解释其原因:
(5)某原子的3d能级中有一个电子,其第四能层中的电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】A、B、C、D、E是五种短周期非金属元素(均为主族元素),且原子序数递增。A元素的某种原子,其核内没有中子;B的价层电子排布式为nsnnp(n+1);C元素的基态原子2p轨道上只有一对成对电子;C与D同主族。请回答下列问题:
(1)E在元素周期表中的位置为___________ 。
(2)第一电离能:B___________ C、D___________ E。
(3)A、E形成的分子与HF相比,其熔、沸点较低,原因是___________ 。
(4)A、B组成的10电子分子中原子B的杂化方式是___________ ,由B构成的单质分子中含___________ 个π键,与该单质分子互为等电子体的常见分子的分子式为___________ 。
(5)C、D形成的常见的三原子分子的VSEPR模型为___________ ,该分子属于___________ (填“极性”或“非极性”)分子,可以预测该分子在水中的溶解度较___________ (填“大”或“小”)。
(1)E在元素周期表中的位置为
(2)第一电离能:B
(3)A、E形成的分子与HF相比,其熔、沸点较低,原因是
(4)A、B组成的10电子分子中原子B的杂化方式是
(5)C、D形成的常见的三原子分子的VSEPR模型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】原子结构与元素周期表存在着内在联系。根据已学知识,请你回答下列问题:
(1)指出31号元素镓(Ga)在元素周期表中的位置:_______ 周期_______ 族。
(2)X原子在第二电子层上只有一个空轨道,则X是_______ ;其轨道表示式为_______ 。
(3)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:_______ 。
(4)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:_______ 。
(5)写出3p轨道上有2个未成对电子的元素符号:_______ 。
(6)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:_______ 。
(1)指出31号元素镓(Ga)在元素周期表中的位置:
(2)X原子在第二电子层上只有一个空轨道,则X是
(3)被誉为“21世纪的金属”的钛(Ti)元素原子的价电子排布式为:
(4)写出原子序数最小的Ⅷ族元素原子的核外电子排布式:
(5)写出3p轨道上有2个未成对电子的元素符号:
(6)日常生活中广泛应用的不锈钢,在其生产过程中添加了某种元素,该元素的价电子排布式为3d54s1,该元素的名称为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】 的资源化利用是解决温室效应的重要途径。科学家致力于
的资源化利用是解决温室效应的重要途径。科学家致力于 与
与 反应制
反应制 的研究。
的研究。
(1) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为________ ;干冰是很好的致冷剂,干冰升华时, 需要克服的作用力是
需要克服的作用力是________ 。
(2) 所含有的三种元素电负性从大到小的顺序为
所含有的三种元素电负性从大到小的顺序为________ (用元素符号表示)。
(3) 被氧化为
被氧化为 ,
, 继续被氧化可生成
继续被氧化可生成 。
。 分子的空间结构为
分子的空间结构为________ , 分子内
分子内 键与
键与 键个数之比为
键个数之比为________ 。
(4) 沸点远远高于乙烷,原因是
沸点远远高于乙烷,原因是________ 。
 的资源化利用是解决温室效应的重要途径。科学家致力于
的资源化利用是解决温室效应的重要途径。科学家致力于 与
与 反应制
反应制 的研究。
的研究。(1)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为 需要克服的作用力是
需要克服的作用力是(2)
 所含有的三种元素电负性从大到小的顺序为
所含有的三种元素电负性从大到小的顺序为(3)
 被氧化为
被氧化为 ,
, 继续被氧化可生成
继续被氧化可生成 。
。 分子的空间结构为
分子的空间结构为 分子内
分子内 键与
键与 键个数之比为
键个数之比为(4)
 沸点远远高于乙烷,原因是
沸点远远高于乙烷,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】甲、乙、丙三种有机物的结构如下:
甲: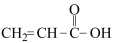 乙:COCl2(
乙:COCl2(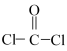 ) 丙:
) 丙:
(1)甲分子中有___________ 个 键,
键,___________ 个 键,
键,___________ (填“有”或“没有”)非极性键。
(2)乙分子中碳原子形成___________ 个 键,
键,___________ 个 键。
键。
(3)丙分子中 键与
键与 键的数目之比为
键的数目之比为___________ 。
甲:
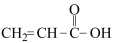 乙:COCl2(
乙:COCl2(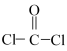 ) 丙:
) 丙:
(1)甲分子中有
 键,
键, 键,
键,(2)乙分子中碳原子形成
 键,
键, 键。
键。(3)丙分子中
 键与
键与 键的数目之比为
键的数目之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按照要求填空:
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
(2)① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。
①既有 键,又有
键,又有 键的是
键的是_______ (用序号作答);既含有极性键又含有非极性键的极性分子的电子式为_______ ;既含有极性键又含有非极性键的非极性分子中碳原子的杂化方式为________ ;苯环中存在的大 键可表示为
键可表示为________ 。
②属于离子化合物的物质的电子式为______ ; 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为_____ ; 中
中 键和
键和 键之比为
键之比为______ 。
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
| 序号 | 化学式 | 分子的极性 | 空间构型 | 中心原子的杂化方式 |
| ① |  | |||
| ② |  | |||
| ③ |  | - |
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。①既有
 键,又有
键,又有 键的是
键的是 键可表示为
键可表示为②属于离子化合物的物质的电子式为
 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为 中
中 键和
键和 键之比为
键之比为
您最近一年使用:0次



