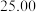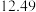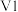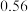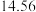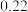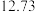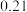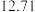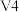名校
解题方法
1 . 回答下列问题
(1)在恒温条件下将一定量 和
和 的混合气体通入容积为
的混合气体通入容积为 的密闭容器中,
的密闭容器中, 和
和 两物质的浓度随时间的变化情况如下图所示。
两物质的浓度随时间的变化情况如下图所示。 、
、 表示):
表示):_______ 。
② 、
、 、
、 、
、 四个点中,表示化学反应处于平衡状态的点是
四个点中,表示化学反应处于平衡状态的点是_______ 。
(2)如下图所示是可逆反应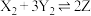 的反应速率
的反应速率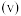 与时间
与时间 的关系曲线,下列叙述正确的是_______。
的关系曲线,下列叙述正确的是_______。
(3)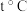 时,将
时,将 和
和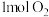 通入体积为
通入体积为 的恒温恒容密闭容器中,发生如下反应:
的恒温恒容密闭容器中,发生如下反应: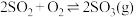 ,
, 时反应达到平衡,此时测得反应物
时反应达到平衡,此时测得反应物 还剩余
还剩余 。从反应开始到化学平衡,平衡时
。从反应开始到化学平衡,平衡时 的转化率为
的转化率为_______ 。
(1)在恒温条件下将一定量
 和
和 的混合气体通入容积为
的混合气体通入容积为 的密闭容器中,
的密闭容器中, 和
和 两物质的浓度随时间的变化情况如下图所示。
两物质的浓度随时间的变化情况如下图所示。
 、
、 表示):
表示):②
 、
、 、
、 、
、 四个点中,表示化学反应处于平衡状态的点是
四个点中,表示化学反应处于平衡状态的点是(2)如下图所示是可逆反应
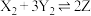 的反应速率
的反应速率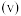 与时间
与时间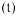 的关系曲线,下列叙述正确的是_______。
的关系曲线,下列叙述正确的是_______。
A. 时,只有正方向反应在进行 时,只有正方向反应在进行 |
B. 时,反应达到最大限度 时,反应达到最大限度 |
C. ,反应不再进行 ,反应不再进行 |
D. ,各物质的浓度不再发生变化 ,各物质的浓度不再发生变化 |
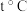 时,将
时,将 和
和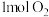 通入体积为
通入体积为 的恒温恒容密闭容器中,发生如下反应:
的恒温恒容密闭容器中,发生如下反应: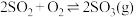 ,
, 时反应达到平衡,此时测得反应物
时反应达到平衡,此时测得反应物 还剩余
还剩余 。从反应开始到化学平衡,平衡时
。从反应开始到化学平衡,平衡时 的转化率为
的转化率为
您最近一年使用:0次
名校
解题方法
2 . 化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现象,下列说法正确的是_______。
(3)请利用反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池(正极材料用碳棒),该电池的负极材料是_______ ,发生的电极反应是_______ ,电解质溶液是_______ 。
(4)正极上出现的现象是_______ 。
(5)若导线上转移电子1 mol,则生成银_______  。
。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
A.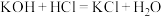 | B. |
C.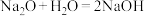 | D. |
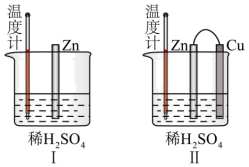
| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
(4)正极上出现的现象是
(5)若导线上转移电子1 mol,则生成银
 。
。
您最近一年使用:0次
名校
解题方法
3 . 归纳、演绎和模型等是化学学习的重要方法,回答下列问题。
元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。
(1)Y的化学式为__________ 。
(2)根据“价-类”二维图预测,下列能与 反应且
反应且 表现氧化性的物质是
表现氧化性的物质是__________ (填序号), 与其反应的化学方程式是
与其反应的化学方程式是__________ 。
a. b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(3)分析 的物质类别,写出它和少量NaOH溶液反应的离子方程式
的物质类别,写出它和少量NaOH溶液反应的离子方程式_______________ 。
(4)从 转化为X的化学方程式为
转化为X的化学方程式为________ ,由 制备X的过程中,一般用
制备X的过程中,一般用___________ 吸收 ,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。

(1)Y的化学式为
(2)根据“价-类”二维图预测,下列能与
 反应且
反应且 表现氧化性的物质是
表现氧化性的物质是 与其反应的化学方程式是
与其反应的化学方程式是a.
 b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(3)分析
 的物质类别,写出它和少量NaOH溶液反应的离子方程式
的物质类别,写出它和少量NaOH溶液反应的离子方程式(4)从
 转化为X的化学方程式为
转化为X的化学方程式为 制备X的过程中,一般用
制备X的过程中,一般用 ,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
您最近一年使用:0次
名校
4 . 有甲、乙两种物质:______________ ,反应Ⅱ的条件是_______________ ,反应Ⅲ的化学方程式为________________ (不需注明反应条件)。
(2)下列物质不能与乙反应的是___________ (填字母)。
a.金属钠 b.溴水 c.碳酸钠溶液 d.乙酸
(3)乙有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体结构简式___________ 。
a.苯环上的一氯代物有两种 b.遇 溶液显示紫色
溶液显示紫色

甲
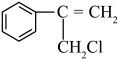
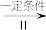 Y
Y 乙
乙
(2)下列物质不能与乙反应的是
a.金属钠 b.溴水 c.碳酸钠溶液 d.乙酸
(3)乙有多种同分异构体,任写其中一种能同时满足下列条件的同分异构体结构简式
a.苯环上的一氯代物有两种 b.遇
 溶液显示紫色
溶液显示紫色
您最近一年使用:0次
名校
解题方法
5 . 电化学原理在污染治理方面有着重要的作用。回答下列问题:
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:
已知:两电极为完全相同的惰性电极。______ 极。
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式______ 。
(3)电解过程中,混合溶液中的pH将______ (填“变大”、“变小”或“不变”),理由是______ 。
Ⅱ.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:______ 。
(5)酸性废水中的 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为______ 。
Ⅰ.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:
已知:两电极为完全相同的惰性电极。

(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(3)电解过程中,混合溶液中的pH将
Ⅱ.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:

(5)酸性废水中的
 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为
您最近一年使用:0次
名校
6 . 25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)HCOOH、 、HCN的酸性由强到弱的顺序为
、HCN的酸性由强到弱的顺序为______ 。
(2)向 溶液中加入足量HCN,反应的离子方程式为
溶液中加入足量HCN,反应的离子方程式为______ 。
(3)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.000mol/L的NaOH标准溶液滴定:
①用NaOH固体配制100mL,1.000mol/L的NaOH溶液,需要用到的仪器 除天平,药匙,烧杯,玻璃棒,胶头滴管,还需要______ 。实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;用标准NaOH溶液进行滴定,滴定过程中,眼睛应注视______ 。
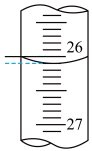
②连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为______ mL。
依据上表数据计算该HCOOH溶液的物质的量浓度为______ mol/L(计算结果保留四位有效数字)。
④下列操作中可能使所测HCOOH溶液的浓度数值偏低的是______ (填字母)。
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
(4)滴定法是一种常见的定量实验分析法,常见的滴定有酸碱中和滴定、氧化还原滴定、沉淀滴定等。
①如据反应 ,可以用碘水滴定
,可以用碘水滴定 溶液,可以选
溶液,可以选______ 作指示剂;
②用 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点,当溶液中的
反应生成砖红色沉淀指示滴定终点,当溶液中的 恰好沉淀完全(浓度为
恰好沉淀完全(浓度为 )时,溶液中的
)时,溶液中的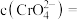
______  。(已知25℃时,
。(已知25℃时, 和AgCl的
和AgCl的 分别为
分别为 和
和 。)
。)
化学式 |
|
|
|
电离平衡常数 |
|
|
|
(1)HCOOH、
 、HCN的酸性由强到弱的顺序为
、HCN的酸性由强到弱的顺序为(2)向
 溶液中加入足量HCN,反应的离子方程式为
溶液中加入足量HCN,反应的离子方程式为(3)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.000mol/L的NaOH标准溶液滴定:
①用NaOH固体配制100mL,1.000mol/L的NaOH溶液,需要用到的
②连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为
实验序号 | 待测 |
| ||
滴定前刻度 | 滴定后刻度 | 溶液的体积 | ||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
④下列操作中可能使所测HCOOH溶液的浓度数值偏低的是
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
(4)滴定法是一种常见的定量实验分析法,常见的滴定有酸碱中和滴定、氧化还原滴定、沉淀滴定等。
①如据反应
 ,可以用碘水滴定
,可以用碘水滴定 溶液,可以选
溶液,可以选②用
 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点,当溶液中的
反应生成砖红色沉淀指示滴定终点,当溶液中的 恰好沉淀完全(浓度为
恰好沉淀完全(浓度为 )时,溶液中的
)时,溶液中的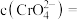
 。(已知25℃时,
。(已知25℃时, 和AgCl的
和AgCl的 分别为
分别为 和
和 。)
。)
您最近一年使用:0次
7 . 自然界的氮循环如图所示,回答下列问题。_____ 。
(2)如图为N2转化为HNO3的流程。
N2 NO
NO NO2
NO2 HNO3
HNO3
①上述物质颜色为红棕色的是_____ (用化学式表示)
②NO2转化为HNO3的反应中,NO2体现_____ 性。
(3)N2也可以转化为NH3,写出工业合成氨的化学方程式_____ 。
(4)稀硝酸与铜反应的还原产物为_____ 。
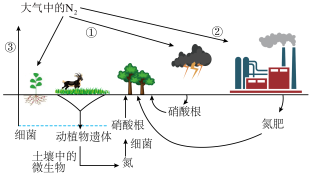
(2)如图为N2转化为HNO3的流程。
N2
 NO
NO NO2
NO2 HNO3
HNO3①上述物质颜色为红棕色的是
②NO2转化为HNO3的反应中,NO2体现
(3)N2也可以转化为NH3,写出工业合成氨的化学方程式
(4)稀硝酸与铜反应的还原产物为
您最近一年使用:0次
名校
8 . A~D是四种烃分子的球棍模型(如图)___________ 。
(2)能使酸性高锰酸钾溶液褪色的物质是___________ (填序号)。
(3)B的结构简式___________ 。
(4)从下列各组物质中,找出合适的序号填在对应的空格内:
①甲烷和丙烷 ②235U和238U ③金刚石和石墨 ④H和D
互为同位素的是___________ (填序号,下同);互为同分异构体的是___________ ;互为同系物的是___________ ;互为同素异形体的是___________ 。
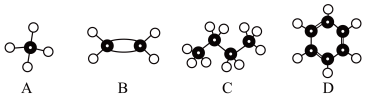
(2)能使酸性高锰酸钾溶液褪色的物质是
(3)B的结构简式
(4)从下列各组物质中,找出合适的序号填在对应的空格内:
①甲烷和丙烷 ②235U和238U ③金刚石和石墨 ④H和D
⑤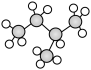 和
和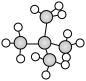 ⑥
⑥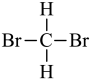 和
和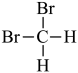 ⑦正丁烷和异丁烷
⑦正丁烷和异丁烷
(5)⑧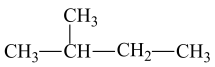 和
和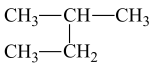 ⑨
⑨ 和
和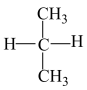
互为同位素的是
您最近一年使用:0次
名校
9 . 有机化合物A是一种重要的化工原料,在一定条件下可以发生如下反应:___________ ,分子中最多有___________ 个原子共平面。
(2)A→B的反应方程式为___________ ,该反应的反应类型为___________ 。
(3)A→D的反应方程式为___________ ,该反应的反应类型为___________ 。
(4)1mol A与足量的氢气反应最多消耗___________ molH2。
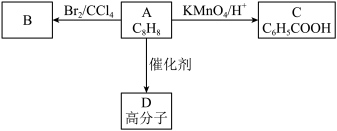

(2)A→B的反应方程式为
(3)A→D的反应方程式为
(4)1mol A与足量的氢气反应最多消耗
您最近一年使用:0次
名校
10 . 按要求回答下列问题:___________ 。
(1) 分子中的含氧官能团的名称为
分子中的含氧官能团的名称为 改写为结构简式
改写为结构简式
① 的名称是
的名称是
② 的名称是
的名称是
③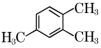 的名称是
的名称是
您最近一年使用:0次

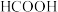

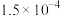
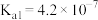
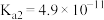

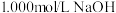 的体积
的体积