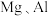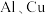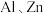名校
解题方法
1 . 有机化合物R为无色粘性液体,易溶于水,可由葡萄糖发酵制得。
(1)化合物 的质谱图如图-1所示(图中最右侧的峰表示
的质谱图如图-1所示(图中最右侧的峰表示 所形成的分子离子峰,其质荷比的数值就是
所形成的分子离子峰,其质荷比的数值就是 的相对分子质量)
的相对分子质量)
将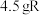 在足量
在足量 中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重
中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重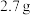 和
和 ,则R的分子式为
,则R的分子式为________ 。
(2)对 进行红外光谱分析,含有官能团
进行红外光谱分析,含有官能团 和
和 ,R的核磁共振氢谱图如图2所示,则R中含有
,R的核磁共振氢谱图如图2所示,则R中含有________ 种氢原子,R的结构简式为________ 。
(3)R在催化剂、加热的条件下发生聚合反应,制得可降解塑料PLA,写出该反应的化学方程式________ 。
(4)某烃的结构如图3所示,若每两个碳原子之间均插入一个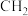 原子团,可以形成金刚烷的结构,金刚烷的分子式为
原子团,可以形成金刚烷的结构,金刚烷的分子式为________ ,其一氯代物有________ 种。
(5)聚碳酸酯(结构如图4)的透光率良好,它可制作车、船、飞机的挡风玻璃,以及眼镜片、光盘、唱片等。它可用绿色化学原料碳酸二甲酯(结构如图5)与另一种原料M在一定条件下反应制得,同时生成甲醇。M的结构简式为________ 。
(1)化合物
 的质谱图如图-1所示(图中最右侧的峰表示
的质谱图如图-1所示(图中最右侧的峰表示 所形成的分子离子峰,其质荷比的数值就是
所形成的分子离子峰,其质荷比的数值就是 的相对分子质量)
的相对分子质量)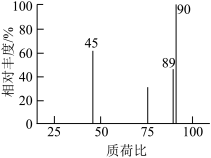
将
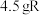 在足量
在足量 中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重
中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现二者分别增重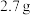 和
和 ,则R的分子式为
,则R的分子式为(2)对
 进行红外光谱分析,含有官能团
进行红外光谱分析,含有官能团 和
和 ,R的核磁共振氢谱图如图2所示,则R中含有
,R的核磁共振氢谱图如图2所示,则R中含有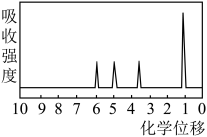
(3)R在催化剂、加热的条件下发生聚合反应,制得可降解塑料PLA,写出该反应的化学方程式
(4)某烃的结构如图3所示,若每两个碳原子之间均插入一个
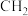 原子团,可以形成金刚烷的结构,金刚烷的分子式为
原子团,可以形成金刚烷的结构,金刚烷的分子式为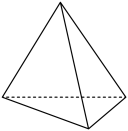
(5)聚碳酸酯(结构如图4)的透光率良好,它可制作车、船、飞机的挡风玻璃,以及眼镜片、光盘、唱片等。它可用绿色化学原料碳酸二甲酯(结构如图5)与另一种原料M在一定条件下反应制得,同时生成甲醇。M的结构简式为

您最近一年使用:0次
名校
解题方法
2 . 根据原电池原理,回答下列问题:
(1)铜铁原电池的装置如图所示:___________ (填“正极”或“负极”),溶液中的 向
向___________ (填“铁”或“铜”)电极方向移动。
②负极的电极反应式为___________ 。
③若反应过程中有 电子的转移,则生成标准状况下氢气的体积为
电子的转移,则生成标准状况下氢气的体积为___________  。
。
(2)某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
已知:实验均为常温下完成;电流计指针偏转方向为正极方向。
①实验3中, 为
为___________ 极,电极反应式为___________ 。
②实验4中, 为
为___________ 极,电池总反应的离子方程式是___________ 。
③根据实验结果总结出影响铝在电池中做正极或负极的因素有___________ 。
(1)铜铁原电池的装置如图所示:

 向
向②负极的电极反应式为
③若反应过程中有
 电子的转移,则生成标准状况下氢气的体积为
电子的转移,则生成标准状况下氢气的体积为 。
。(2)某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | 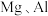 | 稀盐酸 | 偏向 |
| 2 | 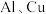 | 稀盐酸 | 偏向 |
| 3 | 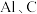 (石墨) (石墨) | 稀盐酸 | 偏向石墨 |
| 4 | 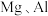 |  溶液 溶液 | 偏向 |
| 5 | 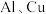 | 浓硝酸 | 偏向 |
①实验3中,
 为
为②实验4中,
 为
为③根据实验结果总结出影响铝在电池中做正极或负极的因素有
您最近一年使用:0次
解题方法
3 . 根据要求,回答下列问题:
(1)为了测定某有机物A的结构,进行如下实验:
a.将2.3 g该有机物完全燃烧,生成0.1mol 和27g水;
和27g水;
b.用质谱仪测定其相对分子质量,得到如图所示的质谱图。___________ 。
②有机物A的实验式是___________ 。
(2)有机物的结构可用“键线式”简化表示,例如: 可简写为
可简写为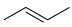 。有机物X的键线式为
。有机物X的键线式为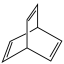 。
。
①有机物Y是X的同分异构体,则Y属于芳香烃的键线式为___________ 。
②X与足量的 在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有
在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有___________ 种,写出其中任意一种的键线式:___________ 。
(1)为了测定某有机物A的结构,进行如下实验:
a.将2.3 g该有机物完全燃烧,生成0.1mol
 和27g水;
和27g水;b.用质谱仪测定其相对分子质量,得到如图所示的质谱图。

②有机物A的实验式是
(2)有机物的结构可用“键线式”简化表示,例如:
 可简写为
可简写为 。有机物X的键线式为
。有机物X的键线式为 。
。①有机物Y是X的同分异构体,则Y属于芳香烃的键线式为
②X与足量的
 在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有
在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有③由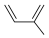 以及必要的无机试剂可合成
以及必要的无机试剂可合成 ,写出第一步合成反应的化学方程式:
,写出第一步合成反应的化学方程式:
④双烯合成反应(即Diels-Alder反应)是由二烯烃与单烯烃或炔烃合成六元环状化合物的重要反应,例如,1,3-丁二烯与乙烯的作用可表示为: ,则由1-丁烯和2-乙基-1,3-丁二烯发生双烯合成反应的产物为
,则由1-丁烯和2-乙基-1,3-丁二烯发生双烯合成反应的产物为
您最近一年使用:0次
解题方法
4 . 有机物的世界很丰富,种类和数目非常庞大,认识简单的有机物是我们学习有机化学的开始。回答下列问题:
(1)有下列几组物质:① 与
与 ;②乙醇和二甲醚(CH3OCH3);③乙二醇(
;②乙醇和二甲醚(CH3OCH3);③乙二醇( )与丙三醇(
)与丙三醇( );④
);④ 和
和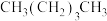 ;⑤CH2=CHCH3和CH2=CH2。
;⑤CH2=CHCH3和CH2=CH2。
①第②组物质中含有的官能团名称为___________ ;上述物质中不属于同分异构体的有___________ (填序号);
②CH3(CH2)3CH3的一氯取代物有___________ 种。
(2)乙酸与乙醇在浓硫酸、加热条件下发生酯化反应的化学方程式为___________ ,根据乙酸与乙醇发生酯化反应的原理,说明乙醇分子结构中极性较大的共价键是___________ 键。
(3)邻二氯苯和间二氯苯属于有机化合物构造异构中的___________ 异构(填“碳架”“位置”或“官能团”)。
(4)类比甲烷,乙烷与Cl2在光照条件下也能发生取代反应,写出第一步反应的化学方程式:___________ ,乙烷与足量的Cl2反应生成___________ 种产物。
(1)有下列几组物质:①
 与
与 ;②乙醇和二甲醚(CH3OCH3);③乙二醇(
;②乙醇和二甲醚(CH3OCH3);③乙二醇( )与丙三醇(
)与丙三醇( );④
);④ 和
和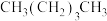 ;⑤CH2=CHCH3和CH2=CH2。
;⑤CH2=CHCH3和CH2=CH2。①第②组物质中含有的官能团名称为
②CH3(CH2)3CH3的一氯取代物有
(2)乙酸与乙醇在浓硫酸、加热条件下发生酯化反应的化学方程式为
(3)邻二氯苯和间二氯苯属于有机化合物构造异构中的
(4)类比甲烷,乙烷与Cl2在光照条件下也能发生取代反应,写出第一步反应的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 碳在地壳中的含量很低,但是含有碳元素的有机物却分布极广。
(1)观察下面几种烷烃的球棍模型:______________ (填字母,下同),与C互为同分异构体的是______________ .
(2)写出下列链状烷烃的分子式:
①含有30个氢原子的烷烃的分子式为______________ .
②假如某烷烃的相对分子质量为142,则该烷烃的分子式为______________ .
(3)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室模拟上述过程,其设计的模拟装置如图.
①装置B有三种功能:a.控制气流速度;b.均匀混合气体;c.______________ .
②设 ,若理论上欲获得最多的氯化氢,则x值应
,若理论上欲获得最多的氯化氢,则x值应______________ .
③装置D的石棉中均匀混有 粉末,其作用是
粉末,其作用是__________________________________________ .
④装置E的作用是______________ (填序号).
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
(1)观察下面几种烷烃的球棍模型:
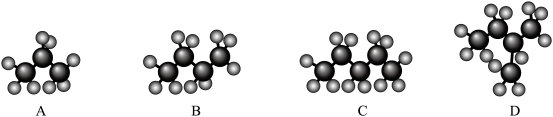
(2)写出下列链状烷烃的分子式:
①含有30个氢原子的烷烃的分子式为
②假如某烷烃的相对分子质量为142,则该烷烃的分子式为
(3)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实.某化学兴趣小组在实验室模拟上述过程,其设计的模拟装置如图.
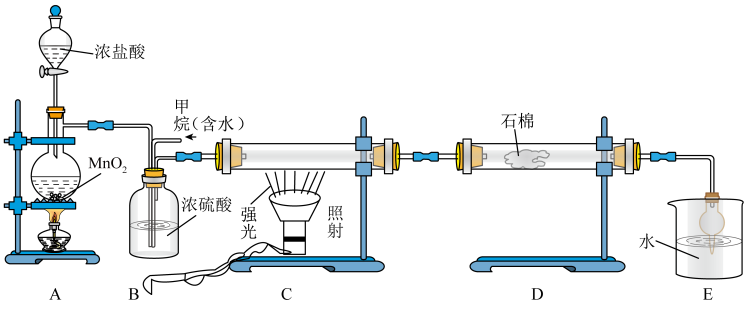
①装置B有三种功能:a.控制气流速度;b.均匀混合气体;c.
②设
 ,若理论上欲获得最多的氯化氢,则x值应
,若理论上欲获得最多的氯化氢,则x值应③装置D的石棉中均匀混有
 粉末,其作用是
粉末,其作用是④装置E的作用是
A.收集气体 B.吸收氯气 C.防止倒吸 D.吸收氯化氢
您最近一年使用:0次
名校
6 . 我国科学家将聚酰亚胺(组成元素为H、C、N、O等)介电聚合物与高绝缘纳米氧化镁(MgO)填料混合,成功制得聚酰亚胺/纳米氧化镁复合材料。该复合材料特点为具有高击穿强度、宽温度范围和低介电损耗。结合所学知识,回答下列问题。
(1)基态Mg原子的电子排布式为_________ 。
(2)C、N、O第一电离能由大到小的顺序为_________ ;C、N、O电负性由大到小的顺序为_________ ,理由是________________ 。
(3) 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为_________ ; 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是__________ ; 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是________ 。
(1)基态Mg原子的电子排布式为
(2)C、N、O第一电离能由大到小的顺序为
(3)
 三种分子的空间结构和相应的键角如图1所示。
三种分子的空间结构和相应的键角如图1所示。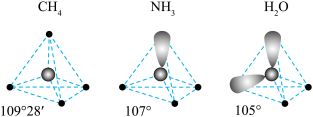
 中O的未成对电子所在原子轨道的形状为
中O的未成对电子所在原子轨道的形状为 的沸点比
的沸点比 的高,其主要原因是
的高,其主要原因是 的键角大于
的键角大于 的键角,其原因是
的键角,其原因是
您最近一年使用:0次
名校
7 . 回答下列问题
(1)利用 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
________ (填“大于”“小于”或“等于”) 。
。
②碳化硅晶体中每个Si原子周围距离最近的C原子数目为________ 。
③碳化硅的晶胞参数为a pm,晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
_______ (用含a和ρ的计算式表示)
④碳化硅的硬度_________ (填“大于”“小于”或“等于”)氮化硅的硬度,原因是_____________ 。
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。______________ 晶体。
②氮化碳的化学式为______________ 。
(3)三氧化铼 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为________ ,已知该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为________ cm。
(1)利用
 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。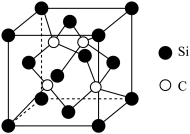

 。
。②碳化硅晶体中每个Si原子周围距离最近的C原子数目为
③碳化硅的晶胞参数为a pm,晶胞密度为
 ,则阿伏加德罗常数
,则阿伏加德罗常数
④碳化硅的硬度
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。
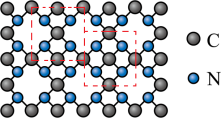
②氮化碳的化学式为
(3)三氧化铼
 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为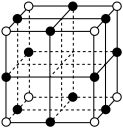
您最近一年使用:0次
2024-06-17更新
|
91次组卷
|
2卷引用:甘肃省酒泉市四校联考2023-2024学年高二下学期5月期中考试化学试题
名校
解题方法
8 . 某化学兴趣小组的同学为了探究铝电极在电池中的作用,设计并进行了以下实验,实验结果记录如下:
根据表中的实验现象回答下列问题.
(1)实验1和实验2中 所作的电极
所作的电极______________ (填“相同”或“不相同”);
(2)对实验3完成下列填空.
①铝为_________ 极,电极反应式为__________________ ;
②石墨为__________ 极,电极反应式为_______________________ ;
③电池总反应的化学方程式为__________ ;
(3)实验4中铝作_________ 极,理由是__________ ;铝电极的电极反应式为__________ ;
(4)解释实验5中电流表指针偏向铝的原因:__________ ;
(5)根据实验结果总结影响铝在原电池中作正极或负极的因素:__________ 。
编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
1 |
| 稀盐酸 | 偏向 |
2 |
| 稀盐酸 | 偏向 |
3 |
| 稀盐酸 | 偏向石墨 |
4 |
|
| 偏向 |
5 |
| 浓硝酸 | 偏向 |
(1)实验1和实验2中
 所作的电极
所作的电极(2)对实验3完成下列填空.
①铝为
②石墨为
③电池总反应的化学方程式为
(3)实验4中铝作
(4)解释实验5中电流表指针偏向铝的原因:
(5)根据实验结果总结影响铝在原电池中作正极或负极的因素:
您最近一年使用:0次
名校
9 . 非金属单质A经下图所示的过程可转化为含氧酸D,已知D为强酸。请回答下列问题.

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体;
①D的化学式为______________ ;
②在工业生产中,B气体大量排放,被雨水吸收后形成的______________ 会污染环境;
③98.3%的D溶液是常见的气体干燥剂,但它不能干燥 和
和 ,原因是
,原因是______________ ;
(2)若A在常温下为气体,C是红棕色的气体;
①A、C的化学式分别为_________ 、___________ ;
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为________ ,该反应_______ (填“属于”或“不属于”)氧化还原反应;
③工业上利用氨制备D,写出氨被催化氧化生成B气体的化学方程式:____________ 。

(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体;
①D的化学式为
②在工业生产中,B气体大量排放,被雨水吸收后形成的
③98.3%的D溶液是常见的气体干燥剂,但它不能干燥
 和
和 ,原因是
,原因是(2)若A在常温下为气体,C是红棕色的气体;
①A、C的化学式分别为
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为
③工业上利用氨制备D,写出氨被催化氧化生成B气体的化学方程式:
您最近一年使用:0次
10 . 回答下问题:
(1)Sm的价层电子排布式为 4f66s2 ,Sm3+价层电子排布式为___________ 。
(2)依据第二周期元素第一电离能的变化规律,参照如图元素 B 、F 的位置,用小黑点标 出 C 、N 、O 三种元素的相对位置___________ 。___________ 。
(4)H2S 和 H2Se 的参数对比见下表,其中 H2S 的键角大于 H2Se 的键角的原因可能为___________
(1)Sm的价层电子排布式为 4f66s2 ,Sm3+价层电子排布式为
(2)依据第二周期元素第一电离能的变化规律,参照如图元素 B 、F 的位置,用小黑点标 出 C 、N 、O 三种元素的相对位置

(4)H2S 和 H2Se 的参数对比见下表,其中 H2S 的键角大于 H2Se 的键角的原因可能为
| 化学式 | 键长/nm | 键角 | 沸点/℃ |
| H2S | 1.34 | 92.3° | -60.75 |
| H2Se | 1.47 | 91.0° | -41.50 |
您最近一年使用:0次