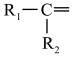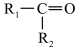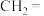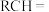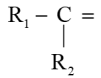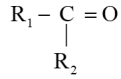名校
解题方法
1 . 能源是现代文明的原动力,化学电池在生产生活中有着广泛的应用。
(1)为了探究化学反应中的能量变化,某同学设计了如图所示两个实验。有关实验现象,下列说法正确的是___________(填标号)。
(2)图II中外电路中的电子是从___________ (填“Zn”或“Cu”)电极经导线流向___________ 电极。若反应过程中有0.2 mol电子发生转移,则生成的氢气在标准状况下的体积为___________ 。若电池的总反应为2Fe3++Cu=2Fe2++Cu2+,则负极材料是___________ (填化学式)。
(3)某蓄电池在充电和放电时发生的反应为:NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。则该电池放电时发生还原反应的物质是
Fe(OH)2+Ni(OH)2。则该电池放电时发生还原反应的物质是___________ (填标号);放电时负极的电极反应式为___________ 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(1)为了探究化学反应中的能量变化,某同学设计了如图所示两个实验。有关实验现象,下列说法正确的是___________(填标号)。
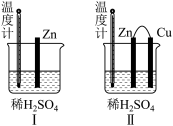
| A.图I和图II的气泡均产生于锌棒表面 |
| B.图II中产生气体的速率比图I快 |
| C.图I中温度计的示数高于图II的示数 |
| D.图I和图II中温度计的示数相等,且均高于室温 |
(2)图II中外电路中的电子是从
(3)某蓄电池在充电和放电时发生的反应为:NiO2+Fe+2H2O
 Fe(OH)2+Ni(OH)2。则该电池放电时发生还原反应的物质是
Fe(OH)2+Ni(OH)2。则该电池放电时发生还原反应的物质是A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
您最近一年使用:0次
名校
解题方法
2 . 回答下列问题:
I.下表中的数据是破坏1 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题
(1)下列氢化物中最稳定的是___________ (填标号)。
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2 mol HI___________ (填“吸收”或“放出”)的热量为___________ kJ。
(3)某化学反应过程能量变化如图所示,该化学反应可能是___________(填标号)
II.某温度时,在一个2 L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据回答下列问题:___________ ;
(5)从开始至2min末,A的平均反应速率为___________ ;
(6)2min时反应达到平衡,容器内混合气体的平均相对分子质量比起始时___________ (填“大”,“小”或“相等”,下同),混合气体密度比起始时___________ 。
(7)在某一时刻采取下列措施能使该反应速率减小的是___________(填标号)。
I.下表中的数据是破坏1
 物质中的化学键所消耗的能量,回答下列问题
物质中的化学键所消耗的能量,回答下列问题| 物质 |  |  |  |  |  |  |  |
| 键能/kJ | 243 | 193 | 151 | 432 | 366 | 298 | 436 |
(1)下列氢化物中最稳定的是
A.HCl B.HBr C.HI
(2)按照反应I2+H2=2HI,生成2 mol HI
(3)某化学反应过程能量变化如图所示,该化学反应可能是___________(填标号)

| A.NaOH+HCl=NaCl+H2O |
| B.Fe+H2SO4=FeSO4+H2↑ |
| C.2Na2O2+2H2O=4NaOH+O2↑ |
| D.Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O |
II.某温度时,在一个2 L的密闭容器中, A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据回答下列问题:
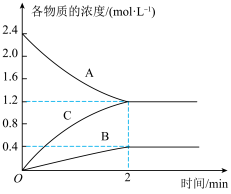
(5)从开始至2min末,A的平均反应速率为
(6)2min时反应达到平衡,容器内混合气体的平均相对分子质量比起始时
(7)在某一时刻采取下列措施能使该反应速率减小的是___________(填标号)。
| A.加催化剂 | B.降低温度 |
| C.容积不变,充入A | D.容积不变,从容器中分离出A |
您最近一年使用:0次
名校
3 . 分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液均为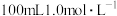 的稀硫酸(假设反应过程中溶液体积不变),乙中
的稀硫酸(假设反应过程中溶液体积不变),乙中 为电流表。
为电流表。
(1)反应过程中能量转化的主要形式:甲为___________ ;乙为___________ 。
(2)以下叙述中,正确的是___________(填字母)。
(3)如图所示为两装置中产生氢气体积随时间的变化图像,其中表示甲的曲线是___________ (填“ ”或“
”或“ ”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是
”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是___________ (填字母),若要加快甲中反应的速率,可以采取的方法是___________ (任写两种)。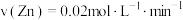 B.
B.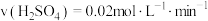
C. D.
D.
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,则铜电极为___________ (填“正极”或“负极”,下同), 离子移向
离子移向___________ , 电极的电极反应式为
电极的电极反应式为___________ ,当外电路中转移 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为___________ g(保留三位小数)。
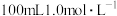 的稀硫酸(假设反应过程中溶液体积不变),乙中
的稀硫酸(假设反应过程中溶液体积不变),乙中 为电流表。
为电流表。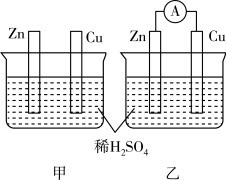
(1)反应过程中能量转化的主要形式:甲为
(2)以下叙述中,正确的是___________(填字母)。
| A.甲中锌片是负极,乙中铜片是正极 | B.两烧杯中铜片表面均有气泡产生 |
| C.两烧杯中溶液pH均增大 | D.两烧杯中发生的反应相同 |
(3)如图所示为两装置中产生氢气体积随时间的变化图像,其中表示甲的曲线是
 ”或“
”或“ ”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是
”),若经过5min甲中产生气体体积为224mL(标准状况),下列能够正确表示该反应速率的是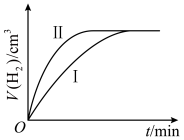
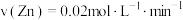 B.
B.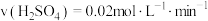
C.
 D.
D.
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,则铜电极为
 离子移向
离子移向 电极的电极反应式为
电极的电极反应式为 电子时,消耗负极材料的质量为
电子时,消耗负极材料的质量为
您最近一年使用:0次
名校
4 . 合理开发和利用自然资源是人类赖以生存的基础。回答下列问题:
Ⅰ.金属矿物的开发利用。
(1)金属的冶炼有多种方法,工业炼铁可采用___________ (填“电解法”“热还原法”或“热分解法”)。
(2)已知MgO、 的熔、沸点数据如表所示:
的熔、沸点数据如表所示:
通过电解法冶炼镁时应选用熔融的___________ (填化学式),不选用另一种物质的原因为___________ 。
Ⅱ.海水资源的开发利用。
(3)任写一种工业上海水淡化的方法:___________ 。
(4)NaCl是海水的主要溶质,可用于制备很多重要的化工原料,制备物质___________ (填选项字母)的主要过程中不涉及氧化还原反应。
A.纯碱 B.氯气 C.钠
Ⅲ.化石能源的综合利用。
(5)煤、石油和天然气(主要成分为甲烷)是重要的化石能源,其中石油分馏后的产物进行裂解后可得到 、
、 、
、 、
、 等重要的化工原料。
等重要的化工原料。
①煤的干馏和石油的分馏均是从化石能源中获得重要化工原料的手段,其中不涉及化学变化的是___________ 。
②上述四种有机物中与甲烷互为同系物的是___________ (填化学式)。
③ 燃料碱性电池工作原理如图所示。乙电极为电源的
燃料碱性电池工作原理如图所示。乙电极为电源的___________ (填“正极”或“负极”),甲电极上的电极反应式为___________ ;电池工作时,当外电路中通过0.3mol电子时,理论上消耗 在标准状况下的体积为
在标准状况下的体积为___________ L。
Ⅰ.金属矿物的开发利用。
(1)金属的冶炼有多种方法,工业炼铁可采用
(2)已知MgO、
 的熔、沸点数据如表所示:
的熔、沸点数据如表所示:| 物质 | MgO |  |
| 熔点/℃ | 2852 | 714 |
| 沸点/℃ | 3600 | 1412 |
Ⅱ.海水资源的开发利用。
(3)任写一种工业上海水淡化的方法:
(4)NaCl是海水的主要溶质,可用于制备很多重要的化工原料,制备物质
A.纯碱 B.氯气 C.钠
Ⅲ.化石能源的综合利用。
(5)煤、石油和天然气(主要成分为甲烷)是重要的化石能源,其中石油分馏后的产物进行裂解后可得到
 、
、 、
、 、
、 等重要的化工原料。
等重要的化工原料。①煤的干馏和石油的分馏均是从化石能源中获得重要化工原料的手段,其中不涉及化学变化的是
②上述四种有机物中与甲烷互为同系物的是
③
 燃料碱性电池工作原理如图所示。乙电极为电源的
燃料碱性电池工作原理如图所示。乙电极为电源的 在标准状况下的体积为
在标准状况下的体积为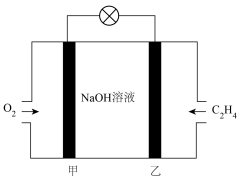
您最近一年使用:0次
名校
5 . 回答下列问题
(1)利用 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
________ (填“大于”“小于”或“等于”) 。
。
②碳化硅晶体中每个Si原子周围距离最近的C原子数目为________ 。
③碳化硅的晶胞参数为a pm,晶胞密度为 ,则阿伏加德罗常数
,则阿伏加德罗常数
_______ (用含a和ρ的计算式表示)
④碳化硅的硬度_________ (填“大于”“小于”或“等于”)氮化硅的硬度,原因是_____________ 。
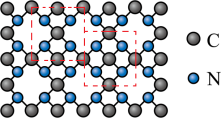
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。______________ 晶体。
②氮化碳的化学式为______________ 。
(3)三氧化铼 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为________ ,已知该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为________ cm。
(1)利用
 与
与 反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。
反应可制得碳化硅晶体,其晶胞结构如图,硅原子位于立方体的顶点和面心,碳原子位于立方体的内部。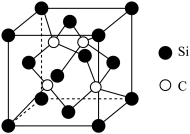

 。
。②碳化硅晶体中每个Si原子周围距离最近的C原子数目为
③碳化硅的晶胞参数为a pm,晶胞密度为
 ,则阿伏加德罗常数
,则阿伏加德罗常数
④碳化硅的硬度
(2)氮化碳比氮化硅的硬度更大,其中β—氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如图,图中线框内表示晶胞结构。
②氮化碳的化学式为
(3)三氧化铼
 晶胞如图所示,其中O原子的配位数为
晶胞如图所示,其中O原子的配位数为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则Re与O的最近距离为
,则Re与O的最近距离为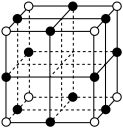
您最近一年使用:0次
7日内更新
|
71次组卷
|
2卷引用:河南省百师联盟2023-2024学年高二下学期五月大联考化学试卷
名校
解题方法
6 . 请回答下列问题:
(1)脱落酸是一种植物激素,结构简式为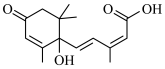 ,其中含有的官能团有
,其中含有的官能团有___________ 种。
(2)烷烃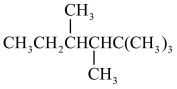 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为___________ ,其一氯代物有___________ 种。若该烃由一种炔烃加氢而成,则该炔烃的结构简式为___________ 。
(3)以烯烃A( )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示:
ⅱ.共轭二烯烃可发生1,2-加成和1,4-加成。
①物质A的系统命名为___________ ;B的同分异构体中,与其碳骨架相同的共有___________ 种。
②物质C与氢气反应,得到的产物最多可能有___________ 种。
③C与适量酸性KMnO4溶液作用后得到的有机氧化产物的结构简式为___________ 。
(1)脱落酸是一种植物激素,结构简式为
 ,其中含有的官能团有
,其中含有的官能团有(2)烷烃
 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为(3)以烯烃A(
 )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示: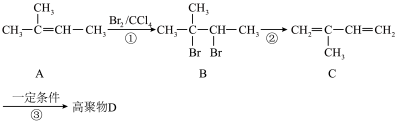
| 烯烃被氧化的部位 | 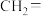 | 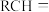 |
|
| 对应的氧化产物 |  | RCOOH |
|
①物质A的系统命名为
②物质C与氢气反应,得到的产物最多可能有
③C与适量酸性KMnO4溶液作用后得到的有机氧化产物的结构简式为
您最近一年使用:0次
名校
7 . 请回答下列问题:
(1)脱落酸是一种植物激素,结构简式为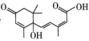 ,其中含有的官能团有
,其中含有的官能团有______ 种。
(2)烷烃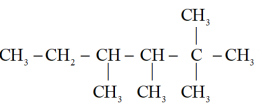 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为______ ,其一氯代物有______ 种。若该烃由一种炔烃加氢而成,则该炔烃的结构简式为______ 。
(3)以烯烃A(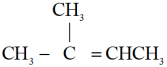 )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示:
已知:ⅰ.烯烃中的不饱和键在酸性高锰酸钾溶液作用下对应的产物如下表所示。
ⅱ.共轭二烯烃可发生1,2-加成和1,4-加成。
①物质A的系统命名为______ ;B的同分异构体中,与其碳骨架相同的共有______ 种。
②物质C与氢气反应,得到的产物最多可能有______ 种;C→D通过1,4-加成的方式聚合,该反应的化学方程式为______ 。
③C与适量酸性 溶液作用后得到的有机氧化产物的结构简式为
溶液作用后得到的有机氧化产物的结构简式为______ 。
(1)脱落酸是一种植物激素,结构简式为
 ,其中含有的官能团有
,其中含有的官能团有(2)烷烃
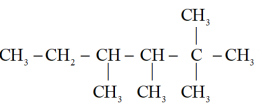 可用于制备裂解汽油,该物质用系统命名法命名为
可用于制备裂解汽油,该物质用系统命名法命名为(3)以烯烃A(
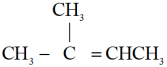 )为原料合成高聚物D的路线如图所示:
)为原料合成高聚物D的路线如图所示:

已知:ⅰ.烯烃中的不饱和键在酸性高锰酸钾溶液作用下对应的产物如下表所示。
烯烃被氧化的部位 |
|
|
|
对应的氧化产物 |
| RCOOH |
|
①物质A的系统命名为
②物质C与氢气反应,得到的产物最多可能有
③C与适量酸性
 溶液作用后得到的有机氧化产物的结构简式为
溶液作用后得到的有机氧化产物的结构简式为
您最近一年使用:0次
名校
解题方法
8 . 高氯酸三碳酰肼合镍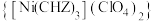 是一种新型的起爆药。设
是一种新型的起爆药。设 为阿伏加德罗常数的值。回答下列问题:
为阿伏加德罗常数的值。回答下列问题:
(1)基态 的电子排布式为
的电子排布式为___________ 。
(2)基态碳原子核外电子有___________ 种不同运动状态。
(3) 的中心原子的价层电子对数为
的中心原子的价层电子对数为________ , 的VSEPR模型是
的VSEPR模型是_________ 。
(4)上述化学式中的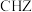 为碳酰肼,其结构为
为碳酰肼,其结构为 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。
①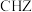 中氮原子的杂化轨道类型为
中氮原子的杂化轨道类型为___________ 。
②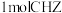 中含有的
中含有的 键数目为
键数目为___________  (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
③键角:
___________ (填“>”“<”或“=”) 。
。
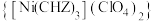 是一种新型的起爆药。设
是一种新型的起爆药。设 为阿伏加德罗常数的值。回答下列问题:
为阿伏加德罗常数的值。回答下列问题:(1)基态
 的电子排布式为
的电子排布式为(2)基态碳原子核外电子有
(3)
 的中心原子的价层电子对数为
的中心原子的价层电子对数为 的VSEPR模型是
的VSEPR模型是(4)上述化学式中的
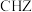 为碳酰肼,其结构为
为碳酰肼,其结构为 ,是一种新型的环保锅炉水除氧剂。
,是一种新型的环保锅炉水除氧剂。①
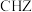 中氮原子的杂化轨道类型为
中氮原子的杂化轨道类型为②
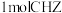 中含有的
中含有的 键数目为
键数目为 (
( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。③键角:

 。
。
您最近一年使用:0次
名校
解题方法
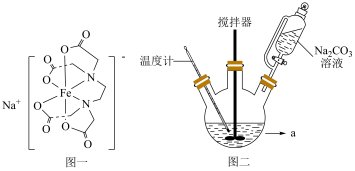
9 . 配合物乙二胺四乙酸铁钠(结构如图一所示,以下简写为NaFeY)可以添加到酱油中作为铁强化剂,制备乙二胺四乙酸铁钠晶体步骤如下:
①称取一定质量的FeCl3⋅6H2O于烧杯中溶解,加入适量浓氨水后搅拌、过滤、洗涤、干燥。
②将第一步得到的 、乙二胺四乙酸(H4Y)、H2O加入图二仪器a中,搅拌,80℃水浴1h,再加入适量碳酸钠溶液反应10min。
、乙二胺四乙酸(H4Y)、H2O加入图二仪器a中,搅拌,80℃水浴1h,再加入适量碳酸钠溶液反应10min。
③经蒸发浓缩、冷却结晶,过滤洗涤,晾干得到产品。
回答下列问题:___________ 、___________ 。
(2)步骤①中氨水应当___________ (填“分批”或“一次性”)加入,原因是___________ 。
(3)盛装Na2CO3溶液仪器名称为___________ ,加入碳酸钠溶液后可观察到产生大量气泡,则步骤②由 生成NaFeY⋅3H2O的总反应化学方程式为
生成NaFeY⋅3H2O的总反应化学方程式为___________ 。
(4)步骤③蒸发浓缩至___________ (填现象)时,停止加热。
(5)市售铁强化剂中含有NaCl、KIO3、NaFeY,其中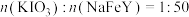 。称取mg样品,加稀硫酸溶解后配成100mL溶液。取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用
。称取mg样品,加稀硫酸溶解后配成100mL溶液。取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用 标准溶液滴定,重复操作2~3次,消耗
标准溶液滴定,重复操作2~3次,消耗 标准溶液的平均值为VmL。
标准溶液的平均值为VmL。
已知:

①滴定终点的现象为___________ 。
②样品中铁元素的质量分数为___________ 。
①称取一定质量的FeCl3⋅6H2O于烧杯中溶解,加入适量浓氨水后搅拌、过滤、洗涤、干燥。
②将第一步得到的
 、乙二胺四乙酸(H4Y)、H2O加入图二仪器a中,搅拌,80℃水浴1h,再加入适量碳酸钠溶液反应10min。
、乙二胺四乙酸(H4Y)、H2O加入图二仪器a中,搅拌,80℃水浴1h,再加入适量碳酸钠溶液反应10min。③经蒸发浓缩、冷却结晶,过滤洗涤,晾干得到产品。
回答下列问题:
(2)步骤①中氨水应当
(3)盛装Na2CO3溶液仪器名称为
 生成NaFeY⋅3H2O的总反应化学方程式为
生成NaFeY⋅3H2O的总反应化学方程式为(4)步骤③蒸发浓缩至
(5)市售铁强化剂中含有NaCl、KIO3、NaFeY,其中
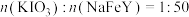 。称取mg样品,加稀硫酸溶解后配成100mL溶液。取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用
。称取mg样品,加稀硫酸溶解后配成100mL溶液。取出10.00mL,加入稍过量的KI溶液,充分反应后,滴入淀粉溶液,用 标准溶液滴定,重复操作2~3次,消耗
标准溶液滴定,重复操作2~3次,消耗 标准溶液的平均值为VmL。
标准溶液的平均值为VmL。已知:


①滴定终点的现象为
②样品中铁元素的质量分数为
您最近一年使用:0次
2024-06-11更新
|
148次组卷
|
2卷引用:2024届河南省漯河市高级中学高三下学期三模理综试题-高中化学
10 . 实验室可用如图装置探究可燃物的燃烧条件,根据所学知识回答下列问题:____ 。
(2)气球的作用是____ 。
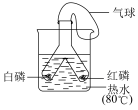
(2)气球的作用是
您最近一年使用:0次