1 . 根据所给信息及要求填空。
(1) 时,四种弱电解质的电离平衡常数如表:
时,四种弱电解质的电离平衡常数如表:
①常温下, 的
的 溶液加水稀释过程,下列说法错误的是
溶液加水稀释过程,下列说法错误的是___________ (填字母)。
a. 增大 b.
增大 b. 增大
增大
c. 的电离程度增大 d.
的电离程度增大 d. 增大
增大
②下列反应不能发生的是___________ (填字母)。
A.
B.
C.
D.
(2)常温下,有 相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:
相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:
①分别加适量醋酸钠晶体后,忽略溶液体积的变化,则醋酸溶液中
___________ (填“增大”、“减小”或“不变”,下同),盐酸溶液中
___________ 。
②分别加等浓度的 溶液至恰好中和,所需
溶液至恰好中和,所需 溶液的体积:醋酸溶液
溶液的体积:醋酸溶液___________ (填“>”、“=”或“<”)盐酸溶液。
(1)
 时,四种弱电解质的电离平衡常数如表:
时,四种弱电解质的电离平衡常数如表:| 化学式 |  |  |  |  |
| 电离平衡常数 | 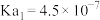 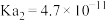 |  |  |  |
 的
的 溶液加水稀释过程,下列说法错误的是
溶液加水稀释过程,下列说法错误的是a.
 增大 b.
增大 b. 增大
增大c.
 的电离程度增大 d.
的电离程度增大 d. 增大
增大②下列反应不能发生的是
A.

B.

C.

D.

(2)常温下,有
 相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:
相同、体积相同的醋酸溶液和盐酸溶液,现采取以下措施:①分别加适量醋酸钠晶体后,忽略溶液体积的变化,则醋酸溶液中


②分别加等浓度的
 溶液至恰好中和,所需
溶液至恰好中和,所需 溶液的体积:醋酸溶液
溶液的体积:醋酸溶液
您最近一年使用:0次
名校
解题方法
2 . CS2是一种重要的化工原料。工业上可以利用固体硫(S8)与CH4为原料制备CS2,S8受热分解成气态S2,发生反应2S2(g)+CH4(g)⇌CS2(g)+2H2S(g),回答下列问题:
(1)某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2:1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为___________ 。
②当以下数值不变时,能说明该反应达到平衡的是___________ (填序号)。
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
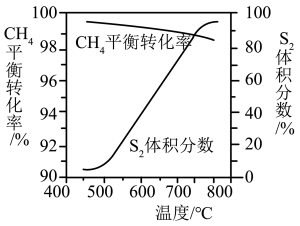
(2)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为___________ (填“放热”或“吸热”)反应。工业上通常采用在600~650℃的条件下进行此反应,不采用低于600℃的原因是___________ 。
(3)已知常温常压下,64gS8完全分解为S2气体吸收的热量为akJ,S2气体的燃烧热为 ,写出表示S8燃烧热的热化学方程式:
,写出表示S8燃烧热的热化学方程式:___________ 。
(1)某温度下,若S8完全分解成气态S2.在恒温密闭容器中,S2与CH4物质的量比为2:1时开始反应。
①当CS2的体积分数为10%时,CH4的转化率为
②当以下数值不变时,能说明该反应达到平衡的是
a.气体密度 b.气体总压 c.CH4与S2体积比 d.CS2的体积分数
(2)一定条件下,CH4与S2反应中CH4的平衡转化率、S8分解产生S2的体积分数随温度的变化曲线如图所示。据图分析,生成CS2的反应为

(3)已知常温常压下,64gS8完全分解为S2气体吸收的热量为akJ,S2气体的燃烧热为
 ,写出表示S8燃烧热的热化学方程式:
,写出表示S8燃烧热的热化学方程式:
您最近一年使用:0次
名校
解题方法
3 . 25℃时,在体积为2L的恒容密闭容器中通入0.08molNO和0.04molCl2发生反应2NO(g)+Cl2(g)⇌2NOCl(g) △H。
(1)若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图I实线所示,则△H___________ 0(填“>”、“<”或“=”);
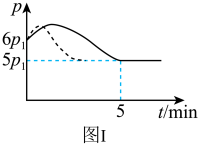
(2)若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图I虚线所示,则改变的条件是___________ ;在5min时,再充入0.08molNO和0.04molCl2,则混合气体的平均相对分子质量将___________ (填“增大”、“减小”或“不变”)。
(3)图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(lgK)与温度的变化关系图,其中正确的曲线是___________ (填“甲”或“乙”),a值为___________ 。25℃时测得该反应在某时刻,NO(g)、Cl2(g)、NOCl(g)的浓度分别为0.8、0.1、0.3,则此时v正___________ v逆(填“>”、“<”或“=”)

(1)若反应开始与结束时温度相同,数字压强仪显示反应过程中压强(p)随时间(t)的变化如图I实线所示,则△H

(2)若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图I虚线所示,则改变的条件是
(3)图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值(lgK)与温度的变化关系图,其中正确的曲线是

您最近一年使用:0次
名校
4 . 按要求回答下列问题
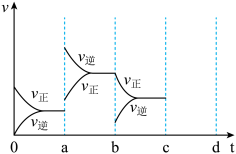
(1)在密闭容器中反应:2SO2+O2⇌2SO3 △H=-QkJmol∙L-1到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如图1所示,a→b过程中改变的条件可能是___________ ;b→c过程中改变的条件可能是___________ ;若增大压强时,将反应速率变化情况画在c~d处(d前已经达到化学平衡)___________ 。
(2)在一个容积固定的密闭容器中进行反应2X(g)+Y(g)⇌2Z(g),已知将2molX和1molY充入该容器,反应在绝热条件下进行达到平衡时,加入催化剂和未加催化剂的速率-时间图(v-t)如图所示,下列说法正确的有___________ (填序号)
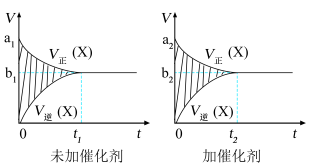
①a1>a2 ②b1>b2 ③t1>t2 ④两图阴影部分面积一样大 ⑤加催化剂的图阴影面积更大
(3)可逆反应CO(g)+H2(g)⇌H2O(g)+C(s),在500K下,向体积为2L的密闭刚性容器中充入1molCO和2molH2进行反应,经10min达到平衡。若初始压强为akPa,平衡时H2的转化率为25%。CO在10min内的平均速率为________ ;500K下,该反应的压强平衡常数为Kp=________ (用含a的式子表示);若平衡后向该容器中加入CO和H2O各0.5mol,平衡_________ (填“向左移动”“向右移动”或“不移动”)。
(1)在密闭容器中反应:2SO2+O2⇌2SO3 △H=-QkJmol∙L-1到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如图1所示,a→b过程中改变的条件可能是

(2)在一个容积固定的密闭容器中进行反应2X(g)+Y(g)⇌2Z(g),已知将2molX和1molY充入该容器,反应在绝热条件下进行达到平衡时,加入催化剂和未加催化剂的速率-时间图(v-t)如图所示,下列说法正确的有

①a1>a2 ②b1>b2 ③t1>t2 ④两图阴影部分面积一样大 ⑤加催化剂的图阴影面积更大
(3)可逆反应CO(g)+H2(g)⇌H2O(g)+C(s),在500K下,向体积为2L的密闭刚性容器中充入1molCO和2molH2进行反应,经10min达到平衡。若初始压强为akPa,平衡时H2的转化率为25%。CO在10min内的平均速率为
您最近一年使用:0次
名校
5 . 按要求回答下列问题。
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应N2(g)+O2(g)⇌2NO(g)是导致汽车尾气中含有NO的原因之一、已知H2可以催化还原NO达到消除污染的目的。
N2(g)+O2(g)⇌2NO(g) △H=+180.5kJ∙mol-1
2H2(g)+O2(g)⇌2H2O(l) △H=-571.6kJ∙mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是___________ ,判断该反应自发进行的条件:___________ 。(填“高温自发”或“低温自发”)
(2)已知H2S为二元弱酸,欲使0.1mol•L-1的H2S溶液中 的比值变大,下列措施可行的是
的比值变大,下列措施可行的是___________
a.加入H2O b.通入少量H2S c.通入少量HCl d.加入少量NaOH固体
(3)有下列物质:①Zn②KAl(SO4)2∙12H2O③Ba(OH)2④乙醇⑤冰醋酸⑥盐酸⑦Cu(NO3)2溶液⑧熔融态AlCl3⑨NH3∙H2O⑩熔融态CH3COONa⑪NaHCO3。其中属于能导电的电解质的是___________ (填编号)属于弱电解质的是___________ (填编号)
(4)若向0.1mol∙L-1的弱碱MOH溶液中逐滴加入0.1mol∙L-1的弱酸HB至恰好反应,溶液的导电性变化规律是___________ (填“逐渐变强”、“逐渐变弱”、“先变强后变弱”、“先变弱后变强”和“几乎不变”)
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应N2(g)+O2(g)⇌2NO(g)是导致汽车尾气中含有NO的原因之一、已知H2可以催化还原NO达到消除污染的目的。
N2(g)+O2(g)⇌2NO(g) △H=+180.5kJ∙mol-1
2H2(g)+O2(g)⇌2H2O(l) △H=-571.6kJ∙mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是
(2)已知H2S为二元弱酸,欲使0.1mol•L-1的H2S溶液中
 的比值变大,下列措施可行的是
的比值变大,下列措施可行的是a.加入H2O b.通入少量H2S c.通入少量HCl d.加入少量NaOH固体
(3)有下列物质:①Zn②KAl(SO4)2∙12H2O③Ba(OH)2④乙醇⑤冰醋酸⑥盐酸⑦Cu(NO3)2溶液⑧熔融态AlCl3⑨NH3∙H2O⑩熔融态CH3COONa⑪NaHCO3。其中属于能导电的电解质的是
(4)若向0.1mol∙L-1的弱碱MOH溶液中逐滴加入0.1mol∙L-1的弱酸HB至恰好反应,溶液的导电性变化规律是
您最近一年使用:0次
名校
6 . 填空。
(1)欲除去FeCl2溶液中的Fe3+,可向溶液中加少量___________ ,请用离子方程式表示除杂原理___________ 。
(2)下列属于氮的固定的是___________ (填序号)。
①工业合成氨
②雷雨天气N2与O2反应
③工业制硝酸的第一步反应:氨的催化氧化
写出上述反应①③的化学方程式:①___________ ,③___________ 。
(3)Fe2O3和铝粉常用于野外焊接钢轨,试写出其化学方程式:___________ 。
(4)检验 的离子方程式:
的离子方程式:___________ 。
(1)欲除去FeCl2溶液中的Fe3+,可向溶液中加少量
(2)下列属于氮的固定的是
①工业合成氨
②雷雨天气N2与O2反应
③工业制硝酸的第一步反应:氨的催化氧化
写出上述反应①③的化学方程式:①
(3)Fe2O3和铝粉常用于野外焊接钢轨,试写出其化学方程式:
(4)检验
 的离子方程式:
的离子方程式:
您最近一年使用:0次
名校
7 . 用铁、铝的混合物进行如图实验:

(1)加入过量NaOH溶液发生的离子反应方程式________ ,操作X的名称是________ 。
(2)铝在空气中表面形成的氧化膜很薄,为了适应不同用途,需将表面氧化膜碱洗除去再进行处理,请写出碱洗氧化膜的离子方程式________ 。
(3)某课外兴趣小组为探究某种铝合金(组成元素为Mg和Al)是否符合国家质量标准(国家规定铝合金中铝含量不能低于78%),设计如图装置在室温下进行实验。

反应前先第一次读取量气管液面刻度,然后倾斜左边装置使足量氢氧化钠溶液与ag铝合金样品充分反应,待反应停止后,体系温度恢复到室温,第二次读取量气管液面刻度之前需要进行的一步操作是________ 。计算两次液面差,并将气体体积折算成标准状况下的体积,为VmL。若a=0.039,V=33.6mL,说明该合金________ (填“符合”或“不符合”)符合国家标准。
(4)若将装置中的足量氢氧化钠溶液换为足量盐酸,则反应停止后量气管内气体体积(折算成标准状况下)_______ mL。

(1)加入过量NaOH溶液发生的离子反应方程式
(2)铝在空气中表面形成的氧化膜很薄,为了适应不同用途,需将表面氧化膜碱洗除去再进行处理,请写出碱洗氧化膜的离子方程式
(3)某课外兴趣小组为探究某种铝合金(组成元素为Mg和Al)是否符合国家质量标准(国家规定铝合金中铝含量不能低于78%),设计如图装置在室温下进行实验。

反应前先第一次读取量气管液面刻度,然后倾斜左边装置使足量氢氧化钠溶液与ag铝合金样品充分反应,待反应停止后,体系温度恢复到室温,第二次读取量气管液面刻度之前需要进行的一步操作是
(4)若将装置中的足量氢氧化钠溶液换为足量盐酸,则反应停止后量气管内气体体积(折算成标准状况下)
您最近一年使用:0次
8 . 回答下列问题:
(1)以下合成材料制品中,属于塑料制品的是_______ ;属于橡胶制品的是_______ ;属于纤维制品的是_______ ;属于复合材料制品的是_______ 。
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子_______ (填“被氧化”或“被还原”),生成阳离子的过程;在海水中为防止钢铁巨轮被腐蚀,常在轮船水面下的船体上焊上_______ (填“锌块”或“铜块”)。
(1)以下合成材料制品中,属于塑料制品的是
A.聚乙烯制品 B.汽车轮胎 C.玻璃钢 D.涤纶
(2)金属腐蚀的本质是金属原子失去电子
您最近一年使用:0次
解题方法
9 . 回答下列问题:
(1)正常雨水的pH为5.6,这是因为大气中二氧化碳溶于雨水的缘故。CO2与水反应生成H2CO3的化学方程式为_______ 。酸雨主要是由人为排放的 _______ 等气体转化为酸造成的。二氧化碳是污染气体吗?_______ (是或不是)。
(2)垃圾处理的常用方法有卫生填埋、焚烧和_______ (填“堆肥”或“排入大海”)。污水处理的主要方法之一是混凝法,_______ (填“食盐或“明矾”)是常用的混凝剂之一。
(3)生活中提倡垃圾分类回收,下列不属于可回收垃圾的是_______ 。
甲:旧报纸 乙:水果皮 丙:废金属
(1)正常雨水的pH为5.6,这是因为大气中二氧化碳溶于雨水的缘故。CO2与水反应生成H2CO3的化学方程式为
(2)垃圾处理的常用方法有卫生填埋、焚烧和
(3)生活中提倡垃圾分类回收,下列不属于可回收垃圾的是
甲:旧报纸 乙:水果皮 丙:废金属
您最近一年使用:0次
10 . 回答下列问题:
(1)蛋白质、淀粉、油脂是三种重要的营养物质,其中_______ 不是高分子化合物,这三种物质水解的最终产物分别是蛋白质
_______ ;淀粉
_______ ;脂肪
_______ 。
(2)俗话说“民以食为天”,食物是维持人体生命和保障健康的物质基础。下列食物中含有不同的营养物质,其中花生油中含有大量的_______ (填字母);新鲜水果和蔬菜中富含_______ ;牛奶中含有大量的_______ ;大米中_______ 的含量为75%左右。
A. 蛋白质 B.油脂 C.淀粉 D.维生素
(1)蛋白质、淀粉、油脂是三种重要的营养物质,其中



(2)俗话说“民以食为天”,食物是维持人体生命和保障健康的物质基础。下列食物中含有不同的营养物质,其中花生油中含有大量的
A. 蛋白质 B.油脂 C.淀粉 D.维生素
您最近一年使用:0次



