按要求回答下列问题。
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应N2(g)+O2(g)⇌2NO(g)是导致汽车尾气中含有NO的原因之一、已知H2可以催化还原NO达到消除污染的目的。
N2(g)+O2(g)⇌2NO(g) △H=+180.5kJ∙mol-1
2H2(g)+O2(g)⇌2H2O(l) △H=-571.6kJ∙mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是___________ ,判断该反应自发进行的条件:___________ 。(填“高温自发”或“低温自发”)
(2)已知H2S为二元弱酸,欲使0.1mol•L-1的H2S溶液中 的比值变大,下列措施可行的是
的比值变大,下列措施可行的是___________
a.加入H2O b.通入少量H2S c.通入少量HCl d.加入少量NaOH固体
(3)有下列物质:①Zn②KAl(SO4)2∙12H2O③Ba(OH)2④乙醇⑤冰醋酸⑥盐酸⑦Cu(NO3)2溶液⑧熔融态AlCl3⑨NH3∙H2O⑩熔融态CH3COONa⑪NaHCO3。其中属于能导电的电解质的是___________ (填编号)属于弱电解质的是___________ (填编号)
(4)若向0.1mol∙L-1的弱碱MOH溶液中逐滴加入0.1mol∙L-1的弱酸HB至恰好反应,溶液的导电性变化规律是___________ (填“逐渐变强”、“逐渐变弱”、“先变强后变弱”、“先变弱后变强”和“几乎不变”)
(1)汽车尾气是城市主要空气污染物,汽车内燃机工作时发生反应N2(g)+O2(g)⇌2NO(g)是导致汽车尾气中含有NO的原因之一、已知H2可以催化还原NO达到消除污染的目的。
N2(g)+O2(g)⇌2NO(g) △H=+180.5kJ∙mol-1
2H2(g)+O2(g)⇌2H2O(l) △H=-571.6kJ∙mol-1
写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是
(2)已知H2S为二元弱酸,欲使0.1mol•L-1的H2S溶液中
 的比值变大,下列措施可行的是
的比值变大,下列措施可行的是a.加入H2O b.通入少量H2S c.通入少量HCl d.加入少量NaOH固体
(3)有下列物质:①Zn②KAl(SO4)2∙12H2O③Ba(OH)2④乙醇⑤冰醋酸⑥盐酸⑦Cu(NO3)2溶液⑧熔融态AlCl3⑨NH3∙H2O⑩熔融态CH3COONa⑪NaHCO3。其中属于能导电的电解质的是
(4)若向0.1mol∙L-1的弱碱MOH溶液中逐滴加入0.1mol∙L-1的弱酸HB至恰好反应,溶液的导电性变化规律是
更新时间:2024-01-19 16:10:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】有以下9种物质,请回答下列问题:
①干冰②氯化钠③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液⑧氯化氢⑨NH3
(1)其中能导电的是__ (填写序号,下同);属于电解质的是__ ;属于非电解质的是__ 。
(2)分别写出物质⑤在水中的电离方程式:__ 。
(3)写出物质④和⑦反应的离子方程式:__ 。
(4)写出物质⑤和⑥在水中发生反应的离子方程式:__ 。
①干冰②氯化钠③蔗糖④稀硫酸⑤NaHSO4溶液⑥碳酸氢钠⑦氢氧化钡溶液⑧氯化氢⑨NH3
(1)其中能导电的是
(2)分别写出物质⑤在水中的电离方程式:
(3)写出物质④和⑦反应的离子方程式:
(4)写出物质⑤和⑥在水中发生反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某学习小组以氢氧化钡、水、硫酸为实验对象探究离子反应发生的条件。
(1)氢氧化钡与硫酸在溶液中能发生___________ (填字母)反应。
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加水后,灯泡变亮的原因是氢氧化钡发生了___________ 。
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因___________ 。
(4)实验2:用硫酸钠溶液替代稀硫酸,重复实验进行对照。
①硫酸钠溶液中 的浓度与稀硫酸中
的浓度与稀硫酸中 的浓度
的浓度___________ (填“相等”或“不相等”)。
②加入硫酸钠溶液过程中灯泡不熄灭,原因是___________ 。
| 实验1:向烧杯依次加入下列试剂,记录灯泡变化 | |
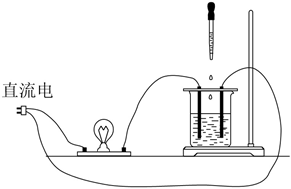 | ①氢氧化钡粉末:灯泡不亮 ②加入蒸馏水:灯泡变亮 ③逐滴滴加稀硫酸,灯泡变化如下: 亮  暗 暗 熄灭 熄灭 亮 亮 |
(1)氢氧化钡与硫酸在溶液中能发生
a.复分解反应 b.氧化还原反应 c.置换反应
(2)加水后,灯泡变亮的原因是氢氧化钡发生了
(3)用离子方程式解释过程Ⅰ中灯泡变暗的原因
(4)实验2:用硫酸钠溶液替代稀硫酸,重复实验进行对照。
①硫酸钠溶液中
 的浓度与稀硫酸中
的浓度与稀硫酸中 的浓度
的浓度②加入硫酸钠溶液过程中灯泡不熄灭,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有下列十种物质:①H2 ②铝 ③醋酸 ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦氨水 ⑧稀硝酸⑨熔融Al2(SO4)3 ⑩NaHSO4。
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是__________ ;属于电解质的是__________ ;能导电的是____________ 。
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH−===H2O,该离子反应对应的化学方程式为_____________________________ 。
(3)写出③和⑦反应的离子方程式为__________________ ,34.2 g ⑨溶于水配成250 mL溶液,SO42-的物质的量浓度为_________________ 。
(4)过量的④通入⑥的溶液中反应的离子方程式为______________________ 。
(5)将⑩的溶液加入⑥的溶液中至溶液中的Ba2+离子恰好完全沉淀时反应的离子方程式为__________ 。
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH−===H2O,该离子反应对应的化学方程式为
(3)写出③和⑦反应的离子方程式为
(4)过量的④通入⑥的溶液中反应的离子方程式为
(5)将⑩的溶液加入⑥的溶液中至溶液中的Ba2+离子恰好完全沉淀时反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】从能量的角度看,断开化学键要________ , 形成化学键要________ . 已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151k J、299k J.则由氢气和碘反应生成1mol HI需要________ (填“放出”或“吸收”)_________ k J的热量.当反应物的总能量高于生成物总能量时,该反应为________ 反应;当反应物的总能量低于生成物总能量时,该反应为______ 反应.
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)CO还原脱硝技术可有效降低烟气中的NOx的排放量。回答下列问题:
CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g) △H1=—226kJ•mol—1
N2(g)+2O2(g)⇌2NO2(g) △H2=+68kJ•mol—1
N2(g)+O2(g)⇌2NO(g) △H3=+183kJ•mol—1
脱硝反应△H=______ ,该反应向正反应方向自发进行的倾向很大,其原因是_______ ,有利于提高NO平衡转化率的条件是(写出两条)________ 、___________ 。
(2)直接供氨式燃料电池是以NaOH溶液为电解质的.电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为_________ 。
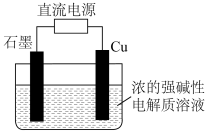
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出阳极的电极反应式_______ 。
CO还原NO的脱硝反应:2CO(g)+2NO(g)⇌2CO2(g)+N2(g) △H
已知:CO(g)+NO2(g)⇌CO2(g)+NO(g) △H1=—226kJ•mol—1
N2(g)+2O2(g)⇌2NO2(g) △H2=+68kJ•mol—1
N2(g)+O2(g)⇌2NO(g) △H3=+183kJ•mol—1
脱硝反应△H=
(2)直接供氨式燃料电池是以NaOH溶液为电解质的.电池反应为:4NH3+3O2=2N2+6H2O,则负极电极反应式为
(3)用甲醇燃料电池作为直流电源,设计如图装置制取Cu2O,电解总反应为:2Cu+H2O=Cu2O+H2↑。写出阳极的电极反应式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2021年12月9日,神舟十三号航天员翟志刚、王亚平和叶光富在中国空间站太空授课,空间站内氧气和二氧化碳的循环利用引发了同学们强烈的好奇心。请根据有关信息回答下列问题。
(1)空间站主要利用电解生活废水及尿液实现氧气再生,阳极的电极反应式为______ 。
(2)叶光富介绍,有望在空间站利用CO2与H2反应生成水和燃料,实现呼吸产生的CO2与电解水产生的H2的高效循环利用。二氧化碳与氢气制甲醇的总反应可表示为:CO2(g)+3H2(g)→CH3OH(g)+H2O(g) △H。
该反应一般通过如下步骤来实现:
i.CO2(g)+H2(g)→CO(g)+H2O(g) △H1=+41kJ•mol-1
ii.CO(g)+2H2(g)→CH3OH(g) △H2=-90kJ•mol-1
①总反应的△H=_____ kJ•mol-1;若反应i为慢反应,下列示意图中能体现上述反应能量变化的是_____ (填标号),判断的理由是_____ 。
A. B.
B.
C.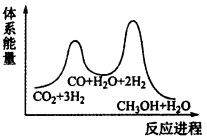 D.
D.
②甲醇是燃料电池的重要原料,若电解质为H2SO4溶液,则负极的电极反应式为_____ 。
(3)利用电化学原理可以将H2O和CO2转化为O2和燃料(C3H8O),实验装量如图所示,则H+移向_____ 极(填“a”或“b”)。

(1)空间站主要利用电解生活废水及尿液实现氧气再生,阳极的电极反应式为
(2)叶光富介绍,有望在空间站利用CO2与H2反应生成水和燃料,实现呼吸产生的CO2与电解水产生的H2的高效循环利用。二氧化碳与氢气制甲醇的总反应可表示为:CO2(g)+3H2(g)→CH3OH(g)+H2O(g) △H。
该反应一般通过如下步骤来实现:
i.CO2(g)+H2(g)→CO(g)+H2O(g) △H1=+41kJ•mol-1
ii.CO(g)+2H2(g)→CH3OH(g) △H2=-90kJ•mol-1
①总反应的△H=
A.
 B.
B.
C.
 D.
D.
②甲醇是燃料电池的重要原料,若电解质为H2SO4溶液,则负极的电极反应式为
(3)利用电化学原理可以将H2O和CO2转化为O2和燃料(C3H8O),实验装量如图所示,则H+移向

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)==2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:_______ 。
(2)下列反应中,在高温下不能自发进行的是_____ (填字母)。
a.CO(g)==C(s)+ O2(g)
O2(g)
b.2N2O5(g)==4NO2(g)+O2(g)
c.(NH4)2CO3(s)==NH4HCO3(s)+NH3(g)
d.MgCO3(s)===MgO(s)+CO2(g)
(3)运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)==H2(g)+CO(g) ΔH=+131.3kJ·mol-1,ΔS=+133.7J·mol-1·K-1,该反应在低温下______ (填“能”或“不能”)自发进行。
(1)汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:2CO(g)==2C(s)+O2(g)。已知该反应的ΔH>0,简述该设想能否实现的依据:
(2)下列反应中,在高温下不能自发进行的是
a.CO(g)==C(s)+
 O2(g)
O2(g)b.2N2O5(g)==4NO2(g)+O2(g)
c.(NH4)2CO3(s)==NH4HCO3(s)+NH3(g)
d.MgCO3(s)===MgO(s)+CO2(g)
(3)运用化学反应原理研究合成氨反应有重要意义,请完成下列探究。生产氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)==H2(g)+CO(g) ΔH=+131.3kJ·mol-1,ΔS=+133.7J·mol-1·K-1,该反应在低温下
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】填空。
(1)(2023·湖北宜昌市协作体高二上学期期中)甲烷是重要的气体燃料和化工原料,由CH4制取合成气(CO、H2)的反应原理为CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0。当体系温度等于TK时ΔH−TΔS=0,温度大于T时ΔH−TΔS___________ (填“>”“<”或“=”)0。
(2)(2023·四川内江市高二上学期期末)反应I(2NH3(g)+CO2(g)⇌H2NCOONH4 ΔH1<0)在___________ (填“高温”、“低温”或“任何温度”)下能自发进行。
(3)(2023·新疆生产建设兵团部分名校高二上学期期中)已知:H2(g)+C2H4(g)⇌C2H6(g) ΔH=-137kJ·mol-1。该反应在___________ (填“低温”、“高温”或“任何温度”)下能自发进行。
(1)(2023·湖北宜昌市协作体高二上学期期中)甲烷是重要的气体燃料和化工原料,由CH4制取合成气(CO、H2)的反应原理为CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH>0。当体系温度等于TK时ΔH−TΔS=0,温度大于T时ΔH−TΔS
(2)(2023·四川内江市高二上学期期末)反应I(2NH3(g)+CO2(g)⇌H2NCOONH4 ΔH1<0)在
(3)(2023·新疆生产建设兵团部分名校高二上学期期中)已知:H2(g)+C2H4(g)⇌C2H6(g) ΔH=-137kJ·mol-1。该反应在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇被称为2l世纪的新型燃料,工业上通过下列反应Ⅰ和Ⅱ,用CH4和H2O为原料来制备甲醇。
(1)将1.0molCH4和2.0molH2O(g)通入容积为10L的反应室,在一定条件下发生反应Ⅰ:CH4(g)+H2O(g) CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图:
CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图:
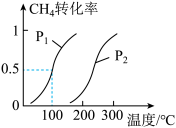
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为______ 。
②在其它条件不变的情况下升高温度,化学平衡常数将_______ (填“增大”“减小”或“不变”)。
③图中的P1_____ P2(填“<”、“>”或“=”),100℃时平衡常数为________ 。
④保持反应体系为100℃,5min后再向容器中充入H2O、H2各0.5mol,化学平衡将向_____ 移动(填“向左”“向右”或“不”)。
(2)在压强为0.1MPa条件下,将amolCO与3amol H2的混合气体在催化剂作用下能自发发生反应Ⅱ:
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
①该反应的△H_____ 0,△S_____ 0(填“<”、“>”或“=”)。
②若容器容积不变,下列措施可以提高CO转化率的是______ 。
A.升高温度
B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大
D.再充入1molCO和3molH2
(1)将1.0molCH4和2.0molH2O(g)通入容积为10L的反应室,在一定条件下发生反应Ⅰ:CH4(g)+H2O(g)
 CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图:
CO(g)+3H2(g),CH4的转化率与温度、压强的关系如图:
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为
②在其它条件不变的情况下升高温度,化学平衡常数将
③图中的P1
④保持反应体系为100℃,5min后再向容器中充入H2O、H2各0.5mol,化学平衡将向
(2)在压强为0.1MPa条件下,将amolCO与3amol H2的混合气体在催化剂作用下能自发发生反应Ⅱ:
CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)①该反应的△H
②若容器容积不变,下列措施可以提高CO转化率的是
A.升高温度
B.将CH3OH(g)从体系中分离出来
C.充入He,使体系总压强增大
D.再充入1molCO和3molH2
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在0.5 mol/L的NaHSO3溶液中滴入石蕊,溶液变红。试回答有关问题:
(1)该溶液中 的电离程度
的电离程度___________ (填“大于”“小于”或“等于”)  的水解程度。
的水解程度。
(2)溶液中Na+、 、
、 、H+、OH-、H2SO3、H2O等粒子的浓度由大到小的顺序为
、H+、OH-、H2SO3、H2O等粒子的浓度由大到小的顺序为___________ 。
(3)在Na2SO3溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是___________ ,其原因是(以离子方程式和简要文字说明)___________ 。
(1)该溶液中
 的电离程度
的电离程度 的水解程度。
的水解程度。(2)溶液中Na+、
 、
、 、H+、OH-、H2SO3、H2O等粒子的浓度由大到小的顺序为
、H+、OH-、H2SO3、H2O等粒子的浓度由大到小的顺序为(3)在Na2SO3溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)室温下,Ksp(BaSO4)=1.1×10-10,将pH=9 的 Ba(OH)2溶液与 pH=4 的 H2SO4溶液混合,若所得混合溶液的 pH=7,则 Ba(OH)2溶液与 H2SO4溶液的体积比为___________ 。欲使溶液中c(SO42-)≤1.0×10-5mol·L-1,则应保持溶液中 c(Ba2+) ≥_____ mol·L-1。
(2)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 molCH3COONa固体,则醋酸的电离平衡向____ (填“正”或“逆”)反应方向移动;溶液中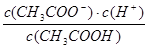 的值
的值_____ (填“增大”、“减小”或“不变”)。
(3)已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5
b.CH3COOH+NaHCO3 = CH3COONa+CO2↑+H2O 室温下,CH3COONH4溶液呈_________ 性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈__________ 性。NH4HCO3溶液中物质的量浓度最大的离子是_____ (填化学式)。
(2)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 molCH3COONa固体,则醋酸的电离平衡向
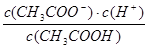 的值
的值(3)已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5
b.CH3COOH+NaHCO3 = CH3COONa+CO2↑+H2O 室温下,CH3COONH4溶液呈
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知25℃时,电离平衡常数:
回答下列问题:
(1)下列四种物质电离出质子的能力由大到小的顺序是___________ (填标号)。
a、HCO3- b、HClO c、CH3COOH d、H2CO3
(2)下列反应不能发生的是___________。
(3)用蒸馏水稀释0.10mol·L-1的醋酸,则下列各式表示的数值随水量的增加而增大的是___________。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1=4.4×10-7K2=4.7×10-11 | 3.0×10-8 |
(1)下列四种物质电离出质子的能力由大到小的顺序是
a、HCO3- b、HClO c、CH3COOH d、H2CO3
(2)下列反应不能发生的是___________。
A. |
| B.ClO-+CH3COOH=CH3COO-+HClO |
C.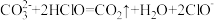 |
D.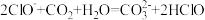 |
A. | B. | C. | D. |
您最近一年使用:0次



