名校
1 . I.回答下列问题:
(1)对以下有机物进行系统命名: 的结构简式改写为键线式:
的结构简式改写为键线式:___________ 。
(3)上述(1)中分子②最多有___________ 个碳原子共平面。
(4)分子式为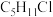 的同分异构体共有___________(不考虑立体异构)。
的同分异构体共有___________(不考虑立体异构)。
II.青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物,其分子结构如图所示,它可以用有机溶剂A从中药中提取。
(5)下列关于青蒿素的说法不正确的是___________ (填字母)。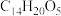
b.分子中含有酯基和醚键
c.易溶于有机溶剂A,不易溶于水
d.分子的空间结构不是平面形
(6)使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如下:___________ 。
②根据图2,推测A可能所属的有机化合物类别:___________ ,A的分子式:___________ 。
③根据以上结果和图3(两个峰的面积比为2:3),推测A的结构简式___________ 。
(1)对以下有机物进行系统命名:
①键线式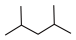 :
:
② :
:
 的结构简式改写为键线式:
的结构简式改写为键线式:(3)上述(1)中分子②最多有
(4)分子式为
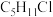 的同分异构体共有___________(不考虑立体异构)。
的同分异构体共有___________(不考虑立体异构)。| A.6种 | B.7种 | C.8种 | D.9种 |
II.青蒿素是我国科学家从传统中药中发现的能治疗疟疾的有机化合物,其分子结构如图所示,它可以用有机溶剂A从中药中提取。
(5)下列关于青蒿素的说法不正确的是

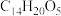
b.分子中含有酯基和醚键
c.易溶于有机溶剂A,不易溶于水
d.分子的空间结构不是平面形
(6)使用现代分析仪器对有机化合物A的分子结构进行测定,相关结果如下:
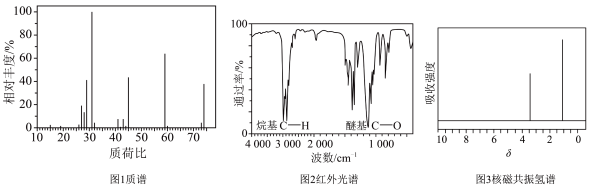
②根据图2,推测A可能所属的有机化合物类别:
③根据以上结果和图3(两个峰的面积比为2:3),推测A的结构简式
您最近一年使用:0次
名校
解题方法
2 . I.有一块镀铜的铁制品,已严重锈蚀[铜锈成分视为 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
(1)气体甲的成分是___________ (填化学式),固体乙的成分是___________ (填名称)。
(2)铁发生的反应属于四种基本反应类型中的___________ 。
(3)滤液丙的颜色可能是___________(选填编号)。
(4)确认滤液丙中是否含有亚铁离子,适宜的试剂是___________(选填编号)。
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为 。
。
(5)假若反应生成的还原产物只有一种,则还原产物是___________ 。
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式___________ 。
 ],铁锈成分视为
],铁锈成分视为 ],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。
],实验小组同学将它粉碎后,放入过量的稀硫酸中微热使之充分反应,收集到气体甲,过滤得到固体乙和滤液丙。(1)气体甲的成分是
(2)铁发生的反应属于四种基本反应类型中的
(3)滤液丙的颜色可能是___________(选填编号)。
| A.棕黄色 | B.蓝色 | C.浅绿色 | D.无色 |
A. 溶液 溶液 | B.NaOH溶液 |
C.KSCN溶液和 溶液 溶液 | D. 淀粉试纸 淀粉试纸 |
Ⅱ.铁与不同浓度硝酸反应时主要还原产物不同。现将过量铁与一定浓度的硝酸充分反应,测得消耗的铁与被还原的硝酸的物质的量之比为
 。
。(5)假若反应生成的还原产物只有一种,则还原产物是
(6)所得溶液与碳酸氢铵溶液混合可获得碳酸亚铁沉淀,同时有气体生成。写出反应生成碳酸亚铁的离子方程式
您最近一年使用:0次
3 . Ⅰ. 、
、 、
、 都是重要的能源物质,也是重要的化工原料。
都是重要的能源物质,也是重要的化工原料。
(1)下列事实能说明 分子呈正四面体结构的是_______(填字母)。
分子呈正四面体结构的是_______(填字母)。
(2)甲烷与下列烃的通式相同的是_______ (填字母)。_______ 。
②写出装置C中 与
与 反应生成氯仿(
反应生成氯仿( )的化学方程式
)的化学方程式_______ 。
③若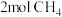 与
与 发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是
发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是_______ mol。
Ⅱ.用 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。
(4)反应过程中的能量变化如下图所示。若生成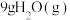 ,该反应会
,该反应会_____ (填“放出”或“吸收”)______ KJ热量。(用含有 、
、 的式子表示)
的式子表示) 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: 的浓度随时间变化曲线为
的浓度随时间变化曲线为_______ (填“a”、“b”或“c”),在M点,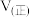
_______ 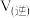 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
②2min时,反应速率改变的原因可能是_______ 。
A.升高温度 B.降低温度 C.充入一定量的 D.加入催化剂
D.加入催化剂
 、
、 、
、 都是重要的能源物质,也是重要的化工原料。
都是重要的能源物质,也是重要的化工原料。(1)下列事实能说明
 分子呈正四面体结构的是_______(填字母)。
分子呈正四面体结构的是_______(填字母)。A. 分子的4个C—H共价键键长相等 分子的4个C—H共价键键长相等 | B. 分子中每个键角都是109°28′ 分子中每个键角都是109°28′ |
C.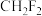 没有同分异构体 没有同分异构体 | D. 分子的沸点高于 分子的沸点高于 |
(2)甲烷与下列烃的通式相同的是
a. b.
b.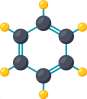 c.
c.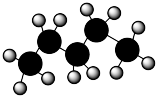 d.
d.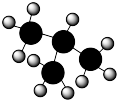
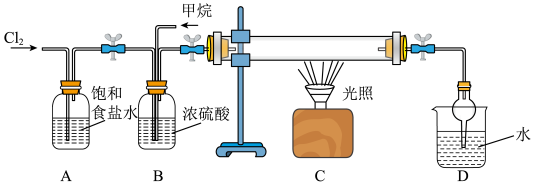
②写出装置C中
 与
与 反应生成氯仿(
反应生成氯仿( )的化学方程式
)的化学方程式③若
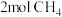 与
与 发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是
发生取代反应,测得生成4种有机取代产物的物质的量相等,则产物中最多的物质,其物质的量是Ⅱ.用
 还原
还原 能有效促进“碳中和”,反应的化学方程式为
能有效促进“碳中和”,反应的化学方程式为 。
。(4)反应过程中的能量变化如下图所示。若生成
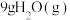 ,该反应会
,该反应会 、
、 的式子表示)
的式子表示)
 和
和 ,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题:
,反应过程中测得各物质的物质的量浓度随时间变化如图所示。回答下列问题: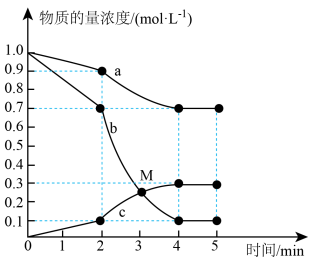
 的浓度随时间变化曲线为
的浓度随时间变化曲线为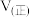
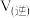 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。②2min时,反应速率改变的原因可能是
A.升高温度 B.降低温度 C.充入一定量的
 D.加入催化剂
D.加入催化剂
您最近一年使用:0次
名校
4 . 完成下列问题。
(1)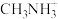 中H-N-H键角比
中H-N-H键角比 中H-N-H键角
中H-N-H键角___________ (填“大”或“小”)。
(2)正硝酸钠( )为白色晶体,是一种重要的化工原料。
)为白色晶体,是一种重要的化工原料。
① 阴离子的空间构型为
阴离子的空间构型为___________ ,其中心原子杂化方式为___________ 。
②写出一种与 的阴离子互为等电子体的阴离子或分子
的阴离子互为等电子体的阴离子或分子___________ (填化学式)。
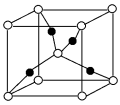
(3)①一个Cu2O晶胞(见图)中,Cu原子的数目为___________ 。
②Cu2O晶胞参数为anm,摩尔质量为M,求Cu2O的密度___________ g/cm3(只列出计算表达式)
(1)
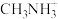 中H-N-H键角比
中H-N-H键角比 中H-N-H键角
中H-N-H键角(2)正硝酸钠(
 )为白色晶体,是一种重要的化工原料。
)为白色晶体,是一种重要的化工原料。①
 阴离子的空间构型为
阴离子的空间构型为②写出一种与
 的阴离子互为等电子体的阴离子或分子
的阴离子互为等电子体的阴离子或分子(3)①一个Cu2O晶胞(见图)中,Cu原子的数目为
②Cu2O晶胞参数为anm,摩尔质量为M,求Cu2O的密度
您最近一年使用:0次
名校
解题方法
5 . 处理工业废气中的氮氧化物NOx对于环境保护具有重要的意义。
(1)催化还原法。NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:_______ 。
②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=______ 。按最佳脱氮率,每生成2molN2,转移电子数目为_______ 。
(2)可用NaClO2将氮氧化物转化成NO ,碱性条件下NaClO2去除NO反应的离子方程式为
,碱性条件下NaClO2去除NO反应的离子方程式为_______ 。
(3)对NO和NO2脱除后产生的含NO 溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为_______ 。
(1)催化还原法。NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示:

②用Fe做催化剂时,在氨气足量的情况下,不同c(NO2)/c(NO)对应的脱氮率如图2所示,脱氮效果最佳的c(NO2)/c(NO)=
(2)可用NaClO2将氮氧化物转化成NO
 ,碱性条件下NaClO2去除NO反应的离子方程式为
,碱性条件下NaClO2去除NO反应的离子方程式为(3)对NO和NO2脱除后产生的含NO
 溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
溶液可用如图装置在弱酸性条件下进行电化学环保处理。碳电极上的电极反应式为
您最近一年使用:0次
名校
6 . 随着“碳达峰”、“碳中和”战略的提出,大气中CO2含量的控制和回收利用已成为当今化学研究的主题。
(1)科学家以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。______ 转化为______ 。过程①中TiO2发生了______ 反应(填“氧化”或“还原”)。根据数据计算,分解2molCO2需吸收______ kJ的能量。
(2)利用光解海水产生的H2将CO2转化为甲醇有利于减少温室气体二氧化碳排放,反应的化学方程式:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是
CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是______ (填标号)。
(3)某温度下,向2L的恒容密闭容器充入6molCO2和8molH2,发生反应CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。______ mol•L-1•min-1;4min时,v正(H2)______ (填“>”“<”或“=”)v逆(H2)。
②能作为反应达到平衡状态的依据的是______ (填序号)。
a.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
b.容器内混合气体的密度不再改变
c.容器内总压强不再改变
d.单位时间内断裂3mol的H-H键,同时生成1mol的C=O键
(1)科学家以TiO2为催化剂的光热化学循环分解CO2反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
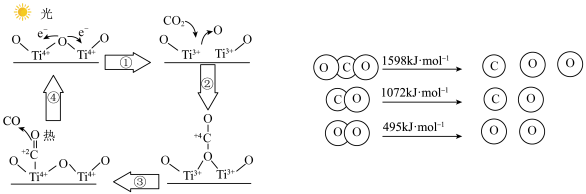
(2)利用光解海水产生的H2将CO2转化为甲醇有利于减少温室气体二氧化碳排放,反应的化学方程式:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是
CH3OH(g)+H2O(g) △H<0。下列措施不能提高该反应的速率的是| A.减小容器体积 | B.升高温度 |
| C.使用合适催化剂 | D.恒容条件下充入He |
(3)某温度下,向2L的恒容密闭容器充入6molCO2和8molH2,发生反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。
CH3OH(g)+H2O(g),测得H2物质的量随时间变化如图所示。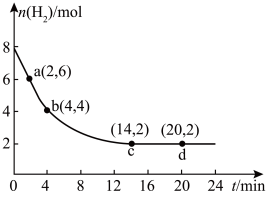
②能作为反应达到平衡状态的依据的是
a.c(CO2):c(H2):c(CH3OH):c(H2O)=1:3:1:1
b.容器内混合气体的密度不再改变
c.容器内总压强不再改变
d.单位时间内断裂3mol的H-H键,同时生成1mol的C=O键
您最近一年使用:0次
名校
解题方法
7 . 氮的化合物广泛应用于工业、航天、医药等领域。
(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的 和
和 。在一定条件下发生反应:
。在一定条件下发生反应: 。该反应已达到平衡状态的标志是
。该反应已达到平衡状态的标志是_______ 。
a.12
 键断裂的同时生成5
键断裂的同时生成5
 键
键
b.容器内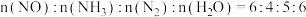
c.容器内 的物质的量分数不再变化
的物质的量分数不再变化
d.混合气体的平均相对分子质量不再改变
(2)肼( )是火箭推进器中常用的高能燃料,已知0.4
)是火箭推进器中常用的高能燃料,已知0.4 液态肼和足量
液态肼和足量 反应,生成
反应,生成 和水蒸气,放出256.65
和水蒸气,放出256.65 的热量,请写出该反应的热化学方程式:
的热量,请写出该反应的热化学方程式:_______ 。
(3)一定条件下,在5L密闭容器内,反应 ,
, 的物质的量随时间变化如表:
的物质的量随时间变化如表:
①用 表示0~2s内该反应的平均速率为
表示0~2s内该反应的平均速率为_______ 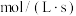 ,在第5s时,
,在第5s时, 的转化率为
的转化率为_______ 。
②为加快反应速率,可以采取的措施是_______ 。
a.升高温度 b.恒容时充入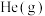 c.恒压时充入
c.恒压时充入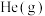 d.恒容时充入
d.恒容时充入
(4)已知: ,不同温度(T)下,
,不同温度(T)下, 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
_______  (填“>”、“=”或“<")。当温度为T、起始压强为
(填“>”、“=”或“<")。当温度为T、起始压强为 ,反应至
,反应至 min时,此时体系压强
min时,此时体系压强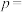
_______ (用 表示)。
表示)。
(1)氨气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的
 和
和 。在一定条件下发生反应:
。在一定条件下发生反应: 。该反应已达到平衡状态的标志是
。该反应已达到平衡状态的标志是a.12

 键断裂的同时生成5
键断裂的同时生成5
 键
键b.容器内
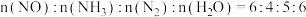
c.容器内
 的物质的量分数不再变化
的物质的量分数不再变化d.混合气体的平均相对分子质量不再改变
(2)肼(
 )是火箭推进器中常用的高能燃料,已知0.4
)是火箭推进器中常用的高能燃料,已知0.4 液态肼和足量
液态肼和足量 反应,生成
反应,生成 和水蒸气,放出256.65
和水蒸气,放出256.65 的热量,请写出该反应的热化学方程式:
的热量,请写出该反应的热化学方程式:(3)一定条件下,在5L密闭容器内,反应
 ,
, 的物质的量随时间变化如表:
的物质的量随时间变化如表:时间/s | 0 | 1 | 2 | 3 | 5 | 4 |
| 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
 表示0~2s内该反应的平均速率为
表示0~2s内该反应的平均速率为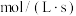 ,在第5s时,
,在第5s时, 的转化率为
的转化率为②为加快反应速率,可以采取的措施是
a.升高温度 b.恒容时充入
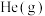 c.恒压时充入
c.恒压时充入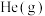 d.恒容时充入
d.恒容时充入
(4)已知:
 ,不同温度(T)下,
,不同温度(T)下, 分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度
分解半衰期随起始压强的变化关系如图所示(图中半衰期指任一浓度 消耗一半时所需的相应时间),则
消耗一半时所需的相应时间),则
 (填“>”、“=”或“<")。当温度为T、起始压强为
(填“>”、“=”或“<")。当温度为T、起始压强为 ,反应至
,反应至 min时,此时体系压强
min时,此时体系压强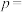
 表示)。
表示)。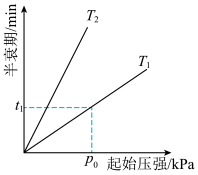
您最近一年使用:0次
名校
解题方法
8 . 人们应用原电池原理制作了多种电池,以满足不同的需要。请回答下列问题。
(1)请你利用下列反应 设计一个化学电池,该电池的负极材料是
设计一个化学电池,该电池的负极材料是_______ ,电解质溶液是_______ 。
(2)“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。在紧急状况下,应急电池会自动启动,工作原理为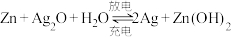 ,其正极的电极反应式为
,其正极的电极反应式为_______ 。
(3)目前正在研发的高能量密度燃料电池车,是以肼( )燃料电池作为动力来源,电池结构如图所示。
)燃料电池作为动力来源,电池结构如图所示。 溶液浓度相同,工作一段时间后,
溶液浓度相同,工作一段时间后, 浓度较大的是
浓度较大的是_______ (填“正”或“负”)极区。
②该电池负极的电极反应式为_______ 。
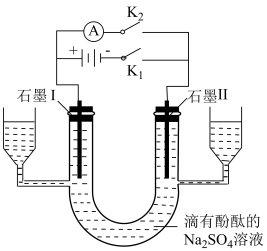
(4)利用如图所示装置探究氢氧燃料电池的工作原理。 、
、 :打开
:打开 ,闭合
,闭合 ,连接电池负极的石墨Ⅱ为
,连接电池负极的石墨Ⅱ为_______ (填“阳极”或“阴极”),阳极的电极反应式为_______ ;_______ (填“石墨Ⅰ”或“石墨Ⅱ”)附近的溶液变红。
②探究燃料电池的工作原理:在上述实验①结束后,立即打开 ,闭合
,闭合 ,可以观察到电流表指针偏转,则外电路中电子的流动方向是
,可以观察到电流表指针偏转,则外电路中电子的流动方向是_______ (填“石墨Ⅱ流向石墨Ⅰ”或“石墨Ⅰ流向石墨Ⅱ”);负极的电极反应式是_______ 。
(1)请你利用下列反应
 设计一个化学电池,该电池的负极材料是
设计一个化学电池,该电池的负极材料是(2)“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。在紧急状况下,应急电池会自动启动,工作原理为
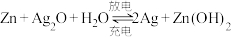 ,其正极的电极反应式为
,其正极的电极反应式为(3)目前正在研发的高能量密度燃料电池车,是以肼(
 )燃料电池作为动力来源,电池结构如图所示。
)燃料电池作为动力来源,电池结构如图所示。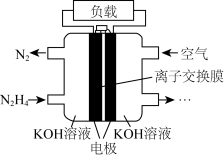
 溶液浓度相同,工作一段时间后,
溶液浓度相同,工作一段时间后, 浓度较大的是
浓度较大的是②该电池负极的电极反应式为
(4)利用如图所示装置探究氢氧燃料电池的工作原理。
 、
、 :打开
:打开 ,闭合
,闭合 ,连接电池负极的石墨Ⅱ为
,连接电池负极的石墨Ⅱ为②探究燃料电池的工作原理:在上述实验①结束后,立即打开
 ,闭合
,闭合 ,可以观察到电流表指针偏转,则外电路中电子的流动方向是
,可以观察到电流表指针偏转,则外电路中电子的流动方向是
您最近一年使用:0次
名校
解题方法
9 . 按要求完成下列问题。
(1)下列物质组合中,互为同系物关系的是___________。
(2)乙酰水杨酸分子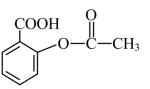 中含有的官能团的名称是
中含有的官能团的名称是___________ 。
(3)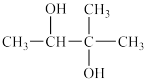 的系统命名法名称
的系统命名法名称___________ 。
(4)请写出2,4-二甲基-2-戊烯的键线式:___________ 。
(5)乙醛与新制氢氧化铜悬浊液反应的化学方程式:___________ 。
(6)HOCH2CH2OH和HOOCCOOH在一定条件下发生缩聚反应的化学方程式:___________ 。
(1)下列物质组合中,互为同系物关系的是___________。
A. 和 和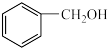 | B.乙二醇和甘油 |
| C.甲苯和对二甲苯 | D.2,2-二甲基丙烷和新戊烷 |
 中含有的官能团的名称是
中含有的官能团的名称是(3)
 的系统命名法名称
的系统命名法名称(4)请写出2,4-二甲基-2-戊烯的键线式:
(5)乙醛与新制氢氧化铜悬浊液反应的化学方程式:
(6)HOCH2CH2OH和HOOCCOOH在一定条件下发生缩聚反应的化学方程式:
您最近一年使用:0次
名校
10 . 按要求回答下列各题:
(1)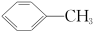 的一溴代物有
的一溴代物有___________ 种。
(2)茅苍术醇(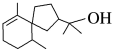 )的分子式为
)的分子式为_________ ,所含官能团名称为_________ 。
(3)用系统命名法命名物质 :
:___________ ;
(4)环癸五烯分子结构可表示为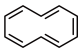 。环癸五烯具有的性质有
。环癸五烯具有的性质有___________ 。
a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(5)写出 的一种同分异构体的结构简式:
的一种同分异构体的结构简式:___________ 。
(6)某物质只含 、
、 、
、 三种元素,其分子的球棍模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)
三种元素,其分子的球棍模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)___________ 。
②下列物质中,与该物质互为同分异构体的是___________ (填字母)。
A.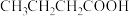 B.
B.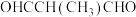
C.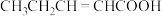 D.
D.
③该分子中共平面的原子个数最多为___________ 个(已知羧基的四个原子可以共平面)。
④该物质与 反应的化学方程式为
反应的化学方程式为___________ 。
(1)
 的一溴代物有
的一溴代物有(2)茅苍术醇(
 )的分子式为
)的分子式为(3)用系统命名法命名物质
 :
:(4)环癸五烯分子结构可表示为
 。环癸五烯具有的性质有
。环癸五烯具有的性质有a.能溶于水 b.能发生氧化反应 c.能发生加成反应 d.常温常压下为气体
(5)写出
 的一种同分异构体的结构简式:
的一种同分异构体的结构简式:(6)某物质只含
 、
、 、
、 三种元素,其分子的球棍模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)
三种元素,其分子的球棍模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)
②下列物质中,与该物质互为同分异构体的是
A.
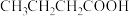 B.
B.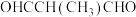
C.
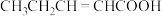 D.
D.
③该分子中共平面的原子个数最多为
④该物质与
 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次