1 . 可利用干法热分解法和湿法催化氧化法高效脱除沼气中的 。
。
(1)已知:部分键能数据为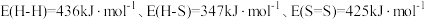 。
。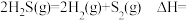
___________  。
。
(2)干法热分解法原理为 。向体积为
。向体积为 恒容容器中充入
恒容容器中充入 ,初始压强为
,初始压强为 ,平衡时体系中各物质
,平衡时体系中各物质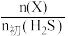 随温度t的变化如图。
随温度t的变化如图。 对应图中的曲线是
对应图中的曲线是___________ (填字母),结合平衡移动原理说明理由。___________
②t1℃时, 的平衡转化率为
的平衡转化率为___________ ,分压平衡常数
___________ (以分压表示,分压=总压×物质的量分数,列计算式即可)。
(3)湿法催化氧化法高效脱除 的过程如下。
的过程如下。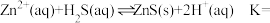
___________ 。(已知:25℃时, 的
的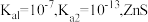 的
的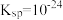 )
)
②“氧化沉硫”中发生反应的离子方程式有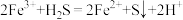 、
、___________ 。
③ 对脱硫效率影响如图。随着
对脱硫效率影响如图。随着 增大,脱硫效率趋于平缓的原因是
增大,脱硫效率趋于平缓的原因是___________ 。___________ (填化学式)。
(4)相比湿法催化氧化法,干法热分解法的优点是___________ ,缺点是___________ 。
 。
。(1)已知:部分键能数据为
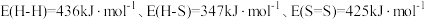 。
。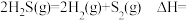
 。
。(2)干法热分解法原理为
 。向体积为
。向体积为 恒容容器中充入
恒容容器中充入 ,初始压强为
,初始压强为 ,平衡时体系中各物质
,平衡时体系中各物质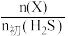 随温度t的变化如图。
随温度t的变化如图。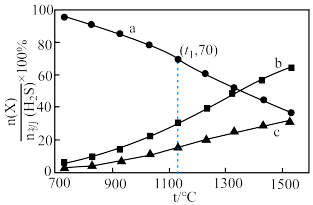
 对应图中的曲线是
对应图中的曲线是②t1℃时,
 的平衡转化率为
的平衡转化率为
(3)湿法催化氧化法高效脱除
 的过程如下。
的过程如下。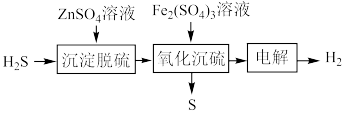
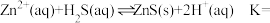
 的
的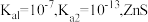 的
的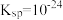 )
)②“氧化沉硫”中发生反应的离子方程式有
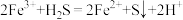 、
、③
 对脱硫效率影响如图。随着
对脱硫效率影响如图。随着 增大,脱硫效率趋于平缓的原因是
增大,脱硫效率趋于平缓的原因是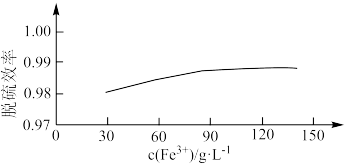
(4)相比湿法催化氧化法,干法热分解法的优点是
您最近一年使用:0次
2 . 利用某阳极泥(含 和
和 单质)回收贵金属
单质)回收贵金属 并合成高能量密度材料
并合成高能量密度材料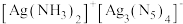 的工艺流程如下。
的工艺流程如下。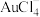 的离子方程式为
的离子方程式为___________ 。
(2)“还原”过程发生反应的化学方程式为___________ 。
(3)溶液中含银微粒的物质的量分数随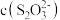 的变化如图。
的变化如图。 ,应调节
,应调节 最佳浓度为
最佳浓度为___________  。
。
②25℃时, 的
的 ,
, 的
的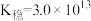 ,
,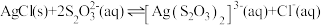 的平衡常数
的平衡常数
___________ 。
(4)“电解”过程生成 的电极反应式为
的电极反应式为___________ 。
(5)“溶解”过程可提高溶解速率的措施有___________ (填1条)。
(6)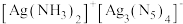 晶体的局部结构如图。
晶体的局部结构如图。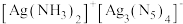 晶体中存在的微粒间作用力有
晶体中存在的微粒间作用力有___________ (填标号)。
A.离子键 B. 键 C.
键 C. 键 D.金属键 E.氢键
键 D.金属键 E.氢键
②晶体中 的杂化轨道类型
的杂化轨道类型___________ (填“相同”或“不同”),依据是___________ 。
 和
和 单质)回收贵金属
单质)回收贵金属 并合成高能量密度材料
并合成高能量密度材料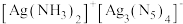 的工艺流程如下。
的工艺流程如下。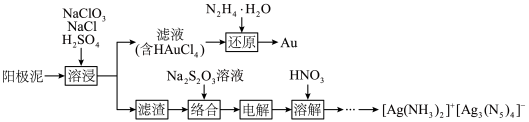
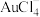 的离子方程式为
的离子方程式为(2)“还原”过程发生反应的化学方程式为
(3)溶液中含银微粒的物质的量分数随
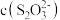 的变化如图。
的变化如图。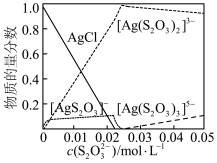
 ,应调节
,应调节 最佳浓度为
最佳浓度为 。
。②25℃时,
 的
的 ,
, 的
的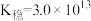 ,
,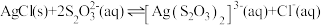 的平衡常数
的平衡常数
(4)“电解”过程生成
 的电极反应式为
的电极反应式为(5)“溶解”过程可提高溶解速率的措施有
(6)
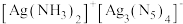 晶体的局部结构如图。
晶体的局部结构如图。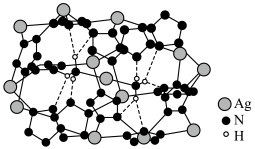
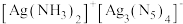 晶体中存在的微粒间作用力有
晶体中存在的微粒间作用力有A.离子键 B.
 键 C.
键 C. 键 D.金属键 E.氢键
键 D.金属键 E.氢键②晶体中
 的杂化轨道类型
的杂化轨道类型
您最近一年使用:0次
名校
3 . 部分短周期主族元素原子半径与原子序数的关系如图,根据所学知识回答下列问题。 、
、 、
、 、
、 四种元素的最简单氢化物中,最稳定的是
四种元素的最简单氢化物中,最稳定的是________ (填化学式)。
(2) 与
与 能形成一种淡黄色的物质,其电子式为
能形成一种淡黄色的物质,其电子式为________ 。
(3) 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 的最高价氧化物对应的水化物反应的离子方程式为
的最高价氧化物对应的水化物反应的离子方程式为________ 。
(4)由 的单质制成的电池需要注意防水,其原因为
的单质制成的电池需要注意防水,其原因为________ (用化学方程式表示)。
(5)门捷列卡在研究元素周期表时,科学地预言了11种当时尚未发现的元素,他认为 的下一周期存在一种“类
的下一周期存在一种“类 ”元素,该元素多年后被法国化学家发现,命名为镓(Ga),镓在元素周期表中的位置为
”元素,该元素多年后被法国化学家发现,命名为镓(Ga),镓在元素周期表中的位置为________ 。预测 与
与 的最高价氧化物对应水化物的碱性较强的是
的最高价氧化物对应水化物的碱性较强的是________ (填最高价氧化物对应水化物的化学式)。
(6)使用下列装置再添加合适的药品,可以证明 和
和 两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸②稀硫酸③盐酸④
两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸②稀硫酸③盐酸④ 固体⑤
固体⑤ ⑥澄清石灰水⑦NaOH溶液
⑥澄清石灰水⑦NaOH溶液________ 、丁________ 。
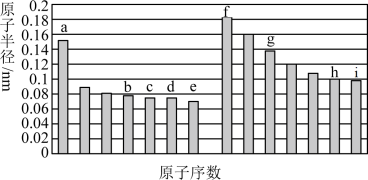
 、
、 、
、 、
、 四种元素的最简单氢化物中,最稳定的是
四种元素的最简单氢化物中,最稳定的是(2)
 与
与 能形成一种淡黄色的物质,其电子式为
能形成一种淡黄色的物质,其电子式为(3)
 的最高价氧化物对应的水化物与
的最高价氧化物对应的水化物与 的最高价氧化物对应的水化物反应的离子方程式为
的最高价氧化物对应的水化物反应的离子方程式为(4)由
 的单质制成的电池需要注意防水,其原因为
的单质制成的电池需要注意防水,其原因为(5)门捷列卡在研究元素周期表时,科学地预言了11种当时尚未发现的元素,他认为
 的下一周期存在一种“类
的下一周期存在一种“类 ”元素,该元素多年后被法国化学家发现,命名为镓(Ga),镓在元素周期表中的位置为
”元素,该元素多年后被法国化学家发现,命名为镓(Ga),镓在元素周期表中的位置为 与
与 的最高价氧化物对应水化物的碱性较强的是
的最高价氧化物对应水化物的碱性较强的是(6)使用下列装置再添加合适的药品,可以证明
 和
和 两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸②稀硫酸③盐酸④
两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸②稀硫酸③盐酸④ 固体⑤
固体⑤ ⑥澄清石灰水⑦NaOH溶液
⑥澄清石灰水⑦NaOH溶液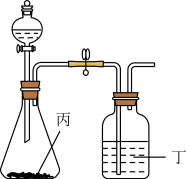
您最近一年使用:0次
名校
4 . 近期我国科技工作者开发了高效 催化净化(脱硝)催化剂,实现
催化净化(脱硝)催化剂,实现 减排,其催化原理如图所示(“□”代表氧原子空位)。下列说法错误的是
减排,其催化原理如图所示(“□”代表氧原子空位)。下列说法错误的是
 催化净化(脱硝)催化剂,实现
催化净化(脱硝)催化剂,实现 减排,其催化原理如图所示(“□”代表氧原子空位)。下列说法错误的是
减排,其催化原理如图所示(“□”代表氧原子空位)。下列说法错误的是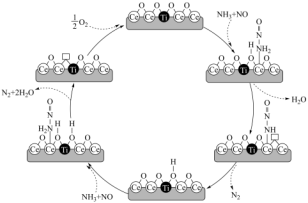
| A.反应过程中涉及O-H的断裂和生成 |
| B.整个过程中Ce原子的化合价发生了改变 |
C.N元素位于元素周期表的第2周期第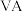 族 族 |
D.催化循环的总反应为: |
您最近一年使用:0次
名校
5 . 辉钼精矿主要成分是二硫化钼( ),还含有石灰石(
),还含有石灰石( )、石英(
)、石英( )、黄铜矿(
)、黄铜矿( )等杂质。某学习小组设计提取
)等杂质。某学习小组设计提取 的过程如下,下列说法错误的是:
的过程如下,下列说法错误的是:
 ),还含有石灰石(
),还含有石灰石( )、石英(
)、石英( )、黄铜矿(
)、黄铜矿( )等杂质。某学习小组设计提取
)等杂质。某学习小组设计提取 的过程如下,下列说法错误的是:
的过程如下,下列说法错误的是:
| A.为加快辉钼精矿溶解,可将矿石粉碎并适当加热 |
B.滤液中含 、 、 、 、 、 、 、 、 等阳离子 等阳离子 |
| C.以上①②③过程中涉及化学反应均为氧化还原反应 |
D.步骤③温度不宜过高,以免 被氧化 被氧化 |
您最近一年使用:0次
名校
6 . 某化学兴趣小组同学进行如下实验:①分别向 溶液和
溶液和 溶液中滴加KSCN溶液,均无明显现象。②向
溶液中滴加KSCN溶液,均无明显现象。②向 和
和 的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质;
的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质; 为无色离子;
为无色离子; 为深蓝色离子。下列说法不正确的是
为深蓝色离子。下列说法不正确的是
 溶液和
溶液和 溶液中滴加KSCN溶液,均无明显现象。②向
溶液中滴加KSCN溶液,均无明显现象。②向 和
和 的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质;
的混合液中滴加少量KSCN溶液,溶液立刻变红,振荡后,红色褪去,产生白色沉淀,继续滴加过量KSCN溶液,红色不再褪去,并产生大量白色沉淀。③过滤②中白色沉淀并洗涤干净,向其中加入过量氨水,白色沉淀溶解得无色溶液,放置过程中,无色溶液变蓝色。已知:CuSCN为白色、难溶性物质; 为无色离子;
为无色离子; 为深蓝色离子。下列说法不正确的是
为深蓝色离子。下列说法不正确的是A.实验①说明 不能与SCN反应生成CuSCN 不能与SCN反应生成CuSCN |
B.实验②中红色褪去的原因是振荡后 降低 降低 |
C.实验③中无色溶液变蓝色的原因是: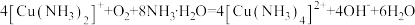 |
D.依据实验①、②、③推测,②中由于生成CuSCN,使 氧化性增强,将 氧化性增强,将 氧化为 氧化为 |
您最近一年使用:0次
名校
7 . 在锌与某浓度的稀盐酸(足量)反应的实验中,得到如下结果:
下列说法中正确的是
① ②
② 和
和 均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量
均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量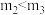 ④若锌均未完全反应,则在相同时间内,产生
④若锌均未完全反应,则在相同时间内,产生 的体积
的体积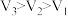
| 序号 | 锌的质量/g | 锌的形式 | 温度/℃ | 锌完全反应所需时间/s | 产生 的体积 的体积 |
| 1 | 2 | 薄片 | 15 | 200 |  |
| 2 | 2 | 粉末 | 15 |  |  |
| 3 | 2 | 粉末 | 35 |  |  |
①
 ②
② 和
和 均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量
均小于200 ③实验2和实验3比较,单位时间内消耗的锌的质量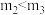 ④若锌均未完全反应,则在相同时间内,产生
④若锌均未完全反应,则在相同时间内,产生 的体积
的体积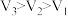
| A.①② | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
名校
8 . 下列有关反应的离子方程式正确的是
A. 通入水中: 通入水中: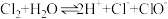 |
B. 溶液中加入过量氨水: 溶液中加入过量氨水: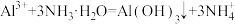 |
C. 溶液中加 溶液中加 ,紫色褪去: ,紫色褪去: |
D.少量 气体通入NaClO溶液中: 气体通入NaClO溶液中: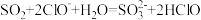 |
您最近一年使用:0次
名校
9 .  为阿伏加德罗常数的值。下列叙述不正确的是
为阿伏加德罗常数的值。下列叙述不正确的是
 为阿伏加德罗常数的值。下列叙述不正确的是
为阿伏加德罗常数的值。下列叙述不正确的是A.含2mol 的浓硫酸与足量铜在加热条件下反应,生成的 的浓硫酸与足量铜在加热条件下反应,生成的 少于1 少于1 |
B.标况下,1molFe粉与足量的S粉加热充分反应,转移电子数为 |
C.用金属铁、Cu片、稀硫酸组成原电池,当金属铁质量减轻5.6g时,正极产生2.24L |
D.1mol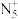 含有的电子数为 含有的电子数为 |
您最近一年使用:0次
名校
10 . 下列物质中既能与稀硫酸反应产生气体,又能与氢氧化钠溶液(允许加热)反应产生气体的是:①Al ② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
 ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦
| A.①⑤⑥ | B.①③⑤⑥ | C.①③⑤⑥⑦ | D.①②③④⑤⑥⑦ |
您最近一年使用:0次



